
【题目】某NaOH样品中含有少量Na2CO3、NaHCO3和H2O,经分析测定,其中含NaOH83.4%(质量分数,下同), NaHCO3 8.8%,Na2CO3 6.4%,H2O 1.4%。将此样品若干克投入到49克21%的稀硫酸中,待反应完全后,需加入20克9.0%的NaOH溶液方能恰好中和。则蒸发中和后的溶液可得固体质量接近于
A. 25 B. 20 C. 15 D. 10
 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案科目:高中化学 来源: 题型:
【题目】某一反应体系有反应物和生成物共七种物质:O2,KMnO4,MnSO4,H2SO4,H2O,H2O2,K2SO4,已知H2O2只发生反应H2O2→O2,回答下列问题:
(1)该反应的氧化剂是________。
(2)氧化剂与还原剂的物质的量之比______________。
(3)若反应转移了0.3mol电子,则在标况下生成气体体积___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列浓度关系正确的是
A.0.1 mol/L的NH4HSO4溶液中滴加0.1 mol/L的Ba(OH)2溶液至沉淀刚好完全:c (NH4+)>c (OH-)>c (SO42-)>c (H+)
B.0.1 mol/L的KOH溶液中通入标准状况下的CO2气体3.36 L,所得溶液中:c (K+)+c (H+)=c (CO32-)+c (HCO3-)+c (OH-)
C.0.1 mol/L的NaOH溶液与0.2 mol/L的HCN溶液等体积混合,所得溶液呈碱性:c (HCN)>c (Na+)>c (CN-)>c (OH-)>c (H+)
D.pH相同的NaOH溶液、CH3COONa溶液、Na2CO3溶液、NaHCO3溶液的浓度:c (NaOH)<c (CH3COONa)<c (NaHCO3)<c (Na2CO3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请回答以下问题:
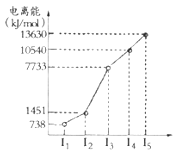
(1)第四周期的某主族元素,其第一至五电离能数据如图所示,则该元素对应原子的M层电子排布式为____________。
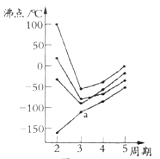
(2)如图所示,每条折线表示周期表ⅣA-ⅦA中的某一族元素氢化物的沸点变化.每个小黑点代表一种氢化物,其中a点代表的是______。
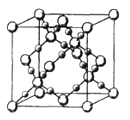
(3)CO2在高温高压下所形成的晶体其晶胞如图所示.该晶体的熔点比SiO2晶体________(填“高”或“低”),该晶体中碳原子轨道的杂化类型为______。
(4)化合物(CH3)3N与盐酸反应生成[(CH3)3NH]+,该过程新生成的化学键为____(填序号)。
A.离子键 B.配位键 C.氢键 D.非极性共价键
若化合物(CH3)3N能溶于水,试解释其原因:_________________________。
(5)一种新型储氢化合物A是乙烷的等电子体,其相对分子质量为30.8,且A是由第二周期两种氢化物形成的化合物。加热A会慢慢释放氢气,同时A转化为化合物B,B是乙烯的等电子体。化合物A的结构式为__________________(若含有配位键,要求用箭头表示)
(6)PCl5是一种白色晶体,在恒容密闭容器中加热可在148 ℃液化,形成一种能导电的熔体,测得其中含有一种正四面体形阳离子和一种正八面体形阴离子,熔体中P-Cl的键长只有198 nm和206 nm两种,这两种离子的化学式为______________________;正四面体形阳离子中键角小于PCl3的键角原因为_____________________________;若PBr5气态分子的结构与PCl5相似,它的熔体也能导电,经测定知其中只存在一种P-Br键长,试用电离方程式解释PBr5熔体能导电的原因______________________。
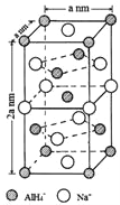
(7)氢化铝钠(NaAlH4)是一种新型轻质材料, NaAlH4可由AlCl3和NaH在适当条件下合成。NaAlH4的晶胞结构如下图所示。NaAlH4晶体中,与Na+紧邻且等距的AlH4- 有_________个;NaAlH4晶体的密度为___________g·cm-3(用含a的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】质子核磁共振谱是研究有机化合物结构的有力手段之一。结构中的等效氢原子核磁共振谱中都给出了相应的峰值(信号),谱中峰的强度与结构中的H原子数成正比。试回答:
(1)结构简式为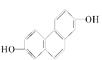 的有机化合物,在核磁共振谱中观察峰给出的强度之比为___________。
的有机化合物,在核磁共振谱中观察峰给出的强度之比为___________。
(2)实践中可根据核共振谱上观察到H原子给出的峰值情况,确定有机化合物的结构。分子式为C3H6O2的链状有机化合物核磁共振谱上峰给出的稳定强度仅有四种,它们分别是①3∶3,②3∶2∶1,③3∶1∶1∶1,④1∶2∶2∶1。
请分别推断出其对应的结构简式:
①________________________; ② ___________________________;
③________________________; ④ ___________________________。
(3)测得CH3CH2CH2CH3化合物核磁共振谱上可观察到两种峰,而CH3CH=CHCH3的核磁共振谱有4种峰,结合其空间结构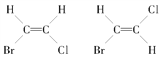 ,解释产生4个峰的原因:_______________。
,解释产生4个峰的原因:_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为配制480 mL 0.2 mol·L-1 NaCl溶液的示意图。

回答下列问题:
(1)在容量瓶的使用方法中,下列操作不正确的是________(填字母)。
A.使用容量瓶前检查它是否漏水
B.容量瓶用蒸馏水洗净后,再用待配溶液润洗
C.配制溶液时,如果试样是固体,把称好的试样用纸条小心倒入容量瓶中,缓慢加入蒸馏水到接近刻度线1~2 cm处,用胶头滴管滴加蒸馏水到刻度线
D.溶解过程中,要等烧杯中溶液冷却到室温再转入容量瓶
(2)①中应称NaCl________ g;②选择容量瓶的规格____________。
(3)玻璃棒在②、③两步中的作用分别是____________________________、____________________________。
(4)若出现如下情况,对所配溶液浓度有何影响?(填“偏高”“偏低”或“无影响”)
A.某同学在第①步称量时物品和砝码放反了 ________。
B.某同学在第⑧步观察液面时仰视________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某离子晶体晶胞如图所示,其摩尔质量为M,阿伏加德罗常数为NA,晶体的密度为d g/cm3。下列说法中正确的是( )

A. 晶体晶胞中阴、阳离子的个数都为1
B. 其中阴、阳离子的配位数都是4
C. 该晶胞可能是NaCl的晶胞
D. 该晶体中两个距离最近的阳离子的核间距为![]() cm
cm
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com