
����Ŀ��������������ѧ��������ش��������⡣
��1�������еĵ�ζƷ�У�����(��Ҫ�ɷ��Ȼ���)���ڼ���(��Ҫ�ɷ�̼����)���۰״�(��Ҫ�ɷ�����)�����������ʷֱ�����ˮ����ˮ��Һ���м��Ե���______(����ţ���ͬ)����Ҫ�ɷ��������������________������ܷ�����Ӧ����______��
��2�������������������⣬���漰����ѧ�仯����________��
�������Ȼ�̼�ɲ�ȥԲ����� ������ˮ����Һ������ �ۿ���ʳ��ϴ��ˮ��
��3����ǰ�����������ѳ�Ϊ��Ҫ���������̡�
���ҹ����з����ġ����������ձ����У��������ʲ�������Ҫ��Ⱦ�����_____������ĸ���ţ���
A���������� B��������̼ C���������� D�������������
��úֱ̿��ȼ�ջ�������ֻ������⡣ȼú������SO2�ǵ���______�������ƣ���Ⱦ�����γɵ�ԭ������CO��SO2�̵�����Ⱦ��һ�ַ����ǽ����ڴ���������ת��Ϊ����S��������Ӧ�Ļ�ѧ����ʽΪ_____________________��
��4������ǵ�ˮ�м�������KAl(SO4)212H2O��ˮ�ɵõ�������д��������ˮ�еĵ��뷽��ʽ___����������Һ����μ���Ba(OH)2��Һֱ��Al3+ǡ�ó�����ȫ��������Ӧ�����ӷ���ʽΪ_______��
���𰸡��� �٢� �ڢ� �� B ���� 2CO+SO2 2CO2+S KAl(SO4)2=K++Al3++2SO42- ����KAl(SO4)2��12H2O=K++Al3++2SO42- +12H2O 2Al3++3Ba2++6OH-+3SO42-=2Al(OH)3��+3BaSO4��
2CO2+S KAl(SO4)2=K++Al3++2SO42- ����KAl(SO4)2��12H2O=K++Al3++2SO42- +12H2O 2Al3++3Ba2++6OH-+3SO42-=2Al(OH)3��+3BaSO4��
��������
(1)ˮ��Һ���м��Ե������Ǽ��ˮ���Լ��Ե��Σ����������Ӻ���������ӹ��̵Ļ�����Ϊ�Σ�̼���ƺ����ᷴӦ���ɴ����ơ�������̼��ˮ��
(2)�����������ɵı仯Ϊ��ѧ�仯��
(3)�ٿ��������ձ����漰����Ⱦ���ж�������(SO2)����������(NO2)�������������ȣ�
��ȼú������SO2������������������γɣ�һ����̼����������ڴ��������·�Ӧ���ɵ�����Ͷ�����̼��
(4)������ˮ��Һ�е�������Al3+��SO42-������KAl(SO4)2Ϊ2mol����Al3+ǡ��ȫ������ʱ����Ҫ3molBa(OH)2�����ݸ����ӵ����ʵ����жϷ�Ӧ�ij̶ȣ��Դ���д���ӷ���ʽ��
(1)�����еĵ�ζƷ������(��Ҫ�ɷ��Ȼ���)���ڼ���(��Ҫ�ɷ�̼����)���۰״�(��Ҫ�ɷ�����)�����������ʷֱ�����ˮ����ˮ��Һ���м��Ե��Ǣڼ���(��Ҫ�ɷ�̼����)��̼�������ˮ����Һ�Լ��ԣ���Ҫ�ɷ�������������Ǣ���(��Ҫ�ɷ��Ȼ���)���ڼ���(��Ҫ�ɷ�̼����)�����Ӧ��������̼���ƺ����ᷴӦ���ɴ����ơ�������̼��ˮ��
�ʴ�Ϊ���ڣ��٢ڣ��ڢۣ�
(2)�������Ȼ�̼�ɲ�ȥԲ����ͣ�������������ԭ���������������ɣ����������仯����ѡ��
������ˮ����Һ������������������ˮ��Ӧ���ɾ���ǿ�����Դ����ᣬ�����������ɣ��ǻ�ѧ�仯���ʲ�ѡ��
�ۿ���ʳ��ϴ��ˮ����������̼��ƣ�������þ��Ӧ���ɿ����Դ����Σ������������ɣ��ǻ�ѧ�仯���ʲ�ѡ��
��ѡ���٣�
(3)�ٿ��������ձ����漰����Ⱦ���ж�������(SO2)����������(NO2)�������������ȣ�������̼Ϊ������ɳɷ֣���������Ⱦ�
��ѡ��B��
��ȼú������SO2������������������γɣ�һ����̼����������ڴ��������·�Ӧ���ɵ�����Ͷ�����̼������ʽ��2CO+SO2 2CO2+S��
2CO2+S��
�ʴ�Ϊ�����ꣻ2CO+SO2 2CO2+S��
2CO2+S��
(4)������ˮ��Һ�е�������Al3+��SO42-�����뷽��ʽΪKAl(SO4)2=K++Al3++2SO42-������KAl(SO4)2Ϊ2mol����Һ�к���2molAl3+��4molSO42-����Al3+ǡ��ȫ������ʱ����Ҫ3molBa(OH)2��������3molBa2+��6molOH-����Ӧ�����ӷ���ʽΪ2Al3++3SO42-+3Ba2++6OH-=3BaSO4��+2Al(OH)3����
�ʴ�Ϊ��KAl(SO4)2=K++Al3++2SO42-��2Al3++3SO42-+3Ba2++6OH-=3BaSO4��+2Al(OH)3����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25�桢101KPaʱ��agNH3��bgCH4�������ͬ��������������ȷ����
A.NH3��CH4�����ʵ���֮��Ϊa: b
B.NH3��CH4����������ܶ�֮��Ϊa: b
C.NH3��CH4��Ħ������֮��Ϊ17: 16
D.NH3��CH4�ķ�����֮��Ϊ1 : 1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ոѣ����������ʣ����ۺ�Ӧ�þ�����Ҫ�����塣�������Խո�Ϊԭ�Ϻϳɾ�����߷��ӻ������·�ߣ�

�ش��������⣺
��1�����й��������˵����ȷ����______________�������ţ�
a.�������ζ������CnH2mOm��ͨʽ
b.��ѿ��ˮ�����ɻ�Ϊͬ���칹��������Ǻ���
c.��������Ӧ�����жϵ���ˮ���Ƿ���ȫ
d.���ۺ���ά�ض����ڶ�������Ȼ�߷��ӻ�����
��2��B����C�ķ�Ӧ����Ϊ______��
��3��D�й���������Ϊ______��D����E�ķ�Ӧ����Ϊ______��
��4��F �Ļ�ѧ������______����F����G�Ļ�ѧ����ʽΪ______��
��5������һ�ֹ����ŵĶ�ȡ�����㻯����W��E��ͬ���칹�壬0.5 mol W������̼��������Һ��Ӧ����44 gCO2��W����______�֣���������ṹ�������к˴Ź�������Ϊ�����Ľṹ��ʽΪ_________��
��6�����������ϳ�·�ߣ��ԣ���������-2��4-����ϩ��C2H4Ϊԭ�ϣ����Լ���ѡ��������Ʊ��Զ���������ĺϳ�·��_______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з��ӵĿռ乹�Ϳ���sp2�ӻ���������͵���( )
��BF3����CH2=CH2����![]() ����CH��CH ��NH3����CH4
����CH��CH ��NH3����CH4
A. �٢ڢ�B. �٢ڢ�C. �ۢܢ�D. �٢ڢۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ɱ�ͭ��mCu2O��nFeS��ұ���õ���ͭ�����Դ�ͭΪԭ���ƴ�ͭ���������£�
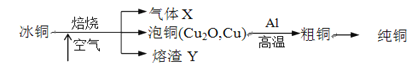
��ش��������⣺
��1������X��________��
��2��д����ͭұ����ͭ��Ӧ�Ļ�ѧ����ʽ_______��
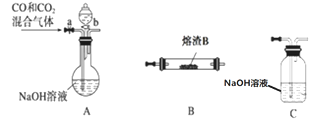
��3��ij�о���ѧϰС��������Y��CO��Ӧ����ȡFe������ȥ����װ�ã���
���밴���������ҵķ����������и�װ�ã�˳��ΪA��________��β������װ�ã�
��װ��C��������________________��

��4������Y����Ԫ�صļ�̬��+2�ۺ�+3�ۣ�Ϊ�˲ⶨ�����ж������ĺ�����ѧϰС��ȡ23.2g��������������ʹ����ȫ�ܽ⣬��Ӧ�����Һ�м�������KMnO4��Һ��һ������200mL0.1mol/L��KMnO4��Һ��
��д����Һ�м������Ը��������Һ���������ӷ���ʽ��________��
�������ж���������������Ϊ___%(������λ��Ч����)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����״����,���Т�6.72LCH4����3.01��1023��HCl���ӣ���13.6gH2S����0.2molNH3,������������Ĺ�ϵ���������ֱ�����������ȷ���� ____________ ��
a.�������>��>��
b.���ʵ�������>��>��
c.������ ��>��>��
d.��ԭ�Ӹ�������>��>��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͨ����ˮ��ɹ�ɵô��Σ����γ�NaCl�⣬������MgCl2��CaCl2��Na2SO4�Լ���ɳ�����ʡ��������Ʊ����ε�ʵ�鷽������������������ͼ��

��1���ڵڢٲ������ܽ������Ҫ�ò��������裬������______��
��2���ڢڲ�������Ŀ���dz�ȥ�����е�______���ѧʽ����ͬ�����ڢ�������Ŀ���dz�ȥ��Һ��______��
��3���ڢݲ������ˡ������еõ������ijɷ��У���ɳ��BaSO4��Mg��OH��2��______���ѧʽ����
��4���ڵڢ۲������У�ѡ��ij��ӵ��Լ�������KOH����NaOH��������______��
��5��ʵ�����þ��ε��������ڴ�����NaCl��������ԭ����______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ����
A.25��ʱ�����һԪ��HA��ҺpH=3����HAһ��Ϊ�������
B.25��ʱ����0.05mol��L-1��H2SO4��Һ��ˮϡ��100����������Һ��pH=3
C.25��ʱ����0.1mol��L-1��һԪ��BOH��Һ��ˮϡ����pH=9��������Һ![]()
D.25��ʱ��pH=11��һԪ��BOH��Һ��pH=3��HA��Һ�������ϣ�������ҺpH����Ϊ7
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾÿһ�����ʾһ�ַ�Ӧ������������A��C��D��E��F��ͨ������¾�Ϊ���壬�Ҽ���X���ɵ�A��C�����ʵ���֮��Ϊ1��1��BΪ����Һ�塣
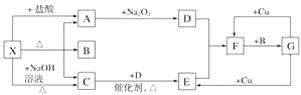
�Իش��������⣺
(1)X��________(�ѧʽ����ͬ)��F��__________��
(2)A�D��D��Ӧ�Ļ�ѧ����ʽΪ_______��
(3)G��Cu�ķ�Ӧ�У�G���ֵ�����Ϊ______��
(4)X�����NaOH��Һ��Ӧ����C�����ӷ���ʽΪ_____________��
(5)��C��B��DΪԭ�Ͽ�����G����ʹamol C��ȫת��ΪG��������������ҪD___ mol��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com