
【题目】下列说法不正确的是
A.25℃时,测得一元酸HA溶液pH=3,则HA一定为弱电解质
B.25℃时,将0.05mol·L-1的H2SO4溶液加水稀释100倍,所得溶液的pH=3
C.25℃时,将0.1mol·L-1的一元碱BOH溶液加水稀释至pH=9,所得溶液![]()
D.25℃时,pH=11的一元碱BOH溶液与pH=3的HA溶液等体积混合,所得溶液pH可能为7
【答案】A
【解析】
A.缺少酸HA的浓度;
B.强电解质稀释100倍pH+2;
C.根据pH可计算出c(H+),根据c(OH-)=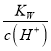 进行计算;
进行计算;
D. 先计算混合溶液中c(H+),再根据pH=-lg c(H+)计算pH的值。
A.题中缺少酸HA的浓度,不能确定酸HA的酸性强弱,A项错误;
B. 强酸稀释100倍,pH+2,0.05mol·L-1的H2SO4溶液pH=1,稀释100倍pH=3,B项正确;
C. pH=9,那么c(H+)=10-9mol/L,25℃时c(OH-)=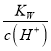 =
=![]() =10-5mol/L,C项正确;
=10-5mol/L,C项正确;
D. pH=11的一元碱BOH溶液中c(OH-)=10-3mol/L,pH=3的HA溶液c(H+)=10-3 mol/L,如果一元碱BOH是强碱,HA溶液为强酸,那么混合后溶液呈中性,若不是强碱或强酸,那么不等于7,D项正确;
答案选A。


科目:高中化学 来源: 题型:
【题目】在一定体积的密闭容器中,进行如下化学反应:
CO2(g)+H2(g)![]() CO(g)+H2O(g),
CO(g)+H2O(g),
其化学平衡常数K 和温度t的关系如下表:
t℃ | 700 | 800 | 830 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K =_____________________。
(2)该反应为____________反应(选填“吸热”、“放热”)。
(3)能判断该反应是否达到化学平衡状态的依据是_____________。
a.容器中压强不变 b.混合气体中 c(CO)不变
c.υ正(H2)=υ逆(H2O) d.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为 _________。
(5)1200℃时,在2L的密闭容器中,反应开始时加入1mol CO2、1mol H2、2molCO、2mol H2O,则反应向__________进行(填“正方向”、“逆方向”或“不移动”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“生活无处不化学”,请你回答下列问题。
(1)厨房中的调味品有:①盐(主要成分氯化钠)、②碱面(主要成分碳酸钠)、③白醋(主要成分乙酸)。将上述物质分别溶于水,其水溶液具有碱性的是______(填序号,下同),主要成分中属于盐类的是________,相互间能发生反应的是______。
(2)生活中遇到下列问题,不涉及到化学变化的是________。
①用四氯化碳可擦去圆珠笔油 ②自来水厂用液氯消毒 ③可用食醋洗掉水垢
(3)当前,环境治理已成为重要的民生工程。
①我国城市发布的“空气质量日报”中,下列物质不列入首要污染物的是_____(填字母代号)。
A.二氧化硫 B.二氧化碳 C.二氧化氮 D.可吸入颗粒物
②煤炭直接燃烧会引起多种环境问题。燃煤产生的SO2是导致______(填名称)污染现象形成的原因;处理含CO、SO2烟道气污染的一种方法是将其在催化剂作用下转化为单质S,发生反应的化学方程式为_____________________。
(4)向浑浊的水中加入明矾KAl(SO4)212H2O后,水可得到净化。写出明矾在水中的电离方程式___,往明矾溶液中逐滴加入Ba(OH)2溶液直至Al3+恰好沉淀完全,发生反应的离子方程式为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:![]() △H=+a kJ·mol-1(a>0)。一定温度下,在体积恒定的密闭容器中,加入1mol
△H=+a kJ·mol-1(a>0)。一定温度下,在体积恒定的密闭容器中,加入1mol ![]() 与3mol
与3mol ![]() ,下列说法正确的是
,下列说法正确的是
A.充分反应后,吸收的总热量一定小于akJ
B.升高反应温度,正反应速率增大,逆反应速率减小
C.当容器中X与Y的物质的量浓度之比为1:1时,体系达到平衡状态
D.达到平衡后,若增加N的浓度,容器内气体的密度减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组在实验室用如图所示装置制取氨并验证氨的某些性质,请回答。
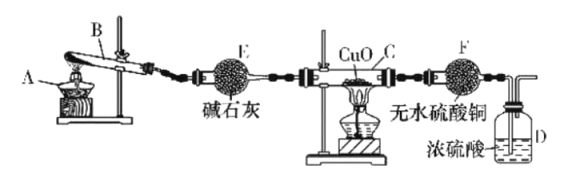
(1)写出此实验中制氨的化学方程式:___。
(2)实验进行一段时间,观察到硬质玻璃管内黑色氧化铜粉末变为红色,盛无水硫酸铜的干燥管内出现蓝色,同时有氮气生成。根据这些现象,写出在硬质玻璃管内发生反应的化学方程式:__,这个反应说明氨具有___(填字母代号)。
A.碱性 B.还原性 C.氧化性 D.不稳定性
(3)装置E的作用是__,装置F的作用是___。E中的碱石灰__(填“能”或“不能”)换成CaCl2。
(4)D中浓硫酸的主要作用是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】白藜芦醇广泛存在于食物(例如桑甚、花生,尤其是葡萄)中,它可能具有抗癌性。能够与1 mol该化合物发生反应的Br2和H2的最大用量分别是( )
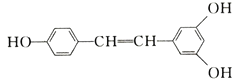
A.1mol、1molB.3.5mol、7mol
C.3.5mol、6molD.6mol、7mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组有机化合物中,不论两者以什么比例混合,只要总物质的量一定,则完全燃烧时消耗氧气的质量不变的是( )
A.CH4O,C3H4O5,C2H4O2B.C3H6,C3H8O,C4H8O3
C.C3H8,C4H6,C4H8OD.C2H6,C4H6O,C3H8O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分子式为 C12H14O2 的有机物 F 被广泛用于香精的调香剂。为了合成该物质,某实验室的 科技人员设计了下列合成路线:
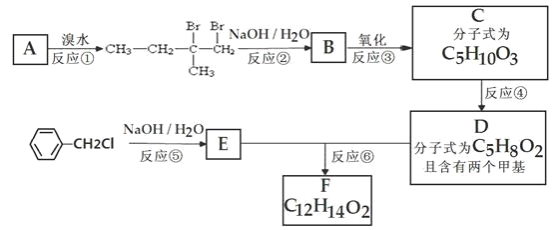
请回答下列有关问题:
(1)A 物质的结构简式为________在核磁共振氢谱中能呈现_____种峰。
(2)C 物质的官能团名称_____、________。
(3)反应①的反应类型是________,反应④的反应类型是_____
(4)E 的结构简式为_____
(5)写出反应⑤、⑥的化学方程式:⑤_____;⑥_____
(6)F 有多种同分异构体,请写出符合下列条件的所有物质结构简式:_____
①属于芳香族化合物,且含有与 F 相同的官能团;
②苯环上有两个取代基,且苯环上的一氯代物只有两种;
③其中一个取代基为-CH2COOCH3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电动汽车(标志为“![]() ”)在改善城市交通、保护环境等方面的作用至关重要。下列说法不正确的是
”)在改善城市交通、保护环境等方面的作用至关重要。下列说法不正确的是
A. 电动汽车的使用有助于减少氮氧化物的排放
B. 燃油汽车也可以悬挂该标志
C. 电动汽车使用时涉及化学能与电能的转换
D. 电动汽车充电、放电过程均有电子转移
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com