
【题目】表示下列变化的化学用语正确的是
A.NaHCO3溶液显碱性:HCO![]() +H2O
+H2O![]() CO
CO![]() +OH-
+OH-
B.醋酸溶液显酸性:CH3COOH=CH3COO-+H+
C.氨水显碱性:NH3·H2O![]() NH
NH![]() +OH-
+OH-
D.铁在潮湿空气中被腐蚀的负极反应:Fe-3e- =Fe3+
 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案科目:高中化学 来源: 题型:
【题目】钛的化合物如TiO2、Ti(NO3)4、TiCl4、 Ti(BH4)2等均有着广泛用途。
(1)写出Ti的基态原子的外围电子排布式____________。
(2)TiCl4熔点是-25℃,沸点136.4℃,可溶于苯或CCl4,该晶体属于_____晶体;BH4-中B原子的杂化类型为____________;
(3)在 TiO2催化作用下,可将CN-氧化成CNO-,进而得到N2。与CNO-互为等电子体的分子化学式为_________________。
(4)Ti3+可以形成两种不同的配合物:[Ti(H2O)6]Cl3(紫色),[TiCl(H2O)5]Cl2H2O(绿色),两者配位数_____(填“相同”或“不同”),绿色晶体中配体是______。

(5)TiO2难溶于水和稀酸,但能溶于浓硫酸,析出含有钛酰离子的晶体,钛酰离子常成为链状聚合形式的阳离子,其结构形式如图1,化学式为____________。
(6)金属钛内部原子的堆积方式是面心立方堆积方式,如图2。若该晶胞的密度为![]() g/cm3,阿伏加德罗常数为NA,则该晶胞的边长为______________cm。
g/cm3,阿伏加德罗常数为NA,则该晶胞的边长为______________cm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)乙醇—氧气燃料电池是一种清洁能源,该电池用金属铂片插入氢氧化钾溶液中作电极,在两极区分别加入乙醇和氧气,其负极反应式为:_____________。
(2)古代铁器(埋藏在地下)在严重缺氧的环境中,仍然锈蚀严重。原因是一种叫做硫酸盐还原菌的细菌,能提供正极反应的催化剂,可将土壤中的![]() 还原为S2-,该反应放出的能量供给细菌生长、繁殖之需。①写出该电化学腐蚀的正极反应式:____________。
还原为S2-,该反应放出的能量供给细菌生长、繁殖之需。①写出该电化学腐蚀的正极反应式:____________。
②文物出土前,铁器表面的腐蚀产物可能有(写化学式)____________。
(3)对金属制品进行抗腐蚀处理,可延长其使用寿命。以下为铝材表面处理的一种方法:
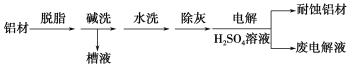
①碱洗的目的是除去铝材表面的自然氧化膜。碱洗时常有气泡冒出,原因是(用离子方程式表示):____________。
②以铝材为阳极,在H2SO4溶液中电解,铝材表面形成氧化膜,阳极电极反应式为:____________。取少量废电解液,加入NaHCO3溶液后产生气泡和白色沉淀,产生沉淀的原因是____________。
(4)采用石墨电极电解CuSO4溶液一段时间后,向所得溶液中加入0.1molCu(OH)2后,恰好使溶液恢复到电解前的浓度。则电解过程中通过导线的电量为____________C(已知NA=6.02×1023mol—1,1个电子所带的电量为1.60×10-19C)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制取的乙烯中常混有少量的![]() ,有人设计如图实验装置以证明上述混合气体中含有乙烯和二氧化硫。试回答下列问题:
,有人设计如图实验装置以证明上述混合气体中含有乙烯和二氧化硫。试回答下列问题:
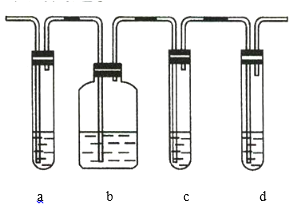
(1)图中a、b、c、d装置盛放的试剂依次是___________________(填序号)。
A.品红溶液 B.![]() 溶液 C.浓硫酸 D.酸性高锰酸钾溶液
溶液 C.浓硫酸 D.酸性高锰酸钾溶液
(2)能说明![]() 存在的实验现象是______________________________________。
存在的实验现象是______________________________________。
(3)使用装置b的目的是________________________。
(4)使用装置c的目的是________________________。
(5)能说明混合气体中含有乙烯的现象是____________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知表中是某些有机物的模型图,根据要求回答下列问题:
有机物 | 甲 | 乙 | 丙 |
模型 |
|
|
|
(1)甲的分子式是___________________,其一氯代物有___________________种。
(2)写出乙与![]() 的
的![]() 溶液发生反应的化学方程式:______________________________________,该反应的反应类型是___________________。
溶液发生反应的化学方程式:______________________________________,该反应的反应类型是___________________。
(3)丙的摩尔质量为![]() ,则用苯制备该物质时的催化剂是___________________。
,则用苯制备该物质时的催化剂是___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在相同温度下,有相同体积的甲、乙两容器,且保持体积不变,甲容器中充入 1 mol SO2 和 1 mol O2,乙容器中充入 2 mol SO2 和 2 mol O2。下列叙述中正确的是( )
A.平衡时 SO2 的转化率:乙<甲B.平衡时 O2 的浓度:乙<甲
C.化学反应速率:乙<甲D.平衡时 SO2 的体积分数:乙<甲
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以硫铁矿![]() 主要成分为
主要成分为![]() ,还有少量CuS、
,还有少量CuS、![]() 等杂质
等杂质![]() 为原料制备绿矾晶体
为原料制备绿矾晶体![]() 的工艺流程如下:
的工艺流程如下:
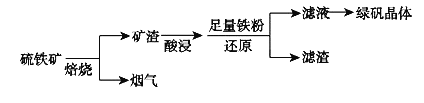
![]() “酸浸”过程,矿渣中的
“酸浸”过程,矿渣中的![]() 与稀
与稀![]() 反应的离子方程式___________________。
反应的离子方程式___________________。
![]() 烟气中的
烟气中的![]() 会污染环境,可用足量氨水吸收,写出该反应的离子方程式________。
会污染环境,可用足量氨水吸收,写出该反应的离子方程式________。
![]() 滤液中金属阳离子的检验方法________________________________。
滤液中金属阳离子的检验方法________________________________。
![]() 溶液制备绿矾晶体过程中要保持
溶液制备绿矾晶体过程中要保持![]() 过量,理由___________________________。
过量,理由___________________________。![]() 结合化学用语说明原因
结合化学用语说明原因![]()
![]() 燃料细菌脱硫法是用氧化亚铁硫杆菌
燃料细菌脱硫法是用氧化亚铁硫杆菌![]() 对硫铁矿进行催化脱硫,同时得到
对硫铁矿进行催化脱硫,同时得到![]() 溶液。其过程如图所示:
溶液。其过程如图所示:
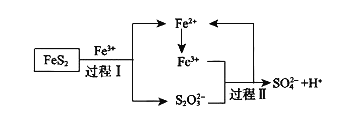
已知总反应为:![]()
![]() 将过程I离子方程式补充完整
将过程I离子方程式补充完整
____FeS2+_____Fe3++______ _______=7Fe2++________S2O32-+_____ _____
![]() 过程II反应的离子方程式___________________________________。
过程II反应的离子方程式___________________________________。
![]() 绿矾晶体在空气中易被氧化。取
绿矾晶体在空气中易被氧化。取![]() 样品,加水完全溶解,用酸化的
样品,加水完全溶解,用酸化的![]() 溶液滴定至终点,消耗
溶液滴定至终点,消耗![]() 溶液
溶液![]() 。反应原理:
。反应原理:![]() 。则绿矾晶体纯度的计算式为_______________。
。则绿矾晶体纯度的计算式为_______________。![]() 摩尔质量为
摩尔质量为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醇烃化新技术是近几年合成氨工业净化精炼原料气,除去少量CO一种新方法,其原理可分为甲醇化与甲烷化两个部分。
甲醇化:![]()
![]()
甲烷化:![]()
![]()
![]() 下列措施有利于提高醇烃化过程CO转化率的是________。
下列措施有利于提高醇烃化过程CO转化率的是________。
A.及时分离出![]() 适当升高反应温度
适当升高反应温度
C.使用高效的催化剂 ![]() 适当增大压强
适当增大压强
![]() 甲醇化平衡常数可用
甲醇化平衡常数可用![]() 表示,
表示,![]() 为平衡组分中各物质的物质的量分数。若CO与
为平衡组分中各物质的物质的量分数。若CO与![]() 混合原料气中CO的体积分数为
混合原料气中CO的体积分数为![]() ,经甲醇化后CO的平衡转化率为w,则
,经甲醇化后CO的平衡转化率为w,则![]() ________
________![]() 用含w的表达式来表示
用含w的表达式来表示![]() 。
。
![]() 测试a、b两种催化剂在不同压强与温度条件下,甲醇化过程中催化效率如下图:
测试a、b两种催化剂在不同压强与温度条件下,甲醇化过程中催化效率如下图:

从上图可知选择哪种催化剂较好________![]() 填a或
填a或![]() ,理由是________。
,理由是________。
![]() 下列关于醇烃化过程说法正确的是________。
下列关于醇烃化过程说法正确的是________。
A.甲醇化与甲烷化过程在任何条件下均为自发反应
B.选择不同的催化剂可以控制醇烃化过程中生成甲醇与甲烷的百分含量
C.当温度与反应容器体积一定时,在原料气中加入少量的惰性气体,有利于提高平衡转化率与甲醇的产率
D.适当增大混合气体中![]() 的百分含量,有利于提高醇烃化过程CO平衡转化率
的百分含量,有利于提高醇烃化过程CO平衡转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸乙酯广泛用于药物、染料、香料等工业,某学习小组设计以下两套装置用乙醇、乙酸和浓硫酸分别制备乙酸乙酯(沸点77.2℃)。下列说法不正确的是
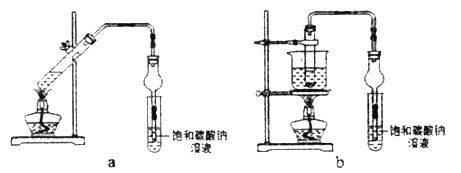
A. 浓硫酸能加快酯化反应速率 B. 不断蒸出酯,会降低其产率
C. 装置b比装置a原料损失的少 D. 可用分液的方法分离出乙酸乙酯
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com