
��ͼװ���У��������ڳ���0.1 mol NO���壬�������װ��һ����Na2O2����A������ͨ��CO2���壮�����£��������л���������D�����ƶ���������C��ʱ���������С����С��Ϊԭ����� ������CO2�ļ���ͨ�룬�������������ƶ����������ǻ�����ĥ����
������CO2�ļ���ͨ�룬�������������ƶ����������ǻ�����ĥ����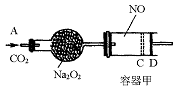
��֪�� 2Na2O2 + 2CO2 �� 2Na2CO3 + O2
��1����֪����������C��ʱ������������ʵ�����������2.24 g��
�ٴ�ʱ��ͨ���״���µ�CO2�������L��
����������NO2ת��ΪN2O4��ת�����Ƕ��٣�
�ۻ�������C������ͨ��a mol CO2����ʱ����ǡ�û���D������aֵ�� 0.01������ڡ�С�ڡ����ڣ����������� ��
��2�����ı�������Na2O2������Ҫͨ�����ڼ��������¶ȼ�ͨ�����CO2��ʹ����������D��C���ִ�C��D���ƶ�����Na2O2��������СֵӦ����________g��
(��16��)
��1����CO2���1.792 L����3�֣� ��25����4�֣�
��С�ڣ�2�֣�����������C����������ټ��٣���������Na2O2�ѷ�Ӧ�꣬������C��D�ƶ����������2NO2 N2O4ƽ�����ƣ�ʹ�������ʵ������࣬��������Dʱ���������ʵ���������0.01 mol���������CO2��С��0.01 mol ��3�֣�
N2O4ƽ�����ƣ�ʹ�������ʵ������࣬��������Dʱ���������ʵ���������0.01 mol���������CO2��С��0.01 mol ��3�֣�
��2��1.56 g��4�֣�
�������������
��1������ͨ���״����CO2��������Ϊx���������������Ϊy
2Na2O2+2CO2=Na2CO3+O2 ��m��
2��22.4 L 22.4 L 56 g
x y 2.24 g
56 g�Ux��2��22.4 L��2.24 g
���x=1.792L��y=0.896L
n��O2��=0.04mol
2NO+ O2=2NO2
2 1 2
0.08 mol 0.04 mol 0.08 mol
0.1 mol>0.08 mol
����NO����������NO2�����ʵ���Ϊ0.08 mol��
����2NO2 N2O4 ��n��
N2O4 ��n��
2 1 1
0.02 mol 0.1 mol��(1��9/10)=0.01mol
����NO2ת��ΪN2O4��ת����Ϊ
��������C����������ټ��٣���������Na2O2�ѷ�Ӧ�꣬������C��D�ƶ����������2NO2 N2O4ƽ�����ƣ�ʹ�������ʵ������࣬��������Dʱ���������ʵ���������0.01 mol���������CO2��С��0.01 mol��
N2O4ƽ�����ƣ�ʹ�������ʵ������࣬��������Dʱ���������ʵ���������0.01 mol���������CO2��С��0.01 mol��
��2��ʵ�ִ�B��C���ƶ���ֻ��ͨ������ʹ2NO2 N2O4��ƽ�������ƶ����˷�ӦΪ���ȷ�Ӧ����
N2O4��ƽ�������ƶ����˷�ӦΪ���ȷ�Ӧ����
������ʱ2NO2 N2O4 ��n��
N2O4 ��n��
2 1 1
0.02 mol 0.1 mol��(1��9/10)
������������Ӧ��0.02 mol��NO2
����ת����ϵʽ��֪��2Na2O2��O2��2NO��2NO2
������ҪNa2O2 0.02 mol
������������СֵΪ0.02 mol��78 g/mol��1.56 g��
���㣺����NO��CO2�������Ʒ�Ӧ���йؼ������ж�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
���ð������������ᣬ�̶���ȡ����李������������������������Ϊ90%����ת��Ϊ����淋�ת����Ϊ94%����100 t�������������ٶ�����泥�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
��2��0 mol��L CuSO4��Һ��1��0 mol��LH2SO4��Һ��100 mL��ϣ������Ϻ���Һ��������ڻ��ǰ������Һ�����֮�ͣ������㣺
��1�����Һ��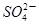 �����ʵ���Ũ��_____________mol��L��
�����ʵ���Ũ��_____________mol��L��
��2������Һ�м����������ۣ����㹻����ʱ���������ʣ�ࡣ��ʱ������������������״����Ϊ_________________L����Һ��Fe2�������ʵ���Ũ����___________mol��L��
��3��������Һ�еμ�1 mol��L��NaOH��Һ��ʹCu2��ǡ����ȫ����������NaOH��Һ�����_____________________mL��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
Na2O2������DZˮͧ��������������Ĺ��������±��������������ijɷ�(��Ϊ����ٷֺ����
| | ���� �ɷ� | ������� ����ɷ� |
| N2 | 78% | 74% |
| O2 | 21% | 16% |
| H2O | 0. 5% | 6% |
| CO2 | 0. 03% | 4% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
��������Ҫ�Ļ�����Ʒ���ڻ�����ѧʵ���У�������Ҫ�����á�
��1�����ʵ���Ũ��Ϊ18��4mol/L,��������Ϊ0��98��Ũ��������ˮ����ʱ���������������½���0��87���ܶ�1��8g?cm-3������ʱ����ʧȥ���������� ��������Ϊ0��87����������ʵ���Ũ��Ϊ
��������λС������ͬ����50mL 18��4mol/L��Ũ������Ϊ�����ʱ��������ˮ___________g��
��2����ҵ���Ը����������ᣮ����Ϊԭ����ȡ�����[NH4Al(SO4)2��12H2O]������������Ӧԭ�����£����Ը����������ɷ�������ķ�Ӧ����
Al2O3 + 3H2SO4 �� Al2(SO4)3 + 3H2O����������
Al2(SO4)3 + H2SO4 + 2NH3 �� 2NH4Al(SO4)2����������
ij������ͬʱ��ȡ���������������ͨ����������������������ֲ�Ʒ�IJ���������ʹ�Ƶõ�������������������ʵ���֮��Ϊ1:1����Ͷ��ʱ����������������ʵ���֮����
��3�����Ṥҵ�ϴ���ýӴ��������ᣨ��������������������Ϊ20%����Ϊʹ���������ճ�֣���ͨ�����40%�Ŀ����������պ�¯����SO2���������Ϊ_____��
��4��������¯��������������ֱ������Ӵ��ң��������������5%��ͬ��ͬѹ�²ⶨ�����Լ���SO2��ת����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�Ի�����(FeS2)�������ƺ�������Һ��Ϸ�Ӧ�Ʊ������������壬����ˮ���ջ�ö���������Һ���ڴ˹�������Ҫ�������˵��¶ȣ����¶Ȳ���������Ӧ���ӣ�Ӱ������ClO2����Ĵ��ȣ��һ�Ӱ��ClO2����������ʡ����������ͼ6��ʾ����ش���������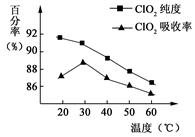
��1����ͼ��֪����Ӧʱ��Ҫ���Ƶ������¶��������棬�ﵽ��Ҫ���ȡ�����˴�ʩ��������
��2����֪���������е���Ԫ�������������±�ClO3��������SO42����д���Ʊ��������ȵ����ӷ���ʽ��������
��3��ijУ��ѧѧϰС�����ԡ�m(ClO2)/m(NaClO3)����Ϊ����ClO2���ʵ�ָ�ꡣ��ȡNaClO3��Ʒ����6.0g��ͨ����Ӧ�����տɵ�400 mL ClO2��Һ��ȡ��20 mL������37.00 mL 0.500mol��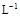 (NH4)2Fe(SO4)2 ��Һ��ַ�Ӧ������Fe2+����0.0500 mol��
(NH4)2Fe(SO4)2 ��Һ��ַ�Ӧ������Fe2+����0.0500 mol��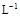 K2Cr2O7����Һ�ζ����յ㣬����20.00 mL����Ӧԭ�����£�
K2Cr2O7����Һ�ζ����յ㣬����20.00 mL����Ӧԭ�����£�
4H++ClO2+5Fe2+=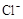 +5Fe3+ +2H2O
+5Fe3+ +2H2O
14H+ +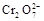 +6 Fe2+ =2Cr3+ + 6 Fe3+ +7H2O
+6 Fe2+ =2Cr3+ + 6 Fe3+ +7H2O
�Լ���ClO2�ġ����ʡ�����д��������̣�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�ⶨ1 mol�����ڱ�״������ռ�����ʵ������������£�
�ٰ���ͼװ��ʵ��װ�á�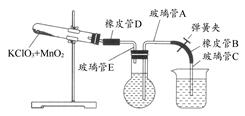
��ϴ���Թ�Ȼ���ָ��
����500 mL��ƿ��װ��ˮ����500 mL�ձ����������ˮ����������ƿ���ձ��IJ�����A����Ƥ��B�Ͳ�����C��Ҳװ��ˮ���м䲻Ҫ�������ݣ�Ȼ���õ��ɼа���Ƥ��B�н���
�ܳƵ��Թܵ�����Ϊ14.45 g�����Թ������KClO3��MnO2�Ļ����ٳ�������Ϊ15.95 g��
�ݴ��ɼУ����ձ�����ʹ��ƿ���ձ��е�ˮ��һ�£��ٹرյ��ɼУ�Ȼ����ձ��е�ˮ������
���ɼУ������ԹܵĻ���ﵽ���ٲ������壬��ˮ���������ձ�ʱΪֹ��
�߷�Ӧ��Ϻ��װ�÷�����ȴ�����¡�
������ձ��ĸ߶�ʹ��ƿ���ձ��е�ˮ��һ�£�Ȼ���ٹرյ��ɼС�
����500 mL��Ͳ�����ձ���ˮ�����Ϊ285.0 mL����������Ϊ��״�������������Ϊ279.7 mL��
���ٳ�����ȴ���Թܵ�����Ϊ15.55 g��
(1)�ڲ������У�װ����ȴʱ��������C�ij��ڣ�һֱҪ���ձ���ˮ�У������뿪ˮ�棬�������� ��
(2)����������ı�Ҫ�ԣ���ΪʲôҪ�����ձ��ĸ߶ȣ�ʹ��ƿ���ձ��е�ˮ��һ�£� ��
(3)��״���£�1 mol������ռ�����(����С������λ)Ϊ L���������MnO2����������Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�����Ǽ���ʵ���г��õ�������
A. B.
B. C.
C. D.
D.
��1��д����������������������ƣ�B___________��C___________��D___________
ʵ����Ҫ����500 mL 0.2 mol/L NaOH��Һ����ش��������⣺
��2����������ƽ��ȡ�������ƣ�������Ϊ_______________g��
��3��������Ҫ�����������ȷ˳����_______________������ţ���
�ٳ�ȡһ���������������ƣ������ձ��У�����������ˮ�ܽ⣻
�ڡ����ݡ�
�۴���ȴ�����º���Һת�Ƶ�500 mL ����ƿ�У�
�ܸǺ�ƿ�����������µߵ���ҡ�ȣ�
��������������ˮϴ���ձ��ڱںͲ�����2��3�Σ�ϴ��Һת�Ƶ�����ƿ�С�
��4�������ƹ����У���������������ȷ�ģ����в�������������Ũ��ƫ�ߵ���__________��
��û��ϴ���ձ��Ͳ����� ��ת����Һʱ������������������ƿ����
������ƿ�����������������ˮ �ܶ���ʱ���ӿ̶���
��δ��ȴ�����¾ͽ���Һת�Ƶ�����ƿ������
��5��д������ڡ����ݡ��ľ��������
��6������ֲ���纣���������к��зḻ�ĵ�Ԫ�أ���Ԫ���Ե����ӵ���ʽ���ڡ�ijѧ����
��С�����Ӻ�������ȡ�⣬������µ����̣�
����֪���̢��з�Ӧ�����ӷ���ʽΪ��2I�� + Cl2 = 2Cl�� + I2��
��.ָ����ȡ��Ĺ������йص�ʵ����������ƣ��� �� �� ��
��.��ȡ��Ĺ����У���ѡ����л��ܼ��� (�����) ��
A���ƾ� B������ C �����Ȼ�̼
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
�������������Ϊ�������ܸ������ӣ�H+���Ķ����ᣬ���ܽ�����ӵĶ��Ǽ�����������������������������ʵ���
| A��HCl | B��NaOH |
| C��Fe2O3 | D��NaHCO3 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com