
常温下,取0.2mol/LHX溶液与0.2mol/LNaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=8,则下列说法(或关系式)正确的是( )
A.C(X-)-C(Na+)=9.9×10-7mol/L
B.C(Na+)=C(X-)+C(HX)=0.1mol/L
C.C(OH-)-C(HX)=C(H+)=1×10-6mol/L
D.混合溶液中由水电离出的C(OH-)大于0.2mol/LHX溶液中由水电离出的C(H+)
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:2013届江西省高二下学期期中考试化学试卷(解析版) 题型:填空题
(18分)按要求回答下列问题
(1)用标准NaOH溶液滴定未知浓度的盐酸,用酚酞作指示剂,下列操作中会导致实验结果偏低的是 (填序号 )
①碱式滴定管用蒸馏水洗净后没有用标准液润洗
②用酸式滴定管加待测液时,刚用蒸馏水洗净后的滴定管未用待测液润洗
③锥形瓶用蒸馏水洗净后没有用待测液润洗
④滴定前滴定管尖端有气泡,滴定后气泡消失
⑤终点读数时俯视,其他读数方法正确
(2)某课外活动小组同学用如图甲装置进行实验,试答下列问题:
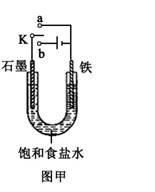
①若开始时开关K与a连接,则铁发生电化学腐蚀中的 腐蚀。
②若开始时开关K与b连接,则总反应的离子方程式为 。
(3)已知:铅蓄电池总的化学方程式为:Pb+PbO2 +2H2SO4 2PbSO4+2H2O
2PbSO4+2H2O
①铅蓄电池在放电时负极反应为 ,
②铅蓄电池在充电时阳极反应为 ;
③如果铅蓄电池在放电时回路中有2mol电子转移时,消耗H2SO4 mol。
(4)常温下,如果取0.1mol/L HA溶液与0.1mol/L NaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=8,求出混合液中下列算式的精确计算结果(填具体数字):
c(OH-)-c(HA)= ___________ mol/L。
(5)在Cl-、Al3+、HSO4-、K+、HS-五种离子中,只能水解不能电离的离子是 ,只能电离不能水解的离子是 ,既能电离又能水解的离子是 ,写出能水解离子的水解离子方程式 , 。
(6)已知25℃时,Mg(OH)2的溶度积常数Ksp = 5.6×10-12,测得某溶液的pH = 13,则此温度下溶液中的c(Mg2+) = ____________________。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年河北省衡水中学高二第一次调研考试化学试卷(带解析) 题型:单选题
常温下,取0.2mol/LHX溶液与0.2mol/LNaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=8,则下列说法(或关系式)正确的是( )
| A.C(X-)-C(Na+)=9.9×10-7mol/L |
| B.C(Na+)=C(X-)+C(HX)=0.1mol/L |
| C.C(OH-)-C(HX)=C(H+)=1×10-6mol/L |
| D.混合溶液中由水电离出的C(OH-)大于0.2mol/LHX溶液中由水电离出的C(H+) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com