
【题目】“接触法制硫酸”的主要反应是2SO2+O2![]() 2SO3在催化剂表面的反应历程如下:
2SO3在催化剂表面的反应历程如下:
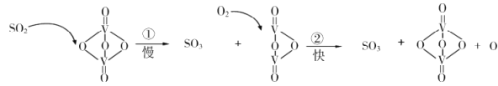
下列说法正确的是
A.使用催化剂只能加快正反应速率B.反应②的活化能比反应①大
C.该反应的催化剂是V2O4D.过程中既有V—O键的断裂,又有V—O键的形成
科目:高中化学 来源: 题型:
【题目】常温下,将amol氮气与bmol氢气的混合气体通入一个固定容积的密闭容器中,发生反应N2(g)+3H2(g)![]() 2NH3(g)。
2NH3(g)。
(1)若反应进行到某时刻t时,nt(N2)=13 mol,nt(NH3)=6 mol,则a值为________。
(2)反应达到平衡时,混合气体的体积为716.8 L(标准状况下),其中氨气体积分数为25%,平衡时氨气的物质的量为________。
(3)原混合气体与平衡混合气体的总物质的量之比(写最简整数比,下同)n始∶n平=________。
(4)原气体中a∶b=________。
(5)达到平衡时,N2和H2的转化率之比α(N2)∶α(H2)=________。
(6)达到平衡时混合气体中,n(N2)∶n(H2)∶n(NH3)=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲烷是一种清洁能源,下列有关说法正确的是( )
A.一定温度下,反应CO2(g)+4H2(g)=CH4(g)+2H2O(g)能自发进行,该反应的ΔH>0
B.碱性甲烷-空气燃料电池的负极反应为CH4-8e-+10OH-=CO![]() +7H2O
+7H2O
C.标准状况下,5.6LCH4在空气中完全燃烧,转移电子的数目约为2.408×1024
D.甲烷和微生物共同作用可以实现城市废水脱氮处理,反应温度越高,脱氮速率越快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化镓(GaN)是一种重要的半导体材料。某工厂利用铝土矿(成分为Al2O3、Ga2O3、Fe2O3等)为原料制备GaN的流程如下图所示:
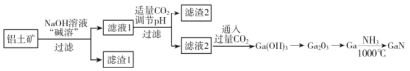
已知:镓与铝同主族,镓的熔点是29.8°C,沸点是2403°C;其氧化物和氢氧化物均为两性化合物;氢氧化物的电离常数如下:
两性氢氧化物 | Al( OH)3 | Ga( OH)3 |
酸式电离常数Ka | 2×10-11 | 1×10-7 |
碱式电离常数Kb | 1.3×10-33 | 1.4×10-34 |
回答下列问题:
(1)为了提高 “碱溶”效率应采用的措施是__________(回答两种措施)。
(2)滤渣1的成分是_________。
(3)滤液2中通入过量CO2的理由是________(用离子方程式表示)。
(4)流程中利用镓与NH3在1000℃反应生成固体半导体材料 GaN,每生成l molGaN时放出15. 45 kJ热量,写出该反应的热化学方程式________。
(5)在密闭容器中,充入一定量的Ga与NH3发生反应 ,测得反应平衡体系中NH3的体积分数与压强 P和温度T 的关系曲线如下图所示。图中A 点和C点化学平衡常数的大小关系: KA____KC (填“<”“=”或 “ > ”) , 判断的依据是________。
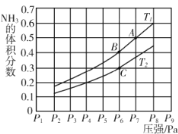
(6)已知铝土矿中Ga2O3的质量分数为 a%,某工厂使用 w 吨铝土矿经过一系列反应, 反应过程中镓元素的总利用率为 b%能制得________吨氮化镓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫代硫酸钠(Na2S2O3)可作为照相业的定影剂,反应的化学方程式为:AgBr+2Na2S2O3=Na3[Ag(S2O3)2]+NaBr。下列说法正确的是
A.基态Br原子中电子的空间运动状态有35种B.[Ag(S2O3)2]3-中含有离子键、共价键、配位键
C.![]() 中心原子S的杂化方式为sp3D.非金属元素S、O、Br中电负性最大的是Br
中心原子S的杂化方式为sp3D.非金属元素S、O、Br中电负性最大的是Br
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Cl2O能与水反应生成次氯酸,可杀死新型冠状病毒等多种病毒。一种制备Cl2O原理为HgO(红色粉末)+2Cl2=HgCl2(白色粉末)+Cl2O,某化学小组用下图装置制备Cl2O(夹持装置略去)
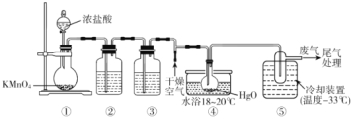
已知:①Cl2O的熔点为-116°C、沸点为3.8°C,易溶于水;②高浓度的Cl2O易爆炸,Cl2O与有机物接触或加热时会发生剧烈反应。
下列说法错误的是
A.装置③中盛装的试剂是饱和食盐水,④中现象是红色粉末逐渐变为白色
B.装置④中橡胶塞用锡箔包裹,防止Cl2O与橡胶塞反应
C.从装置⑤中逸出气体的主要成分是Cl2O
D.通入干燥空气的目的是将生成的Cl2O稀释,防止发生爆炸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向7.5mL0.03molL-1的H3PO4溶液中,逐滴加入相同浓度的NaOH溶液,溶液pH与NaOH溶液体积关系如图所示,已知Ka1>Ka2>Ka3,下列说法错误的是
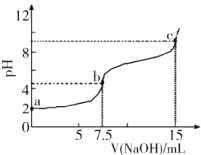
A.H3PO4第一级电离平衡常数Ka1的数量级为10-3
B.水的电离程度:b<c
C.b点溶液中离子浓度:c(Na+)>c(![]() )>c(
)>c(![]() )>c(
)>c(![]() )>c(H+)>c(OH-)
)>c(H+)>c(OH-)
D.c点溶液中:2c(H3PO4)+c(![]() )+c(H+)=c(OH-)+c(
)+c(H+)=c(OH-)+c(![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据vt图分析外界条件改变对可逆反应A(g)+3B(g) ![]() 2C(g) ΔH<0的影响。该反应的速率与时间的关系如图所示:
2C(g) ΔH<0的影响。该反应的速率与时间的关系如图所示:
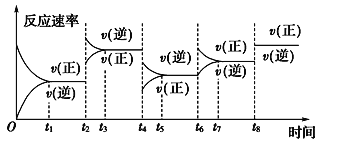
可见在t1、t3、t5、t7时反应都达到平衡,如果t2、t4、t6、t8时都只改变了一个反应条件,则下列对t2、t4、t6、t8时改变条件的判断正确的是
A. 使用了催化剂、增大压强、减小反应物浓度、降低温度
B. 升高温度、减小压强、减小反应物浓度、使用了催化剂
C. 增大反应物浓度、使用了催化剂、减小压强、升高温度
D. 升高温度、减小压强、增大反应物浓度、使用了催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学按照课本实验要求,用50mL0.50mol/L的盐酸于50mL0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量计算中和热,下列说法中,正确的是( )
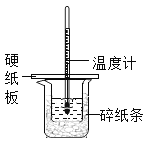
A. 烧杯间填满碎纸条的作用是固定小烧杯
B. 用如图装置可以完成中和热测定的实验
C. 为防止混合溶液时溅出产生误差,因此混合时速度要慢
D. 若将盐酸体积改为60mL,不考虑热量损失,理论上所求中和热相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com