
为了探究原电池的工作原理,某化学学习小组设计了一组实验,其装置如下图:
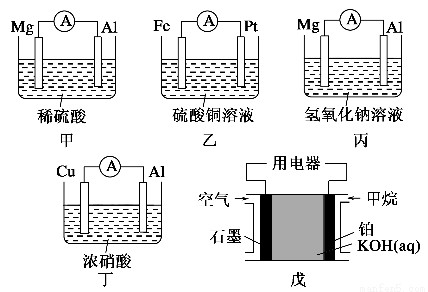
回答下列问题:
(1)根据原电池原理填写下表:
装置序号 | 正极 | 负极反应式 | 阳离子移动方向 |
甲 |
|
|
|
乙 |
|
|
|
丙 |
|
|
|
丁 |
|
|
|
戊 |
|
|
|
(2)电极类型除与电极材料的性质有关外,还与________有关。
(3)根据上述电池分析,负极材料是否一定参加电极反应?_____
(填“是”“否”或“不一定”),请举例说明:__________________________________________。
(4)指出下列电池的放电过程中,电解质溶液酸碱性的变化:甲_______,丙_______,戊_______。(填酸性或碱性增强或减弱)
(1)
装置 序号 | 正极 | 负极反应式 | 阳离子 移动方向 |
甲 | Al | Mg-2e-=Mg2+ | 铝极 |
乙 | Pt | Fe-2e-=Fe2+ | 铂极 |
丙 | Mg | Al-3e-+4OH-=AlO2-+2H2O | 镁极 |
丁 | Al | Cu-2e-=Cu2+ | 铝极 |
戊 | 石墨 | CH4-8e-+10OH-=CO32-+7H2O | 石墨 |
(2)电解质溶液的性质
(3)不一定 上述五个原电池中,戊装置的负极材料没有参与反应,其他电池的负极发生了氧化反应
(4)酸性减弱 碱性减弱 碱性减弱
【解析】(1)电池甲:在稀硫酸中,镁比铝活泼,镁为负极,发生氧化反应,铝为正极,H+在铝极上发生还原反应;
乙电池:铁比铂活泼,铁为负极;
丙电池:在氢氧化钠溶液中,铝与NaOH溶液反应,铝失去电子,发生氧化反应,铝离子与氢氧化钠反应生成偏铝酸根离子和水;
丁电池:常温下,浓硝酸使铝钝化,铜溶解,铜为负极;
戊电池是燃料电池,甲烷与氧气反应,甲烷发生氧化反应,在碱中生成碳酸盐和水,氧气发生还原反应。所以。在负极区通入甲烷,在正极区通入空气。
(2)通过比较甲、丙电池可知,电极都是铝、镁,由于电解质溶液不同,故电极名称不同,即电极类型与电极材料、电解质溶液都有关。
(3)大多数电池的负极材料参与反应发生氧化反应,燃料电池的负极材料不参与反应,可燃物如氢气、一氧化碳、甲烷、乙醇等在负极区发生氧化反应。
(4)根据溶液中离子参加反应情况判断溶液酸碱性的变化。


科目:高中化学 来源:2014年高一化学人教版必修二 3-2-1乙烯练习卷(解析版) 题型:选择题
某烯烃与H2加成后的产物为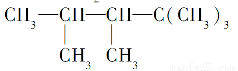 ,则该烯烃的结构简式可能有( )
,则该烯烃的结构简式可能有( )
A.1种 B.2种 C.3种 D.4种
查看答案和解析>>
科目:高中化学 来源:2014年高一化学人教版必修二 2-3-2化学反应的限度练习卷(解析版) 题型:选择题
对于可逆反应:4NH3(g)+5O2(g) 4NO(g)+6H2O(g),下列说法正确的是( )
4NO(g)+6H2O(g),下列说法正确的是( )
A.达到化学平衡时,4v正(O2)=5v逆(NO)
B.若单位时间内生成xmol NO的同时消耗xmol NH3,则反应达到平衡状态
C.达到平衡状态时,若增加容器体积,则正反应速率减小,逆反应速率增大
D.化学反应速率关系是:2v正(NH3)=3v正(H2O)
查看答案和解析>>
科目:高中化学 来源:2014年高一化学人教版必修二 2-3-1化学反应速率练习卷(解析版) 题型:选择题
为了说明影响化学反应进行快慢的因素,甲、乙、丙、丁四位同学分别设计了如下A~D四个实验,你认为结论不正确的是( )
A.大小相同、形状相同的镁条和铝条与相同浓度的盐酸反应时,两者速率一样大
B.在相同条件下,等质量的大理石块和大理石粉与相同浓度的盐酸反应时,大理石粉反应快
C.将浓硝酸分别放在冷暗处和强光照射下,会发现光照可以加快浓硝酸的分解
D.两支试管中分别加入相同质量的氯酸钾,向其中一支试管中再加入少量二氧化锰,同时加热,产生氧气的快慢不同
查看答案和解析>>
科目:高中化学 来源:2014年高一化学人教版必修二 2-3-1化学反应速率练习卷(解析版) 题型:选择题
将5.6g铁粉投入足量的100mL2mol/L稀硫酸中,2min时铁粉刚好完全溶解。下列有关这个反应的反应速率表示正确的是( )
A.铁的反应速率=0.5mol/(L·min)
B.硫酸的反应速率=0.5mol/(L·min)
C.硫酸亚铁的反应速率=0.5mol/(L·min)
D.氢气的反应速率=0.5mol/(L·min)
查看答案和解析>>
科目:高中化学 来源:2014年高一化学人教版必修二 2-2-2发展中的化学电源练习卷(解析版) 题型:选择题
一种新型燃料电池,一极通入空气,另一极通入丁烷气体;电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,它在熔融状态下能传导O2-。下列对该燃料电池的说法中,正确的是( )
A.在熔融的电解质中,O2-由负极移向正极
B.电池的总反应是:2C4H10+13O2=8CO2+10H2O
C.通入空气的一极是正极,电极反应为O2+4e-=2O2-
D.通入丁烷的一极是正极,电极反应为C4H10+26e-+13O2-=4CO2+5H2O
查看答案和解析>>
科目:高中化学 来源:2014年高一化学人教版必修二 2-2-1化学能转化为电能练习卷(解析版) 题型:填空题
利用生活中或实验室中常用的物品,根据氧化还原反应知识和电学知识,自己动手设计一个原电池。请填写下列空白:
(1)实验原理:Fe+2H+=Fe2++H2↑。
(2)实验用品:电极________、________、稀硫酸、________(填写所缺的实验用品)、耳机(或者电流计)。

(3)实验装置:
(4)原电池设计及注意的问题。
①按如图所示连接好实验仪器,注意观察(耳朵听)耳机是否有声音发出,如果没有,可将原电池的两个电极中的一极接触耳机插头上的一极(注意:接触的同时耳机的另一个极是连接在原电池的另一个电极上的),这时可以听见耳机发出“嚓嚓嚓”声音。其原因是:在原电池中,由化学能转化为________。
②如果将装置中的耳机改为电流计,则铁钉应该接电流计的______
极,电极反应是________________;另一极应该接电流计的________极,电极发生了________反应(“氧化”或“还原”)。
查看答案和解析>>
科目:高中化学 来源:2014年高一化学人教版必修二 2-1化学能与热能练习卷(解析版) 题型:填空题
在一个小烧杯里加入约20 g已研磨成粉末的氢氧化钡晶体[Ba(OH)2·8H2O],将小烧杯放在事先已滴有3~4滴水的玻璃片上,然后向烧杯内加入约10 g氯化铵晶体,并立即用玻璃棒迅速搅拌。试回答下列问题:
(1)写出反应的化学方程式:______________。
(2)实验要立即用玻璃棒迅速搅拌的原因是_________________。
(3)如果实验中没有看到“结冰”现象,可能的原因是__________________________(答出三个或三个以上原因)。
(4)如果没有看到“结冰”现象,我们还可以采取哪些方式来说明该反应吸热?__________________________________________________________________________________________(答出两种方案)。
(5)“结冰”现象说明反应是一个________(填“放出”或“吸收”)能量的反应,即断开旧化学键________(填“放出”或“吸收”)能量____________(填“>”或“<”)形成新化学键________(填“吸收”或“放出”)的能量。
(6)该反应在常温下就可以进行,说明______________________。
查看答案和解析>>
科目:高中化学 来源:2014年高一化学人教版必修二 1-3-1离子键练习卷(解析版) 题型:选择题
X元素原子最外层有7个电子。Y元素的原子和X元素的原子次外层都有8个电子。在X与Y形成的离子化合物中,阴、阳离子的电子层结构相同。则X与Y形成的化合物的化学式是( )
A.NaF B.MgCl2 C.NaCl D.CaCl2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com