
【题目】有KOH和Ca(OH)2的混合溶液,pH=13。取此溶液500mL,向其中通入CO2,通入CO2的体积(V)和生成沉淀的物质的量(n)的关系如图所示。图中(V1)为112mL(标准状况),则图中V2、V3的体积(单位为mL)分别是

A. 560、672B. 1008、1120
C. 2240、2352D. 392、504
【答案】B
【解析】
PH=13的溶液中,c(OH-)=0.1mol/L,溶液体积为0.5L,所以n(OH-)=0.05mol。向KOH和Ca(OH)2的混合溶液中通入CO2,CO2先和Ca(OH)2反应生成CaCO3沉淀,通入CO2 V1=112mL即0.005mol时CO2和Ca(OH)2恰好完全反应,生成的CaCO3为0.005mol,消耗的Ca(OH)2为0.005mol,所以n(KOH)=0.05mol-0.005mol×2=0.04mol。再通入的CO2和KOH反应,先生成K2CO3,继续反应生成KHCO3,总反应为:CO2+KOH=KHCO3,所以又通入的CO2为0.04mol,体积为0.896L,即为896mL,所以V2=896+112=1008mL。到B点后,再通入CO2,CO2和CaCO3以及水反应生成溶于水的Ca(HCO3)2:CO2+H2O+ CaCO3=Ca(HCO3)2,0.05mol CaCO3会消耗0.05mol CO2,即为112mL,所以V3=1008+112=1120mL。故选B。


 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案科目:高中化学 来源: 题型:
【题目】下列图中的实验,能达到实验目的的是( )
A.  证明稳定性:Na2CO3>NaHCO3
证明稳定性:Na2CO3>NaHCO3
B.  证明非金属性:Cl>Br>I
证明非金属性:Cl>Br>I
C.  验证镁和盐酸反应的热效应
验证镁和盐酸反应的热效应
D. 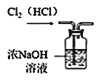 除去 Cl2 中的杂质气体 HCl
除去 Cl2 中的杂质气体 HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“低碳经济”已成为全世界科学家研究的重要课题,其综合利用具有重要意义。回答下列问题:
(1)CO2与CH4经催化重整,制得合成气:CH4(g)+ CO2(g)![]() 2CO (g)+ 2H2(g)
2CO (g)+ 2H2(g)
①已知上述反应中相关的化学键键能数据如下:
化学键 | C—H | C=O | H—H | C |
键能/kJ·mol1 | 413 | 745 | 436 | 1075 |
则该反应的ΔH=_________。有利于提高CH4平衡转化率的条件是____(填标号)。
A.高温低压 B.低温高压 C.高温高压 D.低温低压
②某温度下,在体积为2 L的容器中加入2 mol CH4、1 mol CO2以及催化剂进行重整反应,达到平衡时CO2的转化率是50%,其平衡常数为_______mol2·L-2。
(2)CO2可以被NaOH溶液捕获。若所得溶液c(HCO3)∶c(CO32 -)=2∶1,溶液pH=____。(室温下,H2CO3的K1=4×10-7;K2=5×10-11),0.1mol·L-1 NaHCO3溶液中阴离子的浓度由大到小的顺序为______________
(3)研究证实,CO2也可在酸性水溶液中通过电解生成甲醇,则生成甲醇的反应发生在_______极,该电极反应式是___________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验中“实验内容”与对应“现象或结论”关系都正确的是
选项 | 实验内容 | 实验现象或结论 |
A | 分别往4 mL 0.1 mol/L 、4 mL 0.2 mol/L KMnO4溶液加入2 mL 0.1 mol/L H2C2O4溶液,记录褪色时间 | 浓度越大,反应速率越快越先褪色 |
B | 25℃时,向pH=1的盐酸和醋酸各0.5L的溶液中各加入1.4g铁粉 | 醋酸中生成H2的速率快且最终气体量多 |
C | 以石墨为电极,电解KI溶液(其中含有少量酚酞) | 阴极逸出气体且附近溶液呈现红色 |
D | 向FeCl3+3KSCN | 血红色变浅,说明增加生成物浓度,平衡逆向移动 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,向2L的密闭容器中投入一定量的X和Y,在催化剂的作用下发生反应:X(g) + Y(g)![]() Z(g)。反应过程中测定的部分数据如下表:
Z(g)。反应过程中测定的部分数据如下表:
t/min | n(X)/mol | n(Y)/mol |
0 | 1.20 | 0.60 |
1 | 0.90 | |
2 | 0.80 | |
4 | 0.20 |
下列说法正确的是
A. 反应1~2min末的平均速率v(Z)=0.2mol/(L·min)
B. 在2min~4min间,v(X)正>v(Y)逆
C. 生成1mol Z的同时,生成1mol X能说明该反应已达化学平衡状态
D. 其他条件不变,再充入1.2mol X,X的转化率将增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某元素的一种同位素X的原子质量数为A,含N个中子,它与![]() 原子组成HmX分子.在a克HmX中所含质子的物质的量是( )
原子组成HmX分子.在a克HmX中所含质子的物质的量是( )
A. ![]() (A-N+m)molB.
(A-N+m)molB. ![]() (A-N)molC.
(A-N)molC. ![]() (A-N)molD.
(A-N)molD. ![]() (A-N+m)mol
(A-N+m)mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】开发和利用矿物资源有重要的意义。某厂用无机矿物资源生产部分材料,其产品流程示意图如下,下列有关说法不正确的是( )

A. 制取粗硅时生成的气体产物为CO
B. 生产铝、铜、高纯硅及玻璃的过程中都涉及氧化还原反应
C. 黄铜矿冶炼铜时,产生的SO2可用于生产硫酸,产生的FeO可用作冶炼铁的原料
D. 粗硅制高纯硅时,提纯四氯化硅可用多次分馏的方法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 难溶电解质的溶度积越小,溶解度越大 B. 难溶电解质的溶解平衡是一种动态平衡
C. 可以通过沉淀反应使杂质离子完全沉淀 D. 一定浓度的NH4Cl溶液不能溶解Mg(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是元素周期表的一部分,元素①~⑨在周期表中的位置如图所示,请回答下列问题:

(1)元素⑨在周期表中的位置是_______。
(2)元素①~⑨中,非金属性最强的元素是_______(填元素符号)。
(3)元素①~⑨中,最高价氧化物对应的水化物中,碱性最强的是_______(填化学式),它与元素⑤的最高价氧化物对应水化物反应的离子方程式为_______。
(4)元素⑨的简单氢化物与元素⑦的简单氢化物中更稳定的是_______(填化学式)。
(5)元素③与元素①形成的淡黄色化合物的电子式为_______。
(6)元素①的简单氢化物比元素⑥的简单氢化物的沸点_______(填“高”或“低”),原因是_______。
(7)元素④与元素⑦形成的化合物是_______(填“离子”或“共价”)化合物,用电子式表示其形成过程_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com