
| A. | ①② | B. | ①③ | C. | ②③ | D. | ③④ |
分析 碱性甲醇燃料电池,具有还原性的甲烷为原电池的负极,发生氧化反应,电极反应式为CH3OH+8OH--6e-=CO32-+6H2O,通入氧气的一极为原电池的正极,发生还原反应,电极反应式为O2+2H2O+4e-=4OH-,原电池工作时,电子从负极经外电路流向正极,电解质溶液中,阳离子向正极移动,阴离子向负极移动.
解答 解:甲醇燃料电池,KOH作电解质,总反应:2CH3OH+3O2+4OH-═2CO32-+6H2O,负极:CH3OH+8OH--6e-═CO32-+6H2O,正极:3O2+12e-+6H2O═12OH-,
①燃料电池中,燃料在负极是典型的发生氧化反应,氧气在正极得到电子发生还原反应,故①正确;
②通入甲醇的电极为负极,电极反应为:CH3OH+8OH--6e-=CO32-+6H2O,每消耗1molCH3OH可以向外电路提供6mole-,故②正确;
③通入CH4的电极为负极失电子反应氧化反应,电极反应为:CH3OH+8OH--6e-=CO32-+6H2O,;通入氧气的一极为原电池的正极,得到电子发生还原反应:O2+2H2O+4e-=4OH-,该电池的总反应式为,4KOH+2CH3OH+3O2=2K2CO3+6H2O,故③错误;
④电池反应式为:CH4+2OH-+2O2=CO32-+3H2O,随着反应的进行,溶液中氢氧根离子不断减少,溶液pH不断减小,故④错误;
故选A.
点评 本题考查原电池工作原理,题目难度不大,电极反应式需要注意电解质溶液的酸碱性,明确原电池工作原理为解答关键,试题有利于提高学生的灵活应用能力.


科目:高中化学 来源: 题型:选择题
| A. | Na2CO3的摩尔质量为106 g | |
| B. | 金刚石与石墨互为同位素 | |
| C. | 常温下,4.6gNa中含有的质子数为2.2NA | |
| D. | 标准状况下,11.2LCO2完全参与反应,转移的电子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
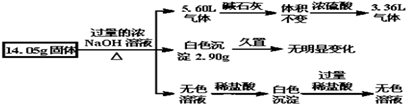
| A. | 一定含有Al,其物质的量为$\frac{5}{3}$mol | |
| B. | 一定不含FeCl2,可能含有MgCl2和AlCl3 | |
| C. | 一定含有(NH4)2SO4和FeCl2 | |
| D. | 一定含有(NH4)2SO4和MgCl2,且物质的量相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
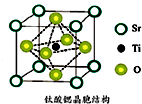 氢能被视作连接化石能源和可再生能源的重要桥梁.
氢能被视作连接化石能源和可再生能源的重要桥梁.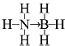 ;与氨硼烷互为等电子体的有机小分子是CH3CH3(写结构简式).
;与氨硼烷互为等电子体的有机小分子是CH3CH3(写结构简式).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(NH4+)相等的NH4HCO3、NH4HSO4、NH4Cl三种溶液的物质的量浓度关系为c(NH4HSO4)>c(NH4HCO3)>c(NH4Cl) | |
| B. | 将10mL0.1mol•L-1Na2CO3溶液逐滴滴加到10mL0.1mol•L-1盐酸中:c(Na+)>c(Cl-)>c(HCO3-)>c(CO32-)>c(OH-) | |
| C. | 室温下,向100mL0.1mol/LNaOH溶液中滴加0.1mol/LNH4HSO4溶液至溶液呈中性,溶液中各离子浓度大小关系:c(Na+)>c(NH4+)>c(SO42-)>c(OH-)=c(H+) | |
| D. | 0.2mol•L-1的某一元弱酸HA溶液和0.1mol•L-1NaOH溶液等体积混合后的溶液:2c(OH-)+c(A-)═2c(H+)+c(HA) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:1 | B. | 2:1 | C. | 3:1 | D. | 1:4 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验方案 | 实验现象 |
| ①用砂纸打磨后的镁带与沸水反应,再向反应液中滴加酚酞. ②向新制的H2S饱和溶液中滴加新制的氯水 ③钠与滴有酚酞试液的冷水反应 ④镁带与2mol/L的盐酸反应 ⑤铝条与2mol/L的盐酸反应 | A.浮于水面,熔成小球,四处游动,逐渐缩小,溶液变红色 B.产生气体,气体可燃,溶液变浅红色 C.反应不十分强烈,产生的气体可燃 D.剧烈反应,产生的气体可燃 E.生成淡黄色沉淀 |
| 实验方案 | 实验现象 | 有关离子方程式 |
| A | ||
| B | 不填 | |
| C | 不填 | |
| D | 不填 | |
| E |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
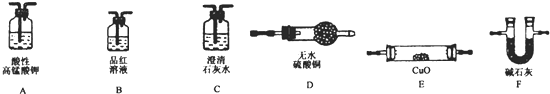
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com