
【题目】根据如图所示的实验装置,回答下列问题:
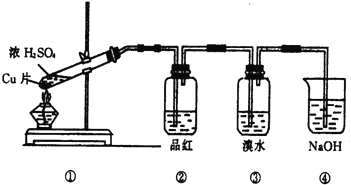
(1)写出铜与浓硫酸反应的化学方程式
(2)证明SO2具有漂白性的现象是 ,再加热该溶液,现象是 .
(3)装置③中的现象是 ,证明SO2具有 .
(4)装置④的作用是 .
【答案】(1)Cu+2H2SO4(浓)![]() CuSO4+2H2O+SO2↑;
CuSO4+2H2O+SO2↑;
(2)褪色;又变为红色;
(3)褪色;还原性;
(4)吸收多余的二氧化硫气体,防止污染空气.
【解析】
(1)浓硫酸和铜在加热的条件下生成硫酸铜、二氧化硫和水,化学方程式为:Cu+2H2SO4(浓)![]() CuSO4+2H2O+SO2↑
CuSO4+2H2O+SO2↑
(2)SO2可以使品红溶液褪色,体现了SO2具有漂白性,SO2的漂白是暂时性的漂白,生成的物质不稳定,受热易分解,重新变为红色
(3)二氧化硫具有较强的还原性,可与溴单质反应生成硫酸和氢溴酸,因此装置③中的现象为溶液褪色
(4)二氧化硫污染空气,二氧化硫可以被氢氧化钠溶液吸收,减少空气污染,因此装置④的作用是:吸收多余的二氧化硫气体,防止污染空气


科目:高中化学 来源: 题型:
【题目】单质X、Y与化合物甲、乙有如图所示的转化关系(必要的反应条件未标出),回答下列问题:

(1)若该反应用于工业上制取粗硅,反应的化学方程式为______________
(2)若X、Y为日常生活中常见的两种金属,且甲为红棕色粉末,相应的化学方程式为_____。
(3)若X、乙的焰色反应均呈黄色,甲是一种常见的无色无味的液体,则乙物质中所含的化学键类型有_________
(4)若X是黄绿色气体,甲、乙两种气体相遇会产生白烟,则X与甲反应的化学方程式为__________。
(5)若X中的元素是海水中含量最多的金属元素,甲是相对分子质量为46且常温下能使酸性KMnO4溶液褪色的烃的含氧衍生物,则X与甲反应的化学方程式为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D是中学化学的常见物质,且A、B、C均含有同一种元素。在一定条件下,它们之间的相互转化关系如图所示(反应中生成的H2O已略去)。

请回答下列问题:
(1)若A是一种常见的强碱,C常用于糕点发酵,则反应①的离子方程 式是__________________。
(2)若A是一种碱性气体,常用作制冷剂,B、D是空气中的主要成分,则C的化学式为_______________。
(3)若A是一种无色、有臭鸡蛋气味的气体,C是导致酸雨的主要气体,则反应③的化学方程式为_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿伏加德罗常数的值为NA,下列说法正确的是
A. 标准状况下,2.24LCH3OH分子中共价键的数目为0.5NA
B. 1molNa2O2与足量CO2充分反应,转移的电子数为2 NA
C. 25℃1LpH=12的Na2CO3溶液中,由水电离出H+的数目为0.01NA
D. 0.1molH2和0.1molI2于密闭容器中充分反应后,HI分子总数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示为一定条件下含碘物质在水溶液中的转化关系图:

(1)转化①中的氧化剂是_____(填化学式)
(2)转化①②③中,碘元素发生氧化反应的是_____(填序号)
(3)转化③中,Cl2发生反应后可能生成以下物质中的_____(填字母)。
A HCl B HClO C.HClO4
(4)转化②的化学方程式为KIO3+KOH+SO2→I2+K2SO4+H2O(未配平)
①配平反应②并用双线桥法表示电子转移的情况_______________
②每生成1.27gI2,反应中转移电子的物质的量为_____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以Cl2、NaOH、(NH2)2CO(尿素)和SO2为原料可制备N2H4·H2O(水合肼)和无水Na2SO3,其主要实验流程如下:

已知:①Cl2+2OH![]() ClO+Cl+H2O是放热反应。
ClO+Cl+H2O是放热反应。
②N2H4·H2O沸点约118 ℃,具有强还原性,能与NaClO剧烈反应生成N2。
(1)步骤Ⅰ制备NaClO溶液时,若温度超过40 ℃,Cl2与NaOH溶液反应生成NaClO3和NaCl,其离子方程式为____________________________________;实验中控制温度除用冰水浴外,还需采取的措施是____________________________________。
(2)步骤Ⅱ合成N2H4·H2O的装置如题19图1所示。NaClO碱性溶液与尿素水溶液在40 ℃以下反应一段时间后,再迅速升温至110 ℃继续反应。实验中通过滴液漏斗滴加的溶液是_____________;使用冷凝管的目的是_________________________________。

(3)步骤Ⅳ用步骤Ⅲ得到的副产品Na2CO3制备无水Na2SO3(水溶液中H2SO3、![]() 、
、![]() 随pH的分布如题19图2所示,Na2SO3的溶解度曲线如题19图3所示)。
随pH的分布如题19图2所示,Na2SO3的溶解度曲线如题19图3所示)。

①边搅拌边向Na2CO3溶液中通入SO2制备NaHSO3溶液。实验中确定何时停止通SO2的实验操作为_________________。
②请补充完整由NaHSO3溶液制备无水Na2SO3的实验方案: _______________________,用少量无水乙醇洗涤,干燥,密封包装。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】a、b、c、d、e五种短周期元素的原子半径和最外层电子数之间的关系如图所示:下列说法正确的是
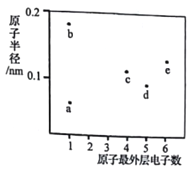
A. 离子半径:b>d
B. 沸点:a与d形成的化合物>a与c形成的化合物
C. a与b、c、d、e均可形成共价化合物
D. e的含氧酸可能既有氧化性又有还原性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】掌握仪器名称、组装及使用方法是中学化学实验的基础,下图为实验装置。

(1)写出下列仪器的名称:a._____________________ b. __________________
(2)若利用此装置分离四氯化碳和酒精的混合物,还缺少的仪器是 ________ ,将仪器补充完整后进行实验,温度计水银球的位置在______________处。冷凝水由__________(填f或g) 口通入,_____ 口流出。
(3)进行蒸馏操作时,需在a装置中加入__________________,目的_________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组在实验室探究过渡金属元素化合物的性质
I、铁及其化合物

(1)向FeSO4溶液中滴加NaOH溶液,产生白色沉淀,但迅速变为灰绿色,最终变为红褐色,为顺利看到较长时间的白色沉淀,设计了图①装置:①检查装置气密性,装入药品;②打开止水夹K;③在试管b出口收集气体并验纯;④关闭止水夹K。以上操作正确的顺序是:___。
(2)某实验小组称量3.60 g草酸亚铁晶体(FeC2O4·2H2O)加热过程中,固体质量变化如图②所示:
①请写出AB段发生反应的化学方程式:___。②C点成分为:___。
(3)向FeCl3溶液中加入过量Na2SO3溶液,设计实验证明两者发生了氧化还原反应并且为可逆反应。(简要说明实验步骤、现象和结论,仪器和药品自选)___。
II、铜及其化合物
向2ml0.2mol·L-1Na2SO3溶液中滴加0.2mol·L-1CuSO4溶液,发现溶液变绿,继续滴加产生棕黄色沉淀,经检验,棕黄色沉淀中不含SO42-,含有Cu+、Cu2+和SO32-。
已知:Cu+![]() Cu+Cu2+,Cu2+
Cu+Cu2+,Cu2+![]() CuI↓(白色)+I2。
CuI↓(白色)+I2。
(4)用稀硫酸证实沉淀中含有Cu+的实验现象是___。
(5)向洗净的棕黄色沉淀中加入足量KI溶液,产生白色沉淀,继续向上层清液中加入淀粉溶液并没有变蓝的现象出现,请结合离子反应方程式解释不变蓝的原因___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com