


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、2.3g金属钠变成钠离子时,失去的电子数为0.2NA |
| B、常温常压下,11.2L氯气中所含的原子数目为NA |
| C、通常状况下,32g氧气所含有的原子数目为2NA |
| D、100ml 2mol?L-1的氯化钠溶液中含各离子数目之和为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铜是一种紫红色金属 |
| B、铜是热和电的良导体 |
| C、铜在自然界中主要以单质的形式存在 |
| D、铜是人类使用最早、应用最广泛的金属之一 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、CO2的电子式 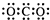 | ||
B、Cl-的结构示意图  | ||
| C、硫离子的核外电子排布式1s22s63s23p4 | ||
D、质量数为37的氯原子
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①② | B、②④ | C、①④ | D、①③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
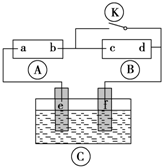 如图所示,A为直流电源,B为浸透饱和氯化钠溶液和酚酞溶液的滤纸,C为装CuSO4溶液的电解槽,e、f均为石墨电极,按图接通电路,发现B上的c点显红色,请填空:
如图所示,A为直流电源,B为浸透饱和氯化钠溶液和酚酞溶液的滤纸,C为装CuSO4溶液的电解槽,e、f均为石墨电极,按图接通电路,发现B上的c点显红色,请填空:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、本实验可选石蕊作指示剂 |
| B、锥形瓶用水洗净后再用待测液润洗2~3次 |
| C、移液管取盐酸后,垂直放入稍倾斜的锥形瓶中并使管尖与内壁接触 |
| D、滴定过程中眼睛应始终注视滴定管内液面变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、MgO、Al2O3、SiO2 |
| B、硫酸钾、碳酸钾、硫酸铝三种溶液 |
| C、氯化镁、氯化铝、氯化钠三种溶液 |
| D、硫酸铵、硝酸铵、氯化铵三种溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com