
| A、①② | B、②④ | C、①④ | D、①③ |


科目:高中化学 来源: 题型:
A、标准状况下,密度为ρg?L-1的某气体纯净物一个分子的质量为
| ||
| B、17g甲基(-14CH3)所含电子数为7NA | ||
| C、在含有4mol Si-O键的石英晶体中,氧原子的数目为4NA | ||
| D、常温下,0.2mol Cl2溶于等体积水中,转移电子数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
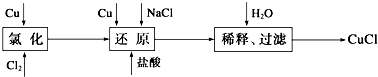
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、35.5:108 |
| B、l:2 |
| C、108:35.5 |
| D、8:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,22.4L乙醇中含有的氧原子数为NA |
| B、标准状况下,1.12L16O2和1.12L18O2均含有0.1NA个氧原子 |
| C、在Na2O2与水的反应中,生成lmolO2转移的电子数为 4×6.02×1023 |
| D、25℃时,pH=13的Ba(OH)2溶液中含有OH-数目为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| O | 2- 7 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加水,用湿润的红色石蕊试纸放在试管口检验 |
| B、将固体加热,用湿润的红色石蕊试纸放在试管口检验 |
| C、加入NaOH溶液,加热,用湿润的红色石蕊试纸放在试管口检验 |
| D、加入NaOH溶液,加热,滴入无色酚酞 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com