
| A、M g | ||
B、
| ||
C、
| ||
D、
|
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、石英与烧碱溶液反应:SiO2+2OH-═SiO32-+H2O |
| B、硅与烧碱溶液反应:Si+2OH-+H2O═SiO32-+2H2↑ |
| C、向小苏打溶液中加入过量的石灰水:2HCO3-+Ca2++2OH-═CaCO3↓+2H2O+CO32- |
| D、往水玻璃中加入盐酸:2H++SiO32-═H2SiO3↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 成分 | Na+ | K+ | Ca2+ | Mg2+ | Cl- | SO42- | HCO3- |
| 含量/mg?L-1 | 9360 | 83 | 200 | 1100 | 16000 | 1200 | 118 |
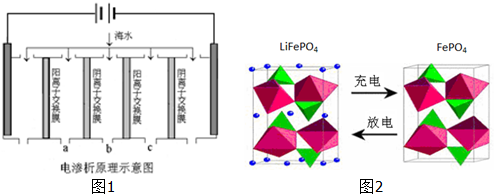
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①② | B、②④ | C、①④ | D、①③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
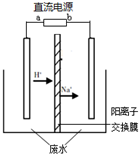 电解CH3CHO是有毒物质,易溶于水,含高浓度CH3CHO的废水可以用隔膜电解法处理,总反应为:
电解CH3CHO是有毒物质,易溶于水,含高浓度CH3CHO的废水可以用隔膜电解法处理,总反应为:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、本实验可选石蕊作指示剂 |
| B、锥形瓶用水洗净后再用待测液润洗2~3次 |
| C、移液管取盐酸后,垂直放入稍倾斜的锥形瓶中并使管尖与内壁接触 |
| D、滴定过程中眼睛应始终注视滴定管内液面变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 容器编号 | 起始时各物质的物质的量/mol | 平衡时反应中的能量变化 | ||
| N2 | H2 | NH3 | ||
| ① | 1 | 3 | 0 | 放出热量a kJ |
| ② | 2 | 3 | 0 | 放出热量b kJ |
| ③ | 2 | 6 | 0 | 放出热量c kJ |
| A、反应的速率:③>①>② |
| B、达到平衡时氨气的浓度:①>② |
| C、放出的热量(kJ):a<b<92.4 |
| D、反应得到1mol NH3(l),放出热量46.2kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、BaCl2溶液 |
| B、NaOH溶液 |
| C、AgNO3溶液 |
| D、Ba(OH)2溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com