
����Ŀ����Ҫ����գ�
(1)�ڵڶ�������(ϡ���������)����һ����������Ԫ�ص�ԭ�ӽṹʾ��ͼ��___����һ��������С��Ԫ�صĵ����Ų�ͼΪ___��
(2)������һЩԭ�ӵ�2p�ܼ���3d�ܼ��е����Ų�����������жϣ���ЩΥ��������������ԭ������ЩΥ���˺��ع���
��![]() ��
��![]() ��
�� ![]() ��
��![]() ��
�� ![]() ��
�� ![]()
Υ������������ԭ������__��Υ�����ع������___��
(3)��VSEPRģ�ͺ��ӻ�����������֪ʶ�����
���ӻ����� | ����ԭ�ӹ���ӻ���ʽ | ���ӻ����ӵ�����ṹ | ���������� |
CH2O | ________ | _______ | _____ |
NH4+ | ________ | _______ | _____ |
CS2 | ________ | _______ | _____ |
���𰸡�![]()
 �� �ڢܢ� sp2 ƽ�������� �� sp3 ���������� �� sp ֱ���� ��
�� �ڢܢ� sp2 ƽ�������� �� sp3 ���������� �� sp ֱ���� ��
��������
(1)ͬ����Ԫ�ص�һ�����ܳ��������ƣ��ڵڶ�������(ϡ���������)����һ����������Ԫ����F����ԭ�ӽṹʾ��ͼΪ![]() ����һ��������С��Ԫ����Li��������Ų�ͼΪ
����һ��������С��Ԫ����Li��������Ų�ͼΪ ��
��
�ʴ�Ϊ��![]() ��
�� ��
��
(2)����������ԭ��ָ��ԭ���в��������˶�״̬��ȫ��ͬ�ĵ��ӣ�ÿһ�����ֻ�����������෴���������ӣ�Υ����ԭ�����Т٣����ع������ڵȼ۹��(��ͬ���Ӳ㡢�����Dz��ϵĸ������)���Ų��ĵ��ӽ������ܷ�ռ��ͬ�Ĺ����������������ͬ���ڢܢ�Υ���˺��ع���
�ʴ�Ϊ���٣��ڢܢݣ�
(3) CH2O����̼ԭ�ӵļ۲���Ӷ���=![]() ��̼ԭ�Ӳ���sp2�ӻ����µ��Ӷԣ�����Ϊƽ�������νṹ��������������IJ����غϣ���Ϊ���Է��ӣ�NH4+���ĵ�ԭ�ӵļ۵��Ӷ���=
��̼ԭ�Ӳ���sp2�ӻ����µ��Ӷԣ�����Ϊƽ�������νṹ��������������IJ����غϣ���Ϊ���Է��ӣ�NH4+���ĵ�ԭ�ӵļ۵��Ӷ���=![]() ��̼ԭ�Ӳ���sp3�ӻ����µ��Ӷԣ�����Ϊ���������Σ���������������غϣ���Ϊ�Ǽ��Է��ӣ�CS2����̼ԭ�ӵļ۲���Ӷ���=
��̼ԭ�Ӳ���sp3�ӻ����µ��Ӷԣ�����Ϊ���������Σ���������������غϣ���Ϊ�Ǽ��Է��ӣ�CS2����̼ԭ�ӵļ۲���Ӷ���=![]() ��̼ԭ�Ӳ���sp�ӻ�������Ϊֱ���Σ���������������غϣ���Ϊ�Ǽ��Է��ӣ�
��̼ԭ�Ӳ���sp�ӻ�������Ϊֱ���Σ���������������غϣ���Ϊ�Ǽ��Է��ӣ�
�ʴ�Ϊ��sp2��ƽ�������Σ��У�sp3�����������Σ��ޣ�sp��ֱ���Σ��ޣ�


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���й�![]() ��˵����ȷ����
��˵����ȷ����
A������̼ԭ�Ӳ����ܶ���ͬһƽ����
B�����ֻ������9��̼ԭ����ͬһƽ����
C����7��̼ԭ�ӿ�����ͬһֱ����
D��ֻ������5��̼ԭ����ͬһֱ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A.��ʢ������ͭ��Һ���Թ�����������ˮ�����õ�����ɫ�ģ�Cu(NH3)4]SO4��H2O����
B.CH4�����е�sp3�ӻ��������4��Hԭ�ӵ�1s�����Cԭ�ӵ�2p�������������γɵ�
C.�ӻ����ֻ�����γ���������������δ����ɼ��ŵ��Ӷ�
D.��AB3�͵Ĺ��ۻ����������ԭ��A������sp3�ӻ�����ɼ��������幹�ζ�����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ��������������������ء������й�˵������ȷ���ǡ�
A.����10�ŷɴ�����̫���ܵ�ذ�ɽ�����ת��Ϊ���ܣ�����ת�������Ƕ�������
B.����ˮ��ʱ�������������ԵĽ������ӣ�������������ˮ��ɱ������
C.![]() ����Ư���ԣ�������Ư��ֽ����Ҳ���Դ�������Ư��ʳƷ
����Ư���ԣ�������Ư��ֽ����Ҳ���Դ�������Ư��ʳƷ
D.���������������ͨ�������ճ�������Ҳ���ô�����Һ����ȥ��Ʒ���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������Ȼ�ѧ����ʽ������C(s)��ȼ���ȡ�H����( )
C(s) + H2O(l) = CO(g) + H2(g) ��H1=175.3kJ��mol-1
2CO(g) + O2(g) = 2CO2(g)��H2= ��566.0 kJ��mol-1
2H2(g) + O2(g) = 2H2O(l) ��H3= ��571.6 kJ��mol-1
A.��H1+��H2����H3B.2��H1+��H2+��H3
C.��H1+��H2/2 +��H3D.��H1+��H2/2 +��H3/2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ӵ�ʳ���м���ĵ������һ�ְ�ɫ�ᾧ��ĩ�������º��ȶ���������560�濪ʼ�ֽ⡣�����������µ������һ�ֽ�ǿ��������������⻯��������εȻ�ԭ�����ʷ�Ӧ����ҵ��������ص��������£�
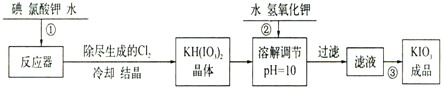
��1����֪����ٷ�Ӧ�������ķ�ӦΪ��6I2+11KClO3+3H2O=6KH(IO3)2+5KCl+3Cl2�����÷�Ӧ�Ļ�ԭ����Ϊ___��
��2�������±�����ص��ܽ�ȣ������۵õ�����ؾ��壬�㽨��ķ�����___��
�¶�/�� | 20 | 40 | 60 | 80 |
KIO3g/100gˮ | 8.08 | 12.6 | 18.3 | 244.8 |
��3������֪��KIO3+3H2SO4+5KI=3K2SO4+3I2+3H2O��I2+2S2O32-=2I-+S4O62-��
�ⶨ�ӵ�ʳ���е�ĺ�����ѧ������Ƶ�ʵ�鲽�����£�
a.ȷ��ȡwgʳ�Σ�����������ˮʹ����ȫ�ܽ⣻
b.��ϡ�����ữ������Һ���������KI��Һ��ʹKIO3��KI��Ӧ��ȫ��
c.�Ե���Ϊָʾ������μ������ʵ���Ũ��Ϊ2.00��10-3mol��L-1��Na2S2O3��Һ10.0mL��ǡ�÷�Ӧ��ȫ����ӵ�ʳ����Ʒ�еĵ�Ԫ�غ�����___mol��kg-1(�Ժ�w�Ĵ���ʽ��ʾ)��
��ѧ�����ֽ���������ʵ�飺
�������� | ʵ������ |
ȡ1g������NaCl����3mLˮ������Һ | ��Һ�ޱ仯 |
����5�ε�����Һ��1mL0.1mol��L-1KI��Һ���� | ��Һ�ޱ仯 |
Ȼ���ٵ���1��1mol��L-1��H2SO4���ӷ��� | ��Һ����ɫ |
���Ʋ�ʵ���в�����ɫ����Ŀ���ԭ�������ӷ���ʽ��ʾ___��
����ѧ���ҵ�ʵ���������ѧ����ʵ����������Ҫ���ۣ�___��
��4��ijѧϰС��Լӵ��ν�������ʵ�飺ȡһ����ij�ӵ���(���ܺ���KIO3��KI��Mg2+��Fe3+)������������ˮ�ܽ⣬����ϡ�����ữ����������Һ��Ϊ3�ݡ���һ����Һ�еμ�KSCN��Һ���Ժ�ɫ���ڶ�����Һ�м�����KI���壬��Һ�Ե���ɫ����CCl4��ȡ���²���Һ���Ϻ�ɫ����������Һ�м�������KIO3����μӵ����Լ�����Һ����ɫ��
�ٸ�������ʵ�����ӵ����п��ܺ��е������в���ȷ������___��
�ڵڶ�����Һ�м�������KI�����Ӧ�����ӷ���ʽΪ___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ��Ƽ�������������������ء������й�˵������ȷ���ǡ�
A.���øߴ����ʹ�İ뵼�����ܣ������Ƴɹ��أ�������ֱ��ת��Ϊ����
B.��Ȼ����������ˮú���ֱ����ڻ�ʯ��Դ����������Դ�Ͷ�����Դ
C.�ҹ����ҹ���001A�ͺ�ĸ���ڽ��ػ�����������������ָ��£����ڽ�������
D.�������ۿ��Ը�Чȥ����Ⱦˮ���е�![]() ��
��![]() ��
��![]() ��
��![]() ���ؽ������ӣ��䱾�����������۶��ؽ��������н�ǿ����������
���ؽ������ӣ��䱾�����������۶��ؽ��������н�ǿ����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijʵ��С����H2O2�ֽ�Ϊ����̽��Ũ�ȡ���������Һ����ԶԷ�Ӧ���ʵ�Ӱ�졣�ڳ����°������±���ʾ�ķ������ʵ�顣
ʵ���� | ��Ӧ�� | ���� |
�� | 10 mL 2% H2O2��Һ | �� |
�� | 10 mL 5% H2O2��Һ | �� |
�� | 10 mL 5% H2O2��Һ | 1 mL 0.1 mol��L-1 FeCl3��Һ |
�� | 10 mL 5% H2O2��Һ+����HCl��Һ | 1 mL 0.1 mol��L-1 FeCl3��Һ |
�� | 10 mL 5% H2O2��Һ+����NaOH��Һ | 1 mL 0.1 mol��L-1 FeCl3��Һ |
(1)ʵ��ٺ͢ڵ�Ŀ����__________��ͬѧ�ǽ���ʵ��ʱû�й۲쵽������������ó����ۡ�������ʾ��ͨ��������H2O2�ȶ������ֽ⡣Ϊ�˴ﵽʵ��Ŀ�ģ����ԭʵ�鷽���ĸĽ�������_________(��һ�ַ�������)��
(2)ʵ��ۢܢ��У�������������������ʱ��仯�Ĺ�ϵ��ͼ��ʾ��
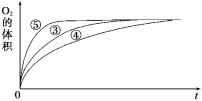
������ͼ�ܹ��ó���ʵ�������___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��800��ʱ����2L�����ܱ�������Ͷ��0.20molNO��0.12mol O2�������з�Ӧ2NO(g)��O2(g) ![]() 2NO2(g)��n(NO)��ʱ��ı仯������±���
2NO2(g)��n(NO)��ʱ��ı仯������±���
ʱ��/s | 0 | 1 | 2 | 3 | 4 |
n(NO)/mol | 0.20 | 0.10 | 0.08 | 0.04 | 0.04 |
��1��800��ʱ���÷�Ӧƽ��ʱ��NO�����ʵ���Ũ��Ϊ______�������¶ȣ�NO��ƽ��Ũ��Ϊ0.03molL-1����÷�ӦΪ_______��Ӧ(��������������������)��
��2����O2��ʾ0��2s�ڸ÷�Ӧ��ƽ����Ӧ����v(O2)��______��
��3����˵���÷�Ӧһ���ﵽƽ��״̬����______��
a v(NO2)��2v(O2)���� b ������ѹǿ���ֲ���
c ������������ɫ���ֲ��� d �����������ܶȱ��ֲ���
��4�� ƽ������д�ʩ��ʹ�÷�Ӧ������Ӧ�����ƶ���������Ӧ�����������____��
a �ʵ������¶� b �ʵ������¶�
c ����O2��Ũ�� d ѡ���Ч����
��5��800��ʱ��������Ӧ��ƽ�ⳣ��K��______���������к�1.00 molL-1 NO��2.00 molL-1O2��2.00 molL-1 NO2�����ʱv��_______v�� (������������������������)��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com