
【题目】A﹣G是初中化学中常见的物质,其相互反应及转化关系如图所示,部分反应条件省略.已知A是易与人体血红蛋白结合的有毒气体,B是赤铁矿的主要成分,C是相对分子质量最小的氧化物,F是最轻的气体.

(1)G的化学式为____________。
(2)写出相应反应的化学方程式:①____________。②____________。
(3)反应③的实验现象是____________。
【答案】 Fe3O4 3CO+Fe2O3![]() 2Fe+3CO2 2H2O
2Fe+3CO2 2H2O![]() 2H2↑+O2↑ 火星四射,剧烈燃烧,生成黑色固体
2H2↑+O2↑ 火星四射,剧烈燃烧,生成黑色固体
【解析】A是易与人体血红蛋白结合的有毒气体,A是CO,B是赤铁矿的主要成分,B是Fe2O3,CO与氧化铁反应生成铁和CO2,C是相对分子质量最小的氧化物,F是最轻的气体,F是氢气,则C是H2O,E是氧气,氧气和D反应生成G,则D是铁,G是四氧化三铁。
(1)根据以上分析可知G的化学式为Fe3O4。(2)反应①的化学方程式为3CO+Fe2O3![]() 2Fe+3CO2。反应②的化学方程式为2H2O
2Fe+3CO2。反应②的化学方程式为2H2O![]() 2H2↑+O2↑。(3)铁在氧气中燃烧的实验现象是火星四射,剧烈燃烧,生成黑色固体。
2H2↑+O2↑。(3)铁在氧气中燃烧的实验现象是火星四射,剧烈燃烧,生成黑色固体。


科目:高中化学 来源: 题型:
【题目】一小块钠置于空气中,产生下列现象:①变成白色粉末②变暗③变成白色固体④有“液滴”出现上述现象出现的先后顺序是( )
A. ①②③④B. ②③①④C. ②③④①D. ③②④①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于σ键和π键的理解不正确的是( )
A.σ键能单独形成,而π键一定不能单独形成
B.σ键可以绕键轴旋转,π键一定不能绕键轴旋转
C.双键中一定有一个σ键、一个π键,三键中一定有一个σ键、两个π键
D.气体单质中一定存在σ键,可能存在π键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用铁片与稀硫酸反应制取氢气时,下列措施不能使氢气生成速率加快的是( )
A. 加热升高温度 B. 改用98%浓硫酸
C. 滴加少量硫酸铜溶液 D. 不用铁片,改用铁粉
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A~G是几种烃的分子球棍模型(如图),据此回答下列问题:
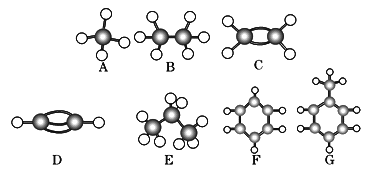
(1)常温下含碳量最高的气态烃是 (填字母).
(2)能够发生加成的烃有 种.
(3)一卤代物种类最多的是 (填写字母).
(4)写出实验室制D的化学方程式 .
(5)写出F发生硝化反应的化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:

苯 | 溴 | 溴苯 | |
密度/g·cm-3 | 0.88 | 3.10 | 1.50 |
沸点/℃ | 80 | 59 | 156 |
水中溶解度 | 微溶 | 微溶 | 微溶 |
按以下合成步骤回答问题:
(1)在a中加入15mL无水苯和少量铁屑。在b中小心加入4.0mL液态溴.向a中滴入几滴溴,有白雾产生,是因为生成了_________气体,继续滴加至液溴滴完。装置d的作用是_________;
(2)液溴滴完后,经过下列步骤分离提纯:
①向a中加入10mL水,然后过滤除去未反应的铁屑;
②滤液依次用10mL水、8mL10%的NaOH溶液、10mL水洗涤.NaOH溶液洗涤的作用是_________;
③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤.加入氯化钙的目的是_________;
(3)经以上分离操作后,粗溴苯中还含有的主要杂质为_________,要进一步提纯,下列操作中必须的是____________(填入正确选项前的字母);
A.重结晶 B.过滤 C.蒸馏 D.萃取
(4)在该实验中,a的容积最适合的是_____________(填入正确选项前的字母):
A.25mL B.50mL C.250mL D.500mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机物的说法正确的是
A. 丁烷的一氯代物有5种
B. 苯与溴水可发生加成反应
C. 以苯甲醇为原料可生成苯甲酸
D. HOCH2CH=CHCOOH能发生酯化、加聚、水解等反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学—选修3:物质结构与性质】
绿柱石被国际珠宝界公认为四大名贵宝石之一。主要成分为Be3Al2[Si6O18],因含适量的Cr2O3(0.15~0.6%),而形成祖母绿。试回答下列问题:
(1)基态Al原子中,电子填充的最高能级是_______,基态Cr原子的价电子排布式是_____。
(2)用“>”或“<”填空:
第一电离能 | 键能 | 沸点 | 离子半径 |
Be_____B | C—C_____Si—Si | H2S_____H2O | Al3+_____O2- |
(3)BeCl2分子的空间构型是______,它的二聚体Be2Cl4结构如右图所示,其中Be原子的杂化方式是_____。
![]()

(4)强还原剂LiAlH4能将SiCl4还原成SiH4,试写出SiH4在空气中自燃的化学方程式______。
(5)Be的氧化物的立方晶胞结构如右图所示,已知氧化铍晶体的密度为ρg·cm-3,则晶胞连长为___cm(设NA为阿伏加德罗常数的值,用含NA、ρ的代数式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com