
【题目】下列关于有机物的说法正确的是
A. 丁烷的一氯代物有5种
B. 苯与溴水可发生加成反应
C. 以苯甲醇为原料可生成苯甲酸
D. HOCH2CH=CHCOOH能发生酯化、加聚、水解等反应
 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案 导学与测试系列答案
导学与测试系列答案科目:高中化学 来源: 题型:
【题目】把卷成螺旋状的铜丝在酒精灯外焰上加热,使表面变黑,然后迅速伸到无水酒精中,有什么现象_______________________铜丝在反应中起的作用__________,写出这个反应的化学方程_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A﹣G是初中化学中常见的物质,其相互反应及转化关系如图所示,部分反应条件省略.已知A是易与人体血红蛋白结合的有毒气体,B是赤铁矿的主要成分,C是相对分子质量最小的氧化物,F是最轻的气体.

(1)G的化学式为____________。
(2)写出相应反应的化学方程式:①____________。②____________。
(3)反应③的实验现象是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各关系式中能说明反应N2+3H2![]() 2NH3已达到平衡状态的是( )
2NH3已达到平衡状态的是( )
A. 3v正(N2)=v正(H2) B. v正(N2)=v逆(NH3)
C. 2v正(H2)=3v逆(NH3) D. v正(N2)=3v逆(H2)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)阅读、分析下列两个材料:
材料一

材料二
物质 | 熔点/℃ | 沸点/℃ | 密度/(g·cm3) | 溶解性 |
乙二醇(C2H6O2) | 11.5 | 198 | 1.11 | 易溶于水和乙醇 |
丙三醇(C3H8O3) | 17.9 | 290 | 1.26 | 能跟水、乙醇以任意比互溶 |
请选择正确的分离方法(填字母):
①将纯碱从氯化钠和纯碱的混合物中分离出来,最好应用________。
②将乙二醇和丙三醇相互分离的最佳方法是_________。
A.蒸馏法 B.萃取法 C.“溶解、结晶、过滤”的方法 D.分液法
(2)阅读材料三:
在溶解性方面,Br2(溴)与I2很相似,其稀的水溶液显黄色。在实验室里从溴水(Br2的水溶液)中提取Br2和提取I2的方法相似。
①常用的提取方法是________________,化学试剂是________,最主要的仪器是__________。
②若观察发现提取Br2以后的水还有颜色,解决该问题的方法是________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用勒夏特列原理解释的是
A.光照新制的氯水时,溶液的pH逐渐减小
B.氨水应密闭保存于低温处
C.打开汽水瓶时,有大量气泡逸出
D.高温高压有利于N2和H2转化为NH3:N2(g)+3H2(g)![]() 2NH3(g) ΔH<0
2NH3(g) ΔH<0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钙及其化合物在生产、生活中的应用比较广泛。
回答下列问题:
(1)草酸钙(CaC2O4)常用于陶瓷上釉。将草酸钙溶于强酸可得草酸(H2C2O4),再加入KMnO4溶液发生氧化还原反应。此反应的氧化产物为_____________(填化学式)。
(2)碳酸钙可用于煤燃烧时的脱硫。
已知:反应I :CaCO3(s)=CaO(s)+CO2(g) △H1= +178.3 kJ mol-1;
反应II:CaO(s)+SO2(g)=CaSO3(s) △H2= -402.0 kJ mol-1;
反应III:2CaSO3(s)+O2(g)=2CaSO4(s) △H3= -2314.8 kJ mol-1 △H3= -2314.8 kJ mol-1。
① 反应2CaCO3(s)+2SO2(g)+O2(g)=2CaSO4(s)+2CO2(g)的△H=______kJ mol-1。

② 向某恒温密闭容器中加入CaCO3,发生反应I,反应达到平衡后,t1时,缩小容器体积,x随时间(t)的变化关系如图1所示,x可能是____________(任写两个)。
(3)将Ca(OH)2加入Na2WO4碱性溶液中,发生反应IV:WO42-(aq)+Ca(OH)2(s) ![]() CaWO4(s)+2OH-(aq)
CaWO4(s)+2OH-(aq)
① 反应IV在较高温度下才能自发进行,则△S_____0(填“>”“=”或“<”,下同),△H_______0。
② T1时,Ksp(CaWO4)=1×10-10,Ksp[Ca(OH)2]=1×10-8,反应Ⅳ:WO42-(aq)+Ca(OH)2(s) ![]() CaWO4(s)+2OH-(aq)的平衡常数K=______;请在图2中画出T1下Ca(OH)2和CaWO4的沉淀溶解平衡曲线。
CaWO4(s)+2OH-(aq)的平衡常数K=______;请在图2中画出T1下Ca(OH)2和CaWO4的沉淀溶解平衡曲线。
③制取CaWO4时,为了提高WO42-的转化率,常需要适时向反应混合液中添加少量的某种稀酸,该稀酸可能为_______(填选项字母)。
A.稀盐酸 B.稀硝酸 C.稀硫酸 D.碳酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素及其化合物的知识是高中化学重要的组成部分,是考查化学基本概念和理论、化学计算、化学实验知识的载体。
(1)元素周期表1-20号元素中,某两种元素的原子序数相差3,周期数相差1。
①这样的两种元素的组合有________种。
②若这样的两种元素形成的化合物中原子数之比为1∶1。
写出其中一种化合物的名称:_______________________;
(2)A是自然界存在最广泛的ⅡA族元素,常以化合物F存在.从单质A起始发生的一系列化学反应可由下图表示:
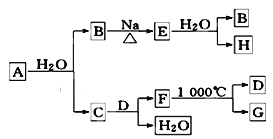
请回答下列问题:
①F的化学式为________,D的电子式为________________。
②E与水反应的化学方程式为___________________________________________;
③实际生产中,可由F为原料制备单质A,写出制备过程的化学方程式(不需考虑综合经济效益)_______________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com