
| 元素 | 部分结构知识 | 部分性质 |
| X | X的单质由双原子分子构成,分子中有14个电子 | X有多种氧化物,如XO、XO2、X2O4等;通常情况下XO2与X2O4共存 |
| Y | Y原子的次外层电子数等于最外层电子数的一半 | Y能形成多种气态氢化物 |
| Z | Z原子的最外层电子数多于4 | Z元素的最高正化合价与最低负化合价代数和等于6 |
| W | W原子的最外层电子数等于2n-3(n为原子核外电子层数) | 化学反应中W原子易失去最外层电子形成Wn+ |
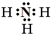 ;Z为Cl元素,有3个电子层,最外层有7个电子,在周期表中位于第三周期第ⅦA族,
;Z为Cl元素,有3个电子层,最外层有7个电子,在周期表中位于第三周期第ⅦA族,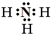 ;第三周期第ⅦA族;
;第三周期第ⅦA族; Al(OH)3+3H+,溶液的pH<7,
Al(OH)3+3H+,溶液的pH<7, Al(OH)3+3H+;
Al(OH)3+3H+;

科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 甲 | 乙 | 丙 | 丁 | |
| 化合物中各元素 原子个数比 | A:C=1:1 | B:A=1:2 | D:E=1:3 | B:E=1:4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、丙醛 | B、丁醛 |
| C、3-甲基丁醛 | D、己醛 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
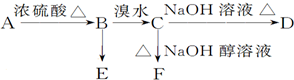 已知有机物A、B、C、D、E、F之间的转化关系如图所示.D是常用做汽车发动机的抗冻剂,E为聚合物,F是一种烃,其相对分子量为26.根据信息回答下列问题.
已知有机物A、B、C、D、E、F之间的转化关系如图所示.D是常用做汽车发动机的抗冻剂,E为聚合物,F是一种烃,其相对分子量为26.根据信息回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:
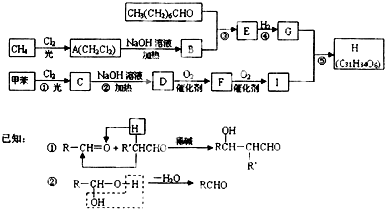
查看答案和解析>>
科目:高中化学 来源: 题型:
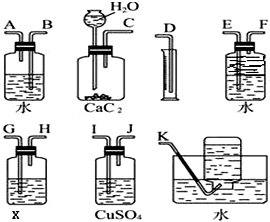 实验室用电石和水反应制备乙炔,其中含有杂质,为了净化和检验乙炔气体,并通过测定气体体积计算电石纯度,按下列要求填空(X为含溴3.2%的四氯化碳溶液150g)
实验室用电石和水反应制备乙炔,其中含有杂质,为了净化和检验乙炔气体,并通过测定气体体积计算电石纯度,按下列要求填空(X为含溴3.2%的四氯化碳溶液150g)查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com