
【题目】下列反应的离子方程式正确的是( )
A.稀硫酸与氢氧化钡溶液混合:Ba2++SO ![]() +OH﹣+H+═H2O+BaSO4↓
+OH﹣+H+═H2O+BaSO4↓
B.Cl2通入水中:Cl2+H2O═H++Cl﹣+HClO
C.将钠加入硫酸铜溶液中的反应:2Na+2Cu2+═2Na++Cu
D.铜片投入稀硫酸中:Cu+2H+═Cu2++H2↑
科目:高中化学 来源: 题型:
【题目】常温下,有浓度均为1 mol·L-1的下列4种溶液:
①H2SO4溶液②NaHCO3溶液③NH4Cl溶液④NaOH溶液
(1)这4种溶液pH由大到小的顺序是 ,其中由水电离的H+浓度最小的是 。(均填序号)
(2)②中各离子浓度由大到小的顺序是 ,NaHCO3的水解平衡常数Kh= mol·L-1。(已知碳酸的电离常数K1=4×10-7,K2=5.6×10-11)
(3)向③中通入少量氨气,此时![]() 的值 (填“增大”、“减小”或“不变”)。
的值 (填“增大”、“减小”或“不变”)。
(4)若将③和④混合后溶液恰好呈中性,则混合前③的体积 ④的体积(填“大于”、“小于”或“等于”之一)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示各物质之间的转化关系.已知D、E、Z是中学化学常见的单质,其他都是化合物.Z、Y是氯碱工业的产品.D元素的原子最外层电子数与电子层数相等,且D的硫酸盐可作净水剂.E为日常生活中应用最广泛的金属.除反应①外,其他反应均在水溶液中进行.请回答下列问题.
(1)写出X的电子式: .
(2)常温时pH=12的G溶液中,溶质的阳离子与溶质的阴离子浓度之差为(写出计算式).
(3)在电镀工业中,若将E作为待镀金属,铜为镀层金属,则铜是极,请写出在E电极上发生的电极反应式: .
(4)写出反应③的离子方程式: .
(5)现有无标签的Y和M的两种无色水溶液,不用其他任何试剂,请你设计一个简单的实验对这两种溶液加以鉴别(回答实验操作、现象及结论).
(6)A溶液与NaOH溶液混合可形成沉淀,某温度下此沉淀的Ksp=2.097×l0﹣39 . 将0.01mol/L的A溶液与0.001molL﹣1的NaOH溶液等体积混合,你认为能否形成沉淀(填“能”或“不能”),请通过计算说明 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两种不同的烃CxHy和CaHb不论以什么比例混合,只要总质量一定,完全燃烧时消耗O2的质量和生成水的质量不变,下列叙述正确的是( )
A.CxHy和CaHb分子中氢原子系数一定相等
B.可能是C2H4和C3H6的混合物
C.CxHy和CaHb一定是同分异构体
D.CxHy和CaHb的最简式可以不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢气是一种清洁能源,又是合成氨工业的重要原料.
(1)已知:CH4(g)+H2O(g)═CO(g)+3H2(g)△H=206.2kJmol﹣1CH4(g)+CO2(g)═2CO(g)+2H2(g)△H=247.4kJmol﹣1
甲烷和H2O(g)反应生成H2和CO2的热化学方程式为 .
(2)工业合成氨的反应原理为N2(g)+3H2(g)═2NH3(g)△H=﹣92.4kJmol﹣1 . 某温度下,把10mol N2与28mol H2置于容积为10L的密闭容器内,10min时反应达到平衡状态,测得氮气的平衡转化率为60%,则10min内该反应的平均速率v(H2)=molL﹣1min﹣1 , 则该温度下该反应的平衡常数K= . 欲增大氮气的平衡转化率,可采取的措施有(写一种措施即可).
(3)如图所示装置工作时均与H2有关. 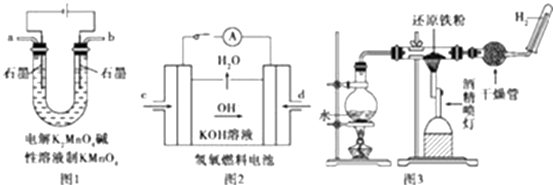
①图1所示装置中阳极的电极反应式为
②图2所示装置中,通入H2的管口是(选填字母代号).
③某同学按图3所示装置进行实验,实验结束后,将玻璃管内固体物质冷却后,溶于稀硫酸,充分反应后,滴加KSCN溶液,溶液不变红,再滴入新制氯水,溶液变为红色.该同学据此得出结论:铁与水蒸气反应生成FeO和H2 . 该结论(填“严密”或“不严密”),你的理由是(用离子方程式和必要的文字说明).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对氯苯甲酸是合成非甾族消炎镇痛药的中间体,还能用于燃料和浓药的合成,实验室中制备对氯苯甲酸的反应、装置图如图2: 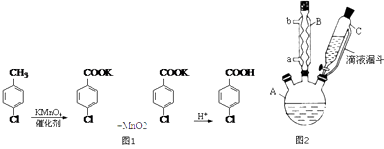
常温条件下的有关数据如表所示:
相对分子质量 | 熔点/℃ | 沸点/℃ | 密度/gcm﹣3 | 颜色 | 水溶性 | |
对氯甲苯 | 126.5 | 7.5 | 162 | 1.07 | 无色 | 难溶 |
对氯苯甲酸 | 156.5 | 243 | 275 | 1.54 | 白色 | 微溶 |
对氯苯甲酸钾 | 194.5 | 具有盐的通性,属于可溶性盐 | ||||
实验步骤:在规格为250mL的装置A中加入一定量的催化剂、适量KMnO4、100mL水;安装好装置,在滴液漏斗中加入6.00mL对氯甲苯,在温度为93℃左右时,逐滴滴入对氯甲苯;控制温度在93℃左右,反应2h,过滤,将滤渣用热水洗涤,使洗涤液与滤液合并,加入稀硫酸酸化,加热浓缩;然后过滤,将滤渣用冷水进行洗涤,干燥后称量其质量为7.19g.
请回答下列问题:
(1)装置B的名称是 .
(2)量取6.00mL对氯甲苯应选用的仪器是 . (填选仪器序号).
A.10mL量筒
B.50mL容量瓶
C.50mL酸式滴定管
D.50mL碱式滴定管
(3)控制温度为93℃左右的方法是 . 对氯甲苯的加入方法是逐滴加入而不是一次性加入,原因是 .
(4)第一次过滤的目的是 , 滤液中加入稀硫酸酸化,可观察到的实验现象是 .
(5)第二次过滤所得滤渣要用冷水进行洗涤,其原因是 .
(6)本实验的产率是(填标号).
A.60%
B.70%
C.80%
D.90%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,CO和CH4燃烧的热化学方程式分别为 2CO(g)+O2(g)═2CO2(g)△H=﹣566kJmol﹣1
CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=﹣890kJmol﹣1
由1mol CO(g)和3mol CH4(g)组成的混合气体在上述条件下充分燃烧,恢复至室温释放的热量为( )
A.2912kJ
B.2953kJ
C.3236kJ
D.3867kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X2是人体呼吸中不可缺少的气体.Y是地壳中含量最多的金属元素,Z元素的焰色为黄色,W2是一种黄绿色气体.请回答下列问题:
(1)写出Z元素符号 , 画出X的原子结构示意图;
(2)工业上利用W2和消石灰制取漂白粉,则漂白粉的有效成分是;
(3)Z元素组成的两种盐A、B在一定条件下可以互相转化,A、B都可与足量盐酸反应且产物完全一样,其中A是发酵粉的主要成分之一,则B通过化合反应转化为A的化学方程式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W,X,Y,Z均为原子序数依次增大的短周期主族元素,W,X,Y处于同一周期,W元素形成的化合物种类最多,W和Y族序数之和为X族序数的2倍,Z的最高价氧化物对应的水化物既能溶于酸又能溶于碱,下列说法中正确的是( )
A.简单气态氢化物沸点Y>X>W
B.原子半径Z>Y>X>W
C.Y元素可能位于第二周期第ⅦA族
D.Y元素与其它三种元素均可形成多种化合物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com