
【题目】如图表示各物质之间的转化关系.已知D、E、Z是中学化学常见的单质,其他都是化合物.Z、Y是氯碱工业的产品.D元素的原子最外层电子数与电子层数相等,且D的硫酸盐可作净水剂.E为日常生活中应用最广泛的金属.除反应①外,其他反应均在水溶液中进行.请回答下列问题.
(1)写出X的电子式: .
(2)常温时pH=12的G溶液中,溶质的阳离子与溶质的阴离子浓度之差为(写出计算式).
(3)在电镀工业中,若将E作为待镀金属,铜为镀层金属,则铜是极,请写出在E电极上发生的电极反应式: .
(4)写出反应③的离子方程式: .
(5)现有无标签的Y和M的两种无色水溶液,不用其他任何试剂,请你设计一个简单的实验对这两种溶液加以鉴别(回答实验操作、现象及结论).
(6)A溶液与NaOH溶液混合可形成沉淀,某温度下此沉淀的Ksp=2.097×l0﹣39 . 将0.01mol/L的A溶液与0.001molL﹣1的NaOH溶液等体积混合,你认为能否形成沉淀(填“能”或“不能”),请通过计算说明 .
【答案】
(1)![]()
(2)(10﹣2﹣10﹣12)mol/L
(3)阳;Cu2++2e﹣=Cu
(4)2Al+2OH﹣+2H2O=2AlO2﹣+3H2↑
(5)Y中滴加M,先没有沉淀后生成沉淀,而M中滴加Y,先生成沉淀后沉淀消失,则Y为NaOH,M为AlCl3
(6)能;Qc=( ![]() ×0.01)×(
×0.01)×( ![]() ×0.001)3=6.25×10﹣13>Ksp=2.097×l0﹣39 , 则生成沉淀
×0.001)3=6.25×10﹣13>Ksp=2.097×l0﹣39 , 则生成沉淀
【解析】解:图中D、E、Z是单质,其余均是化合物.且知E为日常常用金属;D元素的原子最外层电子数与电子层数相等,C+D=E+F是置换反应,推断高温下为铝热反应,推断D为Al,E为Fe,F为Al2O3;Z、Y是氯碱工业的产品,由图中Al、Al2O3和Y反应可推断,Y为NaOH;得到Z为Cl2 , X为HCl,反应均在水溶液中进行,所以推断得到G为NaAlO2 , M为AlCl3 , B为FeCl2 , A为FeCl3 , (1)X为HCl,其电子式为 ![]() , 所以答案是:
, 所以答案是: ![]() ;(2)pH=12的NaAlO2溶液中,水解显碱性,溶质的阳离子与溶质的阴离子浓度之差为0.01mol/L﹣10﹣12mol/L=(10﹣2﹣10﹣12)mol/L,
;(2)pH=12的NaAlO2溶液中,水解显碱性,溶质的阳离子与溶质的阴离子浓度之差为0.01mol/L﹣10﹣12mol/L=(10﹣2﹣10﹣12)mol/L,
所以答案是:(10﹣2﹣10﹣12)mol/L;(3)E作为待镀金属,铜为镀层金属,则铜为阳极失去电子,E为阴极,电极反应为Cu2++2e﹣=Cu,
所以答案是:阳;Cu2++2e﹣=Cu;(4)反应③中D为Al与Y为 NaOH的水溶液,反应生成偏铝酸钠和氢气,反应的离子方程式为2Al+2OH﹣+2H2O=2AlO2﹣+3H2↑,
所以答案是:2Al+2OH﹣+2H2O=2AlO2﹣+3H2↑;(5)Y中滴加M,先没有沉淀后生成沉淀,而M中滴加Y,先生成沉淀后沉淀消失,则试剂互滴现象不同,可以鉴别,
所以答案是:Y中滴加M,先没有沉淀后生成沉淀,而M中滴加Y,先生成沉淀后沉淀消失,则Y为NaOH,M为AlCl3;(6)0.01molL﹣1的FeCl3溶液与0.001molL﹣1的NaOH溶液等体积混合,Qc=( ![]() ×0.01)×(
×0.01)×( ![]() ×0.001)3=6.25×10﹣13>Ksp=2.097×l0﹣39 , 则生成沉淀,
×0.001)3=6.25×10﹣13>Ksp=2.097×l0﹣39 , 则生成沉淀,
所以答案是:能;Qc=( ![]() ×0.01)×(
×0.01)×( ![]() ×0.001)3=6.25×10﹣13>Ksp=2.097×l0﹣39 , 则生成沉淀.
×0.001)3=6.25×10﹣13>Ksp=2.097×l0﹣39 , 则生成沉淀.


科目:高中化学 来源: 题型:
【题目】某小组利用以下装置制取并探究氨气的性质.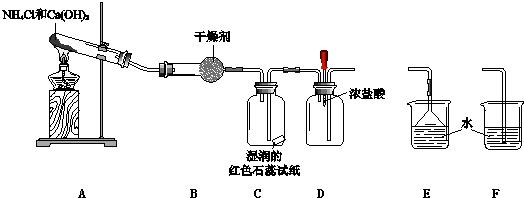
(1)A中反应的化学方程式是 .
(2)B中的干燥剂是 .
(3)C中的现象是 .
(4)实验进行一段时间后,挤压D装置中的胶头滴管,滴入1﹣2滴浓盐酸,可观察到的现象是 .
(5)为防止过量氨气外逸,需要在上述装置的末端增加一个尾气处理装置,应选用的装置是(填“E”或“F”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A. 分子式为C4H8有机物最多存在4个C﹣C单键
B. ![]() 和
和![]() 均是芳香烃,
均是芳香烃,![]() 既是芳香烃又是芳香化合物
既是芳香烃又是芳香化合物
C. ![]() 和
和![]() 分子组成相差一个﹣CH2﹣,因此是同系物关系
分子组成相差一个﹣CH2﹣,因此是同系物关系
D. 分子式为C2H6O的红外光谱图上发现有C﹣H键和C﹣O键的振动吸收,由此可以初步推测有机物结构简式为C2H5﹣OH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列离子方程式中,不能用离子反应方程式 SO42-+Ba2+=BaSO4↓来表示的
A. Ba(NO3)2+H2SO4=BaSO4↓+2HNO3 B. BaCl2 + Na 2SO4=BaSO4↓+ 2NaCl
C. Ba(OH)2+H2SO4=BaSO4↓+2H2O D. BaCl2 +H2SO4=BaSO4↓+2HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在碱性溶液中能大量共存,且溶液为无色透明的是
A. K+、Na+、MnO4-、SO42- B. NH4+、Mg2+、NO3-、SO42-
C. Na+、K+、Cl-、CO32- D. Fe3+、Cu2+、Cl-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列与有机物的结构、性质有关的叙述正确的是
A.苯、油脂均不能使酸性KMnO4溶液褪色
B.聚酯纤维、有机玻璃、光导纤维都属于有机高分子材料
C.乙醇可以被氧化为乙酸,二者都能发生取代反应
D.淀粉和蛋白质均可作为生产葡萄糖的原料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式正确的是( )
A.稀硫酸与氢氧化钡溶液混合:Ba2++SO ![]() +OH﹣+H+═H2O+BaSO4↓
+OH﹣+H+═H2O+BaSO4↓
B.Cl2通入水中:Cl2+H2O═H++Cl﹣+HClO
C.将钠加入硫酸铜溶液中的反应:2Na+2Cu2+═2Na++Cu
D.铜片投入稀硫酸中:Cu+2H+═Cu2++H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】小明同学设计了如图所示装置探究铜跟浓硫酸的反应.先关闭活塞a,加热至烧瓶中不再有气泡产生时,反应停止,此时烧瓶中铜片仍有剩余.接着再打开活塞a,将气球中的氧气缓缓挤入烧瓶,铜片慢慢减少.请回答下列问题:
(1)请写出上述过程A装置中所涉及的任意一个化学反应方程式;
(2)张老师认为整个装置设计有一点错误,你认为(填“A”、“B”或“C”)部分有错误.
(3)B中所收集到的气体既具有氧化性又具有还原性,请写出一个体现其还原性的化学方程式 .
(4)装置C中所选用的溶液试剂一般是(填化学式).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com