
【题目】某小组利用以下装置制取并探究氨气的性质.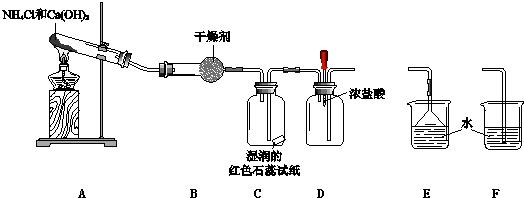
(1)A中反应的化学方程式是 .
(2)B中的干燥剂是 .
(3)C中的现象是 .
(4)实验进行一段时间后,挤压D装置中的胶头滴管,滴入1﹣2滴浓盐酸,可观察到的现象是 .
(5)为防止过量氨气外逸,需要在上述装置的末端增加一个尾气处理装置,应选用的装置是(填“E”或“F”).
【答案】
(1)2NH4Cl+Ca(OH)2 ![]() CaCl2+2NH3↑+2H2O
CaCl2+2NH3↑+2H2O
(2)碱石灰
(3)试纸蓝色
(4)有白烟生成
(5)E
【解析】解:(1)加热氯化铵与氢氧化钙生成氯化钙、氨气和水,方程式;2NH4Cl+Ca(OH)2 ![]() CaCl2+2NH3↑+2H2O;故答案为;2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O;故答案为;2NH4Cl+Ca(OH)2 ![]() CaCl2+2NH3↑+2H2O;(2)氨气为碱性气体,应选择碱性干燥剂碱石灰干燥;故答案为:碱石灰;(3)氨气与水反应生成一水合氨,一水合氨电离生成氢氧根离子,溶液显碱性,遇到石蕊能够使石蕊变蓝,故答案为:试纸蓝色;(4)氨气与挥发的HCl会生成氯化铵晶体,所以有白烟生产,反应方程式为NH3+HCl═NH4Cl,故答案为:有白烟生成;(5)因为氨气极易溶于水,所以吸收氨气时要用防倒吸装置,故选E;故答案为:E. 实验室用加热氯化铵与氢氧化钙制备氨气,氨气为碱性气体,应选择碱性干燥剂,氨气与水反应生成一水合氨,一水合氨电离生成氢氧根离子,溶液显碱性,遇到石蕊能够使石蕊变蓝,氨气与氯化氢反应生成白色氯化铵固体,为防止氨气污染环境,应进行尾气处理,依据氨气极易溶于水的性质选择尾气处理装置.
CaCl2+2NH3↑+2H2O;(2)氨气为碱性气体,应选择碱性干燥剂碱石灰干燥;故答案为:碱石灰;(3)氨气与水反应生成一水合氨,一水合氨电离生成氢氧根离子,溶液显碱性,遇到石蕊能够使石蕊变蓝,故答案为:试纸蓝色;(4)氨气与挥发的HCl会生成氯化铵晶体,所以有白烟生产,反应方程式为NH3+HCl═NH4Cl,故答案为:有白烟生成;(5)因为氨气极易溶于水,所以吸收氨气时要用防倒吸装置,故选E;故答案为:E. 实验室用加热氯化铵与氢氧化钙制备氨气,氨气为碱性气体,应选择碱性干燥剂,氨气与水反应生成一水合氨,一水合氨电离生成氢氧根离子,溶液显碱性,遇到石蕊能够使石蕊变蓝,氨气与氯化氢反应生成白色氯化铵固体,为防止氨气污染环境,应进行尾气处理,依据氨气极易溶于水的性质选择尾气处理装置.


科目:高中化学 来源: 题型:
【题目】下列几种均属烃的含氧衍生物,请按要求作答:
(1)﹣定条件下①可转化为④,下列试剂中能实现该转化的是(填字母).
A.高锰酸钾溶液
B.H2
C.银氨溶液/H+
D.氢氧化钠溶液
(2)请写出满足下列条件的①的同分异构体 .
A.分子中除苯环外不含其它环状结构
B.苯环上一氯代物有三种
C.能与溴水中的Br2按1:4进行反应
(3)官能团是决定化合物特殊性质的原子或原子团,而有机物分子中基团间的相互影响也会导致物质性质的变化,依据此种观点回答以下问题:
①②③三种有机物溶解性由大到小的顺序(填字母),它们互为;
丙三醇、丙烷、乙二醇的沸点由高到低的顺序 .
醋酸、苯酚、苯甲酸的酸性由强到弱的顺序 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CuCl广泛应用于化工和印染等行业.某研究性学习小组拟热分解CuCl22H2O制备CuCl,并进行相关探究.
【资料查阅】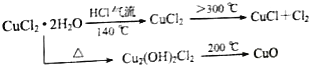
【实验探究】
该小组用如图所示装置进行实验(夹持仪器略).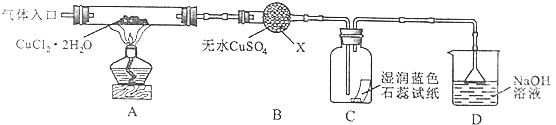
请回答下列问题:
(1)仪器X的名称是 .
(2)实验操作的先后顺序是a→→e(填操作的编号)
a.检查装置的气密性后加入药品
b.熄灭酒精灯,冷却
c.在“气体入口”处通入干燥HCl
d.点燃酒精灯,加热
e.停止通入HCl,然后通入N2
(3)在实验过程中,观察到B中物质由白色变为蓝色,C中试纸的颜色变化是 .
(4)装置D中发生的氧化还原反应的离子方程式是 .
(5)【探究反思】反应结束后,取出CuCl产品进行实验,发现其中含有少量的CuCl2或CuO杂质,根据资料信息分析:
①若杂质是CuCl2 , 则产生的原因是 .
②若杂质是CuO,则产生的原因是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关少量食用油在低温下出现冻结现象后能否食用及解释合理的是
A. 不能,因为已经变质
B. 不能,因为含有杂质
C. 不能,因为含有水份
D. 能,因为那只是油脂主要成份在低温下结晶析出,是正常物理形态变化,并未变质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属元素在自然界中分布很广,其中铜等在生产生活中有着广泛的应用.
(1)科学家通过X射线推测胆矾结构示意图如图1所示,①写出基态Cu原子的核外电子排布式;金属铜采用下列(填字母代号)堆积方式
②胆矾中含有的微粒间作用力有(填字母代号).
a.离子键 b.极性键 c.金属键 d.配位键 e.氢键 f.非极性键
③铜离子形成胆矾中配离子的离子方程式为:;
(2)合成氨工业中,原料气(N2、H2及少量CO、NH3的混合气)在进入合成塔前常用醋酸二氨合铜(I)溶液来吸收原料气体中的CO(Ac﹣表示CH3COO﹣),其反应是:[Cu(NH3)2]Ac+CO+NH3[Cu(NH3)3]Ac.CO[醋酸碳基三氨合铜(Ⅰ)]△H<0①C、N、O三种元素的第一电离能由小到大的顺序为
②氨分子中N原子的杂化方式为
(3)铜的化合物种类也很多,其常见价台为+1,+2价.如CuO、Cu2O、CuH等,如图2是同的一种氯化铜的晶胞结构,则它的化学式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,有浓度均为1 mol·L-1的下列4种溶液:
①H2SO4溶液②NaHCO3溶液③NH4Cl溶液④NaOH溶液
(1)这4种溶液pH由大到小的顺序是 ,其中由水电离的H+浓度最小的是 。(均填序号)
(2)②中各离子浓度由大到小的顺序是 ,NaHCO3的水解平衡常数Kh= mol·L-1。(已知碳酸的电离常数K1=4×10-7,K2=5.6×10-11)
(3)向③中通入少量氨气,此时![]() 的值 (填“增大”、“减小”或“不变”)。
的值 (填“增大”、“减小”或“不变”)。
(4)若将③和④混合后溶液恰好呈中性,则混合前③的体积 ④的体积(填“大于”、“小于”或“等于”之一)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示各物质之间的转化关系.已知D、E、Z是中学化学常见的单质,其他都是化合物.Z、Y是氯碱工业的产品.D元素的原子最外层电子数与电子层数相等,且D的硫酸盐可作净水剂.E为日常生活中应用最广泛的金属.除反应①外,其他反应均在水溶液中进行.请回答下列问题.
(1)写出X的电子式: .
(2)常温时pH=12的G溶液中,溶质的阳离子与溶质的阴离子浓度之差为(写出计算式).
(3)在电镀工业中,若将E作为待镀金属,铜为镀层金属,则铜是极,请写出在E电极上发生的电极反应式: .
(4)写出反应③的离子方程式: .
(5)现有无标签的Y和M的两种无色水溶液,不用其他任何试剂,请你设计一个简单的实验对这两种溶液加以鉴别(回答实验操作、现象及结论).
(6)A溶液与NaOH溶液混合可形成沉淀,某温度下此沉淀的Ksp=2.097×l0﹣39 . 将0.01mol/L的A溶液与0.001molL﹣1的NaOH溶液等体积混合,你认为能否形成沉淀(填“能”或“不能”),请通过计算说明 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com