
A、 反应过程中能量关系可用右图表示 |
| B、1mol锌的能量高于1molH2所含的能量 |
| C、若将该反应设计成原电池,则锌为正极 |
| D、若将其设计为原电池,则当有32.5g锌溶解时,正极放出的气体体积一定为22.4L(标况) |


科目:高中化学 来源: 题型:
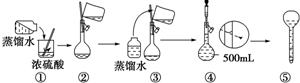
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、V=224 |
| B、样品中Fe的质量为2.14g |
| C、样品中CuO的质量为3.52g |
| D、未氧化前Fe元素的质量分数约为41.2% |
查看答案和解析>>
科目:高中化学 来源: 题型:
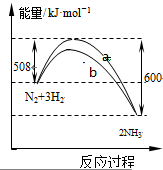
| A、加入催化剂可增大正反应速率,降低逆反应速率 |
| B、正反应的活化能大于逆反应的活化能 |
| C、b曲线是未加入催化剂时的能量变化曲线 |
| D、该反应的热化学方程式为:2NH3?N2+3H2△H=-92 kJ?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氧化还原反应中有一种元素被氧化时,一定有另一种元素被还原 |
| B、含有最低价元素的化合物不一定具有很强的还原性 |
| C、阳离子只能得电子被还原,阴离子只能失电子被氧化 |
| D、在化学反应中,得电子越多的氧化剂,其氧化性就越强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将固体加入容量瓶中溶解并稀释至刻度,配制成一定物质的量浓度的溶液 |
| B、用玻璃棒蘸取溶液,点在湿润的pH试纸上测定其pH |
| C、洗净的锥形瓶和滴定管可以放进烘箱中烘干 |
| D、氢氟酸试剂和NaOH溶液不可用带玻璃塞的玻璃瓶存放 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、一定含有Fe2+、Fe3+、Cu2+、Cl- |
| B、c(Cl-)=3.0 mol?L-1 |
| C、c(Fe2+):c(Cu2+)=1:1 |
| D、c(Fe2+):c(Fe3+)=3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
A、
| ||||||||||||||
B、春蚕到死丝方尽,
| ||||||||||||||
C、宝剑
| ||||||||||||||
D、莫道雪融便无迹,
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com