
【题目】下列物质属于纯净物的是
A.冰水混合物B.矿泉水C.盐酸D.钢
科目:高中化学 来源: 题型:
【题目】下列水解化学方程式或水解离子方程式正确的是: ( )
A.CH3COO- + H2O ![]() CH3COOH + OH-
CH3COOH + OH-
B.NH4+ + H2O=NH4OH + H+
C.CH3COOH + NaOH ![]() CH3COONa + H2O
CH3COONa + H2O
D.NaCl + H2O ![]() NaOH + HCl
NaOH + HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用质量相同的铁单质与下列条件下相同体积的硫酸反应时,生成氢气速率最快的是( )
A.20℃铁片 1mol/L硫酸
B.30℃铁粉 1mol/L硫酸
C.30℃铁粉 2mol/L硫酸
D.30℃铁片 18mol/L硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于实验安全说法正确的是( )
A.少量浓硫酸沾在皮肤上,立即用氢氧化钠溶液冲洗
B.蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶支管口处
C.实验室可用燃着的酒精灯去点燃另一只酒精灯
D.将含硫酸的废液倒入水槽,用水冲入下水道
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】莫尔盐[(NH4)2Fe(SO4)2·6H2O](浅绿色)常用作化学试剂、医药以及用于冶金、电镀等。某课题组通过实验来探究莫尔盐晶体加热时的分解产物,回答下列问题:
(1)甲同学提出猜想;分解产物可能是N2、Fe2O3、SO3、H2O四种物质。你是否同意并说明理由___________________________。
(2)乙同学设计了如图装置:
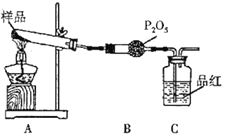
①其中A装置中的固体变为红棕色,则固体产物中含有_________________;C装置中红色褪去,说明气体产物中含有_______________________。
②为验证A中残留物是否含有FeO,需要选的试剂有__________。
A.KSCN溶液 B.浓盐酸 C.KMnO4溶液 D.稀硫酸
(3)丙同学想利用乙同学的装置证明分解产物中含有氨气,只需更换B、C 中的试剂即可,则更换后的试剂B为______________,C为________________。
(4)丁同学认为莫尔盐晶体分解的气体产物中含有SO3(g)、SO2(g)及N2。为了进行验证,丁同学选用乙同学的A装置和下图装置组装后进行实验。
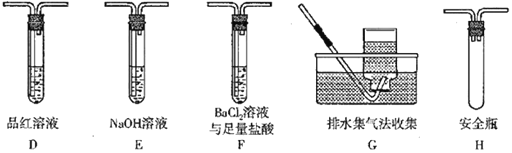
①丁同学的实验中,装置依次连接的合理顺序为A、________。
②装置F中,足量盐酸的作用是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2017年4月26日,海军成立68周年时,我国第一艘国产航母成功下水。建造航母需要大量的新型材料。航母的龙骨要耐冲击,航母的甲板要耐高温,航母的外壳要耐腐蚀。
(1)镍铬钢抗腐蚀性能强,Ni2+最高能级电子的运动状态有_________种,铬元素在周期表中_____区。
(2)航母甲板涂有一层耐高温的材料聚硅氧烷(结构如下图所示),其中C原子杂化方式为__________杂化。
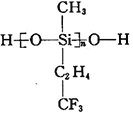
(3)海洋是元素的摇篮,海水中含有大量卤族元素。
①根据下表数据判断:最有可能生成较稳定的单核阳离子的卤素原子是__________(填元素符号)
氟 | 氯 | 溴 | 碘 | |
第一电离能(kJ/mol) | 1681 | 1251 | 1140 | 1008 |
②根据价层电子对互斥理论,预测ClO3-的空间构型为__________形,写出一个C1O3-的等电子体的化学符号__________________。
③已知高碘酸有两种形式,化学式分别为H5IO6(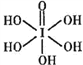 )和HIO4,前者为五元酸,后者为一元酸。请比较二者酸性强弱:H5IO6_________HIO4(填“>”“<”或“= ”)
)和HIO4,前者为五元酸,后者为一元酸。请比较二者酸性强弱:H5IO6_________HIO4(填“>”“<”或“= ”)
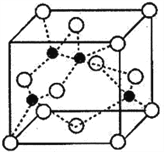
(4)海底金属软泥是在洋海底覆盖着的一层红棕色沉积物,蕴藏着大量的资源,含有硅、氧化铁、锰、锌等。Zn2+与S2-形成的一种晶体结构如图所示(黑球表示Zn2+,白球表示S2-)。则该晶体中与Zn2+等距且最近的S2-形成的立体图形为______________________。已知该晶体的密度为ρg·cm-3,阿伏伽德罗常数为NA,该晶体中Zn2+和S2-原子之间的最短距离为体对角线的1/4,则该晶体中S2-和Zn2+之间的最短距离为__________________pm。(写出计算式即可)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
(1)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是 ______。
A.C(s)+H2O(g)═CO(g)+H2(g)△H>0
B.NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H<0
C.2H2(g)+O2(g)═2H2O(l)△H<0
(2)以KOH溶液为电解质溶液,依据所选反应设计一个原电池,其负极的电极反应式为 。
(3)电解原理在化学工业中有着广泛的应用.现将你设计的原电池通过导线与图中电解池相连,其中a为电解液,X和Y均为惰性电极,则: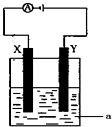
①若a为CuSO4溶液,则电解时的化学反应方程式为 .通电一段时间后,向所得溶液中加入0.2molCuO粉末,恰好恢复电解前的浓度和pH,则电解过程中转移的电子的物质的量为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知 Fe2O3(s)+3CO(g)2Fe(s)+3CO2(g) 在不同温度下的平衡常数如表:
温度/℃ | 1000 | 1150 | 1300 |
平衡常数 | 42.9 | 50.7 | 64.0 |
请回答下列问题:
(1)该反应的平衡常数表达式 K= ,△H 0(填“>”、“<”或“=”)。
(2)在一个容积为10L的密闭容器中,1300℃时加入 Fe、Fe2O3、CO、CO2各1mol , 反应经过10min 后达到平衡.求该时间范围内反应的平均反应速率 v(CO2)= ,CO 的平衡转化率为 。
(3)欲提高(2)中CO的平衡转化率,可采取的措施是 ______。
A.增加Fe2O3的量
B.加入合适的催化剂
C.移出部分CO2
D.提高反应温度.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在体积为2L的密闭容器中发生2SO2+O22SO3反应,现控制下列三种不同的条件:①在400℃时,10molSO2与5molO2反应;
②在400℃时,20molSO2与5molO2反应;
③在300℃时,10molSO2与5molO2反应;
(1)开始时,化学反应速率快慢顺序是;
(2)若10min内测得第①组的平均反应速率为:V(SO2)=0.4mol/(Lmin),则V(O2)= , 10min时,SO3浓度为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com