
【题目】在体积为2L的密闭容器中发生2SO2+O22SO3反应,现控制下列三种不同的条件:①在400℃时,10molSO2与5molO2反应;
②在400℃时,20molSO2与5molO2反应;
③在300℃时,10molSO2与5molO2反应;
(1)开始时,化学反应速率快慢顺序是;
(2)若10min内测得第①组的平均反应速率为:V(SO2)=0.4mol/(Lmin),则V(O2)= , 10min时,SO3浓度为 .
【答案】
(1)②>①>③
(2)0.2mol/(L?min),4mol/L
【解析】解:(1)③的温度最低,反应速率最慢,①②比较,②中浓度大,则反应速率最大,
所以答案是:②>①>③;
所以答案是:②>①>③;
(2)反应速率之比等于化学计算数之比,V(O2)= ![]() V(SO2)=
V(SO2)= ![]() ×0.4mol/(Lmin)=0.2mol/(Lmin);V(SO3)=V(SO2)=0.4mol/(Lmin),则10min时,生成的SO3浓度为0.4mol/(Lmin)×10min=4mol/L;
×0.4mol/(Lmin)=0.2mol/(Lmin);V(SO3)=V(SO2)=0.4mol/(Lmin),则10min时,生成的SO3浓度为0.4mol/(Lmin)×10min=4mol/L;
所以答案是:0.2mol/(Lmin);4mol/L.
【考点精析】利用化学平衡的计算对题目进行判断即可得到答案,需要熟知反应物转化率=转化浓度÷起始浓度×100%=转化物质的量÷起始物质的量×100%;产品的产率=实际生成产物的物质的量÷理论上可得到产物的物质的量×100%.


 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源: 题型:
【题目】中国第二化工设计院提出,用间接电化学法对大气污染物NO进行无害化处理,其原理示意如图(质子膜允许H+和H2O通过),下列相关判断正确的是( )
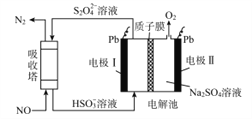
A. 吸收塔中的反应为2NO+2S2O32-+H2O=N2+4HSO3-
B. 电解池中质子从电极I向电极Ⅱ作定向移动
C. 电极I为阴极,电极反应式为2H2O+2e-=2OH-+H2
D. 每处理1 mol NO电解池质量减少16g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属(M)-空气电池的工作原理如图所示,下列说法不正确的是( )
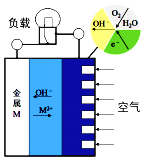
A. 金属M作电池负极
B. M2+移向金属(M)电极
C. 正极的电极反应为O2+4e-+2H2O=4OH-
D. 电池反应为2M+O2+2H2O=2M(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮的固定对工农业及人类生存具有重大意义。
Ⅰ.合成氨是最重要的人工固氮:N2(g)+3H2(g)![]() 2NH3(g)。
2NH3(g)。
(1)下列关于该反应的说法中,正确的是 。
A.△H>0,△S>0 B.△H>0,△S<0
C.△H<0,△S>0 D.△H<0,△S<0
(2) —定温度下,在容积为1L的密闭容器中,加入ImolN2和3molH2,反应达到平衡时H2的转化率为60%,则此条件下反应的平衡常数K= (此处不要求写单位);保持容器体积不变,再向容器中加入lmolN2,3molH2反应达到平衡时,氢气的转化率将 (填“增大”、“减小”或“不变”)
(3)标准状况下,若将22.4mL的氨气通入100mLpH为2的盐酸中.则溶液中各离子浓度的顺序由大到小为 。
(4)将氨气通入盛有CaSO4悬浊液的沉淀池中,再通入适量的CO2气体,充分反应后,过滤所得滤液为(NH4)2SO4溶液,该过程的化学方程式为 。
II.随着研究的不断深入,科学家发明了越來越多有关氮的固定方法。
(5)20世纪末,科学家采用高质子导电性的SCY陶瓷(能传递H+)为介质,用吸附在它内外表面上的金属钯多晶薄膜做电极,实现常压、570℃高温的电解法合成氨,提高了反应物的转化率,其实验简图如下,阴极的电极反应式为 。

(6)近年,又有科学家提出在常温、常压、催化剂等条件下合成氨气的新思路,反应原理为:
2N2(g)+6H2O(I) ![]() 4NH3(g)+3O2(g),则其反应热△H= 。(已知:N2(g)+3H2(g)
4NH3(g)+3O2(g),则其反应热△H= 。(已知:N2(g)+3H2(g) ![]() 2NH3(g) △H=-92.4kJ·mol-1;2H2(g)+O2(g)
2NH3(g) △H=-92.4kJ·mol-1;2H2(g)+O2(g) ![]() 2H2O(I) △H=-571.6kJ·mol-1)
2H2O(I) △H=-571.6kJ·mol-1)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2SO2(g)+O2(g)2SO3(g)△H=a kJmol﹣1 , 反应过程的能量变化如图所示.已知1mol SO2(g)完全转化为1mol SO3(g)放热99kJ.请回答: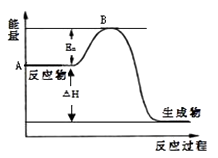
(1)图中A点表示 , a= .
(2)Ea的大小对该反应的△H(填“有”或“无”)影响.
(3)已知常温常压下单质硫的燃烧热为296kJmol﹣1 , 由单质硫和氧气经两步反应,生成3mol SO3(g),放出的总热量为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质,按化合物、单质、混合物顺序排列的是( )
A.烧碱、液态氧、碘酒
B.生石灰、白磷、熟石灰
C.干冰、铁、氯化氢
D.空气、氮气、胆矾
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以熔融Li2CO3和K2CO3为电解质,天然气经重整催化作用提供反应气的燃料电池如右图。下列说法正确的是
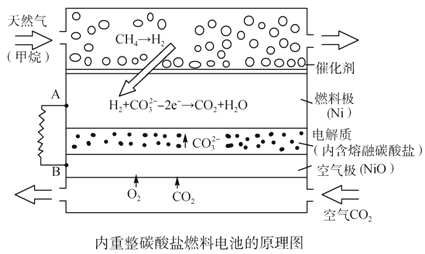
A. 以此电池为电源电解精炼铜,当有0.1 mol e- 转移时,有3.2 g铜溶解
B. 若以甲烷为燃料气时负极电极反应式:CH4+5O2--8e-=CO32-+2H2O
C. 该电池使用过程中需补充Li2CO3和K2CO3
D. 空气极发生的电极反应式为O2+4e-+2CO2===2CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由乙醇制取环乙二酸乙二酯时,最简便的流程需要下列哪些反应,其正确的顺序是:①取代;②加成;③氧化;④还原;⑤消去;⑥酯化;⑦中和
A. ①②③⑤⑦ B. ⑤②①③⑥ C. ⑤②①④⑦ D. ①②⑤③⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com