
【题目】将NO2装入带有活塞的密闭容器中,当反应2NO2(g)![]() N2O4(g)达到平衡后,改变下列一个条件,其中叙述正确的是
N2O4(g)达到平衡后,改变下列一个条件,其中叙述正确的是
A.升高温度,气体颜色加深,则此反应为吸热反应
B.慢慢压缩气体体积,平衡向正反应方向移动,混合气体颜色变浅
C.慢慢压缩气体体积,若体积减小一半,压强增大,但小于原来的两倍
D.恒温恒容时,充入惰性气体,压强增大,平衡向正反应方向移动,混合气体的颜色变浅
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】将ag Fe2O3和Al2O3的混合物溶解在过量的200 ml 浓度为0.1 mol/L 的盐酸溶液中,然后向其中加入NaOH溶液,使Fe3+ 、Al3+ 刚好完全沉淀,用去NaOH溶液100ml ,则NaOH溶液的浓度为 ( )
A. 0.1mol/L B. 0.2mol/L C. 0.4mol/L D. 0.8mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:常温下,0.01mol/LMOH溶液的pH为10,MOH(aq)与H2SO4(aq) 反应生成1 mol正盐的ΔH=-24.2 kJ·mol-1,强酸与强碱的稀溶液的中和热为ΔH=-57.3 kJ·mol-1。则MOH在水溶液中电离的ΔH为
A.-69.4 kJ·mol-1 B.-45.2 kJ·mol-1
C.+69.4 kJ·mol-1 D.+45.2 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在1L定容的密闭容器中,可以证明可逆反应N2+3H2![]() 2NH3已达到平衡状态的是
2NH3已达到平衡状态的是
A.c(N2):c(H2):c(NH3)=1:3:2
B.一个N≡N 断裂的同时,有3个H-H生成
C.其他条件不变时,混合气体的密度不再改变
D.v正(N2)═2 v逆(NH3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以Al2O3为原料制取氢氧化铝,最好的方法是( )
A.将Al2O3溶于水
B.将Al2O3先溶于盐酸中,之后滴加氢氧化钠溶液
C.将Al2O3先溶于盐酸中,之后滴加氨水
D.将Al2O3先溶于NaOH溶液中,之后滴加盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中不正确的是( )
A.Fe在少量Cl2中燃烧生成FeCl2 , 在足量Cl2中燃烧生成FeCl3
B.在空气中用小火慢慢加热蒸干硫酸亚铁溶液,不会得到纯净的硫酸亚铁固体
C.鉴别Fe2+和Fe3+ , 可以使用酸性KMnO4溶液,也可使用KI淀粉溶液
D.Fe3+有氧化性,所以可以用FeCl3溶液来回收旧电路板中的铜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各基态原子或离子的电子排布式正确的是
A. O2-1s22s22p4 B. Ca [Ar]3d2
C. Fe [Ar]3d54s3 D. Si 1s22s22p63s23p2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是
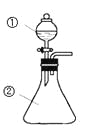
选项 | ①中物质 | ②中物质 | 预测②中的现象 |
A | 稀盐酸 | 碳酸钠与氢氧化钠的混合溶液 | 立即产生气泡 |
B | 浓硝酸 | 用砂纸打磨过的铝条 | 产生红棕色气体 |
C | 氯化铝溶液 | 浓氢氧化钠溶液 | 产生大量白色沉淀 |
D | 草酸溶液 | 酸性高锰酸钾溶液 | 溶液逐渐褪色 |
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com