
【题目】锌与稀硝酸反应生成Zn(NO3)2、NH4NO3和水.当生成1mol Zn(NO3)2时,消耗的硝酸的物质的量为( )
A.2mol
B.1mol
C.2.25 mol
D.2.5 mol
 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源: 题型:
【题目】下列各组物质,按化合物、单质、混合物的顺序排列的是( )
A.干冰、铁、氯化氢
B.生石灰、白磷、熟石灰
C.烧碱、液态氧、碘酒
D.空气、氮气、胆矾
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环境污染问题越来越受到人们的关注,造成环境污染的主要原因大多是由于人类生产活动中过度排放有关物质引起的.下列环境问题与所对应的物质不相关的是( )
A.温室效应﹣﹣CO2
B.光化学污染﹣﹣NO2
C.酸雨﹣﹣SO2
D.臭氧层破坏﹣﹣CO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某新型无机材料A3M4由两种非金属元素组成,元素M位于第二周期VA族。D、E、H均为难溶于水的白色固体:化合物C、E均含A元素。其余物质均为中学化学中常见物质。
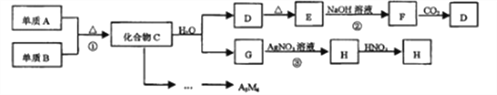
请回答:
(1)写出H的化学式:________________。
(2)化合物A3M4中含有的化学键类型为:________________。
(3)写出反应②的离子方程式:________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列为四个常用的电化学装置,关于它们的叙述正确的是( )

A. 图(a)所示电池中,MnO2的作用是催化剂
B. 图(b)所示电池放电过程中,硫酸浓度不断增大
C. 图(c)所示装置工作过程中,电解质溶液中Cu2+浓度始终不变
D. 图(d)所示电池中,Ag2O是氧化剂,电池工作过程中还原为Ag
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳、硅两元素广泛存在于自然界中.请回答下列问题:
(1)基态14C原子的核外存在________对自旋方向相反的电子,硅原子的电子排布式为__________。
(2)晶体硅的结构与全刚石非常相似。晶体硅硅中硅原子的杂化方式为_______杂化;金刚石、晶体硅和金刚砂(碳化硅)的熔点由高到低的顺序为_____________。
(3)科学研究结果表明,碳的氧化物CO2能够与H2O借助子太阳能制备HCOOH。其反应原理如下:2CO2+2H2O=2HCOOH+O2,则生成的HCOOH分子中δ键和π键的个数比是_______。
(4)碳单质有多种形式,其中C60、石墨烯与金刚石晶体结构如图所示:

①C60、石墨烯与金刚石互为_________。
②C60形成的晶体是分子晶体,C60分子中含有12个五边形和20个六边形,碳与碳之间既有单键又有双键,已知C60分子所含的双键数为30,则C60分子中_______个C—C 键(多面体的顶点数、面数和棱边数的关系,遵循欧拉定理:顶点数+面数-棱边数=2)。在石墨烯晶体中,每个C原子连接______个六元环;在金刚石晶体中,每个C原子连接的最小环也为六元环,六元环屮最多有_______个C原子在同一平面。
③金刚石晶胞含有______个碳原子。若碳原子的半径为r,金刚石晶胞的边长为a,根据硬球接触模型,则r=______a,列式表示碳原子在晶胞中的空间占有率为_______(不要求计算结果)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳、氮、氧、铝都为重要的短周期元素,其单质及化合物在工农业生产生活中有重要作用。请回答下列问题:
(1)在密闭容器内(反应过程保持体积不变),使1molN2和3molH2混合发生下列反应:N2(g)+3H2(g)![]() 2NH3(g) △H=-92.4kJ/mol。当反应达到平衡时,N2和H2的浓度之比是_______;当升高平衡体系的温度,则混合气体的平均式量______(将“增大”“减小”或“不变”);当达到平衡时,再向容器内充入1mol N2,H2的转化率_______(填“提高”“降低”或“不变”);当达到平衡时,将c(N2)、c(H2)、c(NH3)同时增大1倍,平衡_______移动(填“正向”“逆向”或“不”)。
2NH3(g) △H=-92.4kJ/mol。当反应达到平衡时,N2和H2的浓度之比是_______;当升高平衡体系的温度,则混合气体的平均式量______(将“增大”“减小”或“不变”);当达到平衡时,再向容器内充入1mol N2,H2的转化率_______(填“提高”“降低”或“不变”);当达到平衡时,将c(N2)、c(H2)、c(NH3)同时增大1倍,平衡_______移动(填“正向”“逆向”或“不”)。
(2)由题干所述元素中的三种组成的某种强酸弱碱盐的化学式为________,其溶于水能_____水的电离(填“促进”或“抑制”),且使溶液的pH_______(填“升高”“降低”或“不变”),原因是_________(用离子方程式表示)。
(3)空气是硝酸工业生产的重要原料,氨催化氧化是硝酸工业的基础,氨气在铁触媒作用下只发生主反应①和副反应②:
4NH3(g)+5O2![]() 4NO+6H2O(g) △H=-905kJ/mol ①
4NO+6H2O(g) △H=-905kJ/mol ①
4NH3(g)+3O2![]() 2N2+6H2O(g) △H=-1268kJ/mol ②
2N2+6H2O(g) △H=-1268kJ/mol ②
①氮气与氧气反应生成NO的热化学方程式为______________________。
②在氧化炉中催化氧化时,有关物质的产率与温度的关系如图。下列说法中正确的是_____。

A.工业上氨催化氧化生成NO时,最佳温度应控制在780~840℃之间
B.工业上采用物料比![]() 在1.7~2.0,主要是为了提高反应速率
在1.7~2.0,主要是为了提高反应速率
C.加压可提高NH3生成NO的转化率
D.由图可知,温度高于900℃时,生成N2的副反应增多,故NO产率降低
(4)M是重要的有机化工原料,其分子与H2O2含有相同的电子数,将1molM在氧气中完全燃烧,只生成1molCO2和2molH2O,则M的化学式为_______。某种燃料电池采用铂作为电极催化剂,以KOH溶液为电解质,以M为燃料,以空气为氧化剂。若该电池工作时消耗1molM,则电路中通过_____mol电子。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是元素周期表的一部分。

I.用化学用语回答下列问题:
(1)②、⑥、⑧的离子半径由大到小的顺序为_________(用离子符号表示)。
(2)④、⑦、⑧的最高价含氧酸的酸性由强到弱的顺序是_______。(用化学式表示)
(3)As的原子结构示意图为_______;其氢化物的化学式为_______。
(4)Y由②⑥⑧三种元素组成,它的水溶液是生活中常见的消毒剂。As可与Y的水溶液反应,产物有As的最高价含氧酸,该反应的化学方程式为_________,当消耗1mol还原剂时,电子转移了______mol。
Ⅱ.A、B、C、D、E、X是上述周期表给出元素组成的常见单质或化合物。已知A、B、C、D、E、X存在如图所示转化关系(部分生成物和反应条件略去),若常温下A为红棕色气体,B为强酸,X为常见金属单质。

(5)A与水反应的化学方程式为_______________。
(6)工业上常用热还原法冶炼X,写出其化学方程式___________。
(7)某温度下(>100℃)若m克X与H2O反应放出QkJ(Q>0)的热量。写出该反应的热化学方程式_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com