
【题目】黑火药是中国的“四大发明”之一.黑火药在发生爆炸时,发生如下的反应:2KNO3+3C+S═K2S+N2↑+3CO2↑.该反应中,被氧化的元素是______,氧化剂是______,氧化产物是______.
科目:高中化学 来源: 题型:
【题目】如果M、SO42-、Mg2+和Na+四种离子以物质的量之比为2∶4∶1∶2共同存在于同一种溶液中,那么M可能是
A. Ba2+ B. CO32- C. Cu2+ D. Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丙烯腈(CH2===CHCN)是一种重要的化工原料,工业上可用“丙烯氨氧化法”生产,主要副产物有丙烯醛(CH2===CHCHO)和乙腈(CH3CN)等。回答下列问题:
(1)以丙烯、氨、氧气为原料,在催化剂存在下生成丙烯腈(C3H3N)和副产物丙烯醛(C3H4O)的热化学方程式如下:
①C3H6(g)+NH3(g)+3/2O2(g)===C3H3N(g)+3H2O(g)ΔH=-515 kJ·mol-1
②C3H6(g)+O2(g)===C3H4O(g)+H2O(g)ΔH=-353 kJ·mol-1
有利于提高丙烯腈平衡产率的反应条件是__________;提高丙烯腈反应选择性的关键因素是________。
(2)图(a)为丙烯腈产率与反应温度的关系曲线,最高产率对应的温度为460 ℃。低于460 ℃时,丙烯腈的产率____(填“是”或“不是”)对应温度下的平衡产率,判断理由是________________;高于460 ℃时,丙烯腈产率降低的可能原因是________(双选,填标号)。
A.催化剂活性降低 B.平衡常数变大
C.副反应增多 D.反应活化能增大

(3)丙烯腈和丙烯醛的产率与n(氨)/n(丙烯)的关系如图(b)所示。由图可知,最佳n(氨)/n(丙烯)约为_____,理由是______________________________。进料气氨、空气、丙烯的理论体积比约为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图为氢氧燃料电池原理示意图,按照此图的提示,回答以下问题:
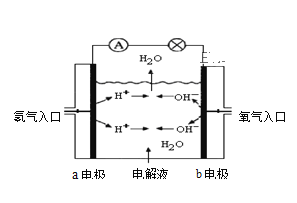
(1)下列叙述不正确的是 ______ 。
A.a电极是负极
B.b电极的电极反应为:4OH--4e-=2H2O+O2↑
C.氢氧燃料电池是一种具有应用前景的绿色电源
D.氢氧燃料电池是一种不需要将还原剂和氧化剂全部储藏在电池内的新型发电装置
(2)若电解质溶液为KOH溶液,则电极反应式为:a极 _________,b极 ____________;
(3)若电解质溶液为稀H2SO4,则电极反应式为:a极 __________,b极____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于甲苯的性质中,能说明苯环对侧链产生影响的是 ( )
A. 甲苯硝化生成三硝基甲苯
B. 甲苯能使酸性高锰酸钾溶液褪色
C. 甲苯与溴蒸汽混合光照可生成![]()
D. 甲苯与氢气可以发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.根据图中数据,试填写下列空白:
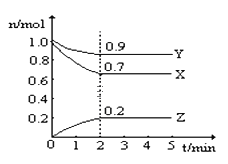
(1)该反应的化学方程式为 _______________________。
(2)从开始至2min,Z的平均反应速率为 ___________。
(3)某探究性学习小组用相同质量的锌和相同浓度的足量的稀盐酸反应得到实验数据如下表所示:
实验编号 | 锌的状态 | 反应温度/℃ | 收集100mL氢气所需时间/s |
Ⅰ | 薄片 | 15 | 200 |
Ⅱ | 薄片 | 25 | 90 |
Ⅲ | 粉末 | 25 | 10 |
①该实验的目的是探究 ______ 、 ______ 对锌和稀盐酸反应速率的影响;
②实验Ⅰ和Ⅱ表明 ________________________________ ,化学反应速率越大;
③能表明固体的表面积对反应速率有影响的实验编号是 ______ 和 ______;
④请设计一个实验方案证明盐酸的浓度对该反应的速率的影响: ______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】表是现行中学化学教科书中元素周期表的一部分,除标出的元素外。表中的每个编号表示一种元素,请根据要求回答问题:
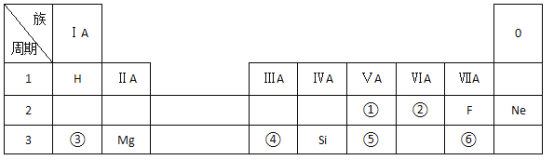
(1)②表示的元素是____________(填元素符号)。
(2)①与⑤两种元素相比较,原子半径较大的是 ______(填元素符号);其非金属性较强的是 ______(填元素符号);其最高正价氧化物水化物酸性较强的酸是_____(填分子式)。
(3)⑥元素的单质可以用来制取漂白粉,其有效成分是______(填化学式)。
③与⑥两种元素所形成化合物的电子式是____________。
(4)写出元素③的最高价氧化物对应的水化物与元素④的最高价氧化物对应的水化物相互反应的化学方程式________________________。
(5)②与⑥元素的氢化物的稳定性 ______大于______(填分子式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】鉴别FeCl3溶液和Fe(OH)3胶体,下列方法中最简单有效的是( )
A. 加入足量的NaOH溶液 B. 加热煮沸
C. 加入足量的盐酸 D. 观察是否产生丁达尔现象(效应)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com