
【题目】为探究铜与6molL﹣1硝酸反应的气态产物中是否含NO2 , 进行如下实验.
已知:FeSO4+NO[Fe(NO)]SO4(棕色),该反应较缓慢,待生成一定量[Fe(NO)]2+时突显明显棕色.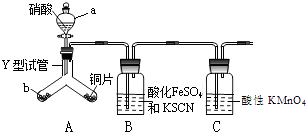
(1)实验前需检验装置的气密性,简述操作 .
(2)仪器a的名称
(3)实验开始时先将Y形试管向盛有块状固体b的支管倾斜,缓慢滴入稀硝酸,该实验操作的目的是;
(4)证明有NO2的实验现象
(5)装置C的作用 , 反应离子方程式 .
(6)测定化学试剂绿矾(FeSO47H2O)纯度的方法:称取绿矾3.000g置于锥形瓶中,加入100mL蒸馏水,加入10mLH2SO4和5mLH3PO4 , 用0.1000molL﹣1KMnO4溶液滴定至终点,消耗KMnO4溶液20.00mL.KMnO4溶液盛放在棕色式(填“酸”或“碱”)滴定管中,列式计算绿矾的纯度 .
【答案】
(1)关闭分液漏斗活塞,用酒精灯加热Y试管,观察到BC导管口有气泡产生,停止加热,BC长导管到吸入一段水柱,则装置气密性良好
(2)分液漏斗
(3)利用生成的CO2将整个装置内的空气赶尽,避免NO和O2反应生成NO2对气体产物的观察产生干扰
(4)利用生成的CO2将整个装置内的空气赶尽,避免NO和O2反应生成NO2对气体产物的观察产生干扰
(5)吸收尾气NO;5NO+3MnO4﹣+4H+=5NO3﹣+3Mn2++2H2O
(6)酸;![]() ×100%=92.67%
×100%=92.67%
【解析】解:(1.)根据压强差进行装置气密性的检验,具体方法为:关闭分液漏斗活塞,用酒精灯加热Y试管,观察到BC导管口有气泡产生,停止加热,BC长导管到吸入一段水柱,则装置气密性良好;所以答案是:关闭分液漏斗活塞,用酒精灯加热Y试管,观察到BC导管口有气泡产生,停止加热,BC长导管到吸入一段水柱,则装置气密性良好;
(2.)根据装置图可知仪器A的名称为分液漏斗,所以答案是:分液漏斗;
(3.)实验开始时先将Y形试管向盛有碳酸钙的支管倾斜,缓慢滴入稀硝酸,碳酸钙与稀硝酸生成CO2 , 将整个装置内的空气赶尽,避免NO和O2反应生成NO2对气体产物的观察产生干扰,所以答案是:利用生成的CO2将整个装置内的空气赶尽,避免NO和O2反应生成NO2对气体产物的观察产生干扰;
(4.)本实验生成的气体中,若有NO2 , NO2溶于水生成硝酸,把Fe2+氧化成Fe3+ , B瓶溶液出现血红色;若无二氧化氮则无血红色,所以证明有NO2的实验现象是铜与硝酸反应不久即观察到B中溶液呈红色,所以答案是:铜与硝酸反应不久即观察到B中溶液呈红色;
(5.)高锰酸钾溶液能将一氧化氮氧化成硝酸根,而防止其污染空气,反应的离子方程式为5NO+3MnO4﹣+4H+=5NO3﹣+3Mn2++2H2O,所以答案是:吸收尾气NO;5NO+3MnO4﹣+4H+=5NO3﹣+3Mn2++2H2O;
(6.)高锰酸钾溶液有强氧化性,应用酸式滴定管中进行滴定,滴定中消耗的高锰酸钾的物质的量为0.1000molL﹣1×0.02L=0.002mol,根据电子得失守恒可知关系式5FeSO47H2O~KMnO4 , 所以样品中FeSO47H2O的质量为5×0.002mol×278g/mol,所以绿矾的纯度为 ![]() ×100%=92.67%,所以答案是:酸;
×100%=92.67%,所以答案是:酸; ![]() ×100%=92.67%.
×100%=92.67%.


 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案 全优冲刺100分系列答案
全优冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】下列热化学方程式中的△H可表示燃烧热的是( )
A.H2(g)+Cl2(g)═2HCl(g)△H=﹣184.8KJ/mol
B.C2H4(g)+O2(g)═2CO2(g)+2H2O(l)△H=﹣1411.0KJ/mol
C.CH4(g)+ ![]() O2(g)═CO(g)+2H2O(l)△H=﹣6071.3KJ/mol
O2(g)═CO(g)+2H2O(l)△H=﹣6071.3KJ/mol
D.H2(g)+ ![]() O2(g)═H2O(g)△H=﹣241.8KJ/mol
O2(g)═H2O(g)△H=﹣241.8KJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家冶炼出了纯度高达99.9999%的铁,你估计它不会具有的性质是
A.在潮湿的空气中放置不易生锈B.硬度比生铁大
C.与2mol/L盐酸的反应生成氢气D.在冷的浓H2SO4溶液中可钝化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D是中学化学常见物质,它们在一定条件下有A+B→C+D的转化关系.
(1)若A为金属铝,B为氧化铁,该反应的一种用途是 .
(2)若A是一种能使湿润的红色石蕊试纸变蓝的气体,且该反应是工业上制取硝酸的重要反应之一,该反应的化学反应方程式为 .
(3)若A是淡黄色粉末,常用作供氧剂,C为强碱,则该反应的化学反应方程式为 .
(4)若A、B、D都是有机化合物,其中A、B是家庭厨房中常见调味品的主要成分,且A 的相对分子质量比B大14.
①该反应的化学反应方程式为 .
②某种以B为反应物的新型电池如右所示,该电池的负极的电极反应式为 .
(5)ClO2可将弱酸性废水中的Mn2+转化为MnO2而除去,同时ClO2被还原为Cl﹣ , 该反应的离子方程式为 . 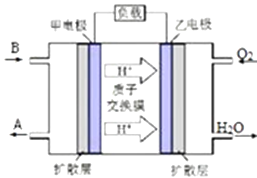
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验现象的描述正确的是( )
A.点燃棉纱线,产生烧焦羽毛气味
B.将浓硝酸加入到鸡蛋清溶液中,出现黄色
C.在空气中打开盛有浓盐酸的试剂瓶,瓶口冒白烟
D.把铜丝放入硫酸铝溶液中,紫红色固体表面产生银白色固体,溶液变成蓝色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于研究物质性质的方法和程序的论述中,正确的是( )
A.“方法”和“程序”完全不是一回事
B.“方法”和“程序”完全是一回事
C.“方法”和“程序”是两个不同的概念
D.“方法”和“程序”只有相互配合才能有效地完成研究物质性质的任务
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)现有碳、二氧化碳、氧化铁、石灰水、稀硫酸和纯碱溶液等6种物质。

①除稀硫酸外,试分别将其他物质的化学式填入如图相应的5个圆圈内,使每个圆圈内的物质都能与相邻物质发生反应。
②用化学方程式将它们与相邻物质间发生的反应表示出来:
_____________________________;
_____________________________;
_____________________________;
_____________________________;
_____________________________;
_____________________________。
(2)以下表示的是碳及其化合物之间的转化关系:
C![]() CO2
CO2![]() H2CO3
H2CO3![]() CaCO3
CaCO3![]() CO2
CO2
其中涉及的基本反应类型依次为_________、__________、__________、__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将2.0mol/L CuSO4溶液和1.0mol/L H2SO4溶液等体积混合(假设混合后溶液的体积等于混合前两种溶液的体积之和)。
(1)混合液中![]() 的物质的量浓度为__________。
的物质的量浓度为__________。
(2)向溶液中加入足量的铁粉,经足够长的时间后,铁粉有剩余,则反应后溶液中Fe2+的物质的量浓度为__________。(假定反应前后溶液的体积不变)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com