
| A、中和此溶液所需的0.1 mol?L-1 NaOH溶液的体积增加 |
| B、c(CH3COOH)减小,平衡向电离方向移动,c(CH3COO-)增大 |
| C、平衡向电离方向移动,c(CH3COOH)、c(H+)、c(OH-)、c(CH3COO-)均减小 |
| D、电离程度增大,由CH3COOH电离出的n(H+)变大 |


科目:高中化学 来源: 题型:
 ,下列说法正确的是( )
,下列说法正确的是( )| A、HOOC-CH2-CH(OH)-COOH与苹果酸互为同分异构体 |
| B、1mol苹果酸可与3mol NaOH发生中和反应 |
| C、1mol苹果酸与足量金属Na反应生成生成1mol H2 |
| D、苹果酸在一定条件下能发生缩聚反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、蛋白质溶液里加入饱和硫酸铵溶液,蛋白质析出,虽再加水,也不再溶解 |
| B、人工合成的具有生命活力的蛋白质-结晶牛胰岛素是我国科学家在1965年首次合成的 |
| C、重金属盐能使蛋白质凝结,所以误食重金属盐会中毒 |
| D、浓硝酸溅在皮肤上,使皮肤呈黄色是由于浓硝酸和蛋白质发生了“颜色反应” |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、a、b、c、d四个点中处于平衡状态的点是a、b d |
| B、反应进行至25min时,曲线发生变化的原因是加入了 0.4molN |
| C、若调节温度使35min时体系内N的百分含量与15min时相等,应升高温度 |
| D、若40min后出现如图所示变化,则可能是加入了某种催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
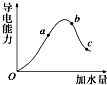 一定温度下,冰醋酸加水稀释过程中溶液的导电能力变化曲线如图所示,请回答:
一定温度下,冰醋酸加水稀释过程中溶液的导电能力变化曲线如图所示,请回答:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、均不变 |
| B、均增大 |
| C、①增大,②不变,③减少 |
| D、①减少,②不变,③增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、同时增大 |
| B、同时减小 |
| C、v1增加,v2减小 |
| D、v1减小,v2增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在室内放置一些特别的绿色植物,可用于室内空气的净化 |
| B、合金的熔点一般高于各组成成分金属的熔点 |
| C、氢氧化钠溶液用盖橡胶塞的试剂瓶盛装 |
| D、工业上用盐酸刻蚀玻璃 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| KCl | K2SO4 | ZnSO4 | ZnCl2 | |
| 1 | 0.3mol | 0.2mol | 0.1mol | - |
| 2 | 0.1mol | 0.3mol | - | 0.1mol |
| A、只有n(K+)相同 |
| B、只有n(Cl-)相同 |
| C、各离子的物质的量均不同 |
| D、各离子的物质的量完全相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com