
人类将在未来将逐渐由“碳素燃料文明时代”过渡至“太阳能文明时代”(包括风能、生物质能等太阳能转换形态),届时人们将适应“低碳经济”和“低碳生活”。下列说法错误的是
A.煤、石油和天然气都属于碳素燃料 B.发展太阳能经济有助于减缓温室效应
C.太阳能电池可将太阳能直接转化为电能
D.目前研究菠菜蛋白质“发电”不属于“太阳能文明”
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
(1)元素周期表是我们研究物质性质、结构的重要工具,对周期表的熟悉和掌握程度直接影响我们对化学的学习。元素周期表共有 个周期 个族;第六周期共有____种元素;在周期表中有些族的元素还有些特别的名称,如第ⅠA族(除氢)_______________,卤族元素位于第 纵行;最高正价与最低负价的绝对值相等的元素位于__________族。
(2)迁移是一种重要的学习能力,在学习时应充分发挥已有的知识从而迁移获取新的知识。在元素周期表中,上一周期的左上角某些元素与相邻的下一周期的右下角另一些元素性质相似,称为对角线规则。根据对角线规则,金属铍(Be)与铝单质及其化合物的性质相似。试写出氢氧化铍与氢氧化钠反应的化学方程式:______________________________________。
(3)现有部分短周期元素的性质或原子结构如下表:
| 元素编号 | 元素性质或原子结构 |
| A | 该元素有一种核素质量数为1 |
| B | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| C | 形成的简单离子是第三周期元素形成简单离子半径中最小的 |
①由元素A、B形成的核外电子总数为10e-的微粒:____________;(写2种)
②C元素在周期中的位置:_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在探究新制饱和氯水成分的实验中,下列根据实验现象得出的结论不正确的是
A.氯水的颜色呈浅绿色,说明氯水中含有Cl2
B.向氯水中滴加硝酸酸化的AgNO3溶液,产生白色沉淀,说明氯水中含有Cl-
C.向氯水中加入NaHCO3粉末,有气泡产生,说明氯水中含有H+
D.向FeCl2溶液中滴加氯水,溶液颜色变成棕黄色,说明氯水中含有HClO
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验设计方案中,可行的是( )
|
| A. | 用洗气瓶中的NaOH溶液除去CO2中混有的HCl气体 |
|
| B. | 在某试样中加入NaOH溶液加热,产生能使蓝色石蕊试纸变红的气体即证明有NH4+ |
|
| C. | 焰色反应实验中用硫酸清洗铁丝,灼烧后再沾取试样在酒精灯上灼烧观察 |
|
| D. | 分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)氢气、甲烷(CH4)、水各1g,其中含分子数最多的是 H2 ;含氢原子最多的是 H2 ;
(2)氢气、甲烷、水各1mol,含分子数是否一样多? 是 (填“是”或“否”)
含氢原子数最多的是 CH4 .
(3)6.02×1024个Na+约含 10 mol Na+,其质量为 230 g;49gH2SO4约含有 6.02×1023 个H,共含有 3.5 mol原子.
查看答案和解析>>
科目:高中化学 来源: 题型:
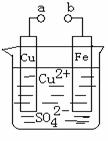
某小组为研究电化学原理,设计如图装置,下列叙述不正确的是
A.a和b不连接时,铁片上会有金属铜析出
B.a和b用导线连接时,溶液中的SO42-向铁电极移动,铜片上发生的反应为:Cu2++2e-= Cu
C.无论a和b是否连接,铁片均会溶解,溶液从蓝色逐渐变成浅绿色
D.a和b分别连接直流电源正、负极, 溶液中的Cu2+向铜电极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
水的电离过程为H2O H++OH-,在25℃、35℃时其离子积分别为
H++OH-,在25℃、35℃时其离子积分别为
K(25℃)=1.0×10-14、K(35℃)=2.1×10-14,则下列说法中正确的是
A.水的电离过程是吸热过程 B.c(H+)随着温度的降低而升高
C.在35℃时,纯水中c(H+)>c(OH-) D.水的电离度α(25℃)>α(35℃)
查看答案和解析>>
科目:高中化学 来源: 题型:
工厂使用石油热裂解的副产物甲烷来制取氢气,其生产流程如下图:
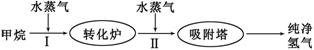
(1)此流程的第II步反应为:CO(g)+H2O(g) H2(g)+CO2(g),该反应的平衡常数随温度的变化如下表:
H2(g)+CO2(g),该反应的平衡常数随温度的变化如下表:
| 温度/℃ | 400 | 500 | 830 |
| 平衡常数K | 10 | 9 | 1 |
从上表可以推断:此反应是 (填“吸”或“放”)热反应。在830℃下,若开始时向恒容密闭容器中充入1mo1CO和2mo1H2O,则达到平衡后CO的转化率为 。
(2)在500℃,以下表的物质的量(按照CO、H2O、H2、CO2的顺序)投入恒容密闭容器中进行上述第II步反应,达到平衡后下列关系正确的是 。
| 实验编号 | 反应物投入量 | 平衡时H2浓度 | 吸收或放出的热量 | 反应物转化率 |
| A | 1、1、0、0 | c1 | Q1 | α1 |
| B | 0、0、2、2 | c2 | Q2 | α2
|
| C | 2、2、0、0 | c3 | Q3 | α3 |
A.2c1= c2 =c3 B.2Q1=Q2=Q3 C.α1 =α2 =α3 D.α1 +α2 =1
(3)在一个绝热等容容器中,不能判断此流程的第II步反应达到平衡的是 。
①体系的压强不再发生变化 ②混合气体的密度不变
③混合气体的平均相对分子质量不变 ④各组分的物质的量浓度不再改变
⑤体系的温度不再发生变化 ⑥v(CO2)正=v(H2O)逆
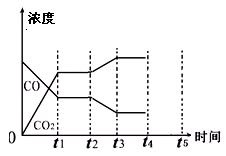
(4)下图表示此流程的第II步反应,在t1时刻达到平衡、在t2时刻因改变某个条件浓度发生变化的情况:图中t2时刻发生改变的条件是 、
(写出两种)。若t4时刻通过改变容积的方法将压强增大为原先的两倍,在图中t4和t5区间内画出CO、CO2浓度变化曲线,并标明物质(假设各物质状态均保持不变)。
查看答案和解析>>
科目:高中化学 来源: 题型:
最近我国学者发现,以精CuFeS2矿为原料在沸腾炉中和O2(空气)反应,生成物冷却后经溶解、除铁、结晶,得到CuSO4•5H2O.实验结果如下下列关于这一过程的叙述错误的是
| 沸腾炉炉度/℃ | 560 | 580 | 600 | 620 | 640 | 660 | |
| 生成物 | 水溶性Cu% | 90.12 | 91.24 | 93.50 | 92.38 | 89.96 | 84.23 |
| 酸溶性Cu% | 92.00 | 93.60 | 97.08 | 97.82 | 98.16 | 98.19 | |
| 酸溶性Fe% | 8.56 | 6.72 | 3.46 | 2.78 | 2.37 | 2.28 |
A.反应中有二氧化硫生成
B.产物中铜元素主要以氧化物形式存在
C.随温度升高,铁的氧化物在酸中的溶解度降低
D.温度于600~620℃生成物中水溶性Cu(%)下降的原因是水溶性铜分解所致
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com