
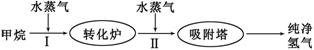
工厂使用石油热裂解的副产物甲烷来制取氢气,其生产流程如下图:
(1)此流程的第II步反应为:CO(g)+H2O(g) H2(g)+CO2(g),该反应的平衡常数随温度的变化如下表:
H2(g)+CO2(g),该反应的平衡常数随温度的变化如下表:
| 温度/℃ | 400 | 500 | 830 |
| 平衡常数K | 10 | 9 | 1 |
从上表可以推断:此反应是 (填“吸”或“放”)热反应。在830℃下,若开始时向恒容密闭容器中充入1mo1CO和2mo1H2O,则达到平衡后CO的转化率为 。
(2)在500℃,以下表的物质的量(按照CO、H2O、H2、CO2的顺序)投入恒容密闭容器中进行上述第II步反应,达到平衡后下列关系正确的是 。
| 实验编号 | 反应物投入量 | 平衡时H2浓度 | 吸收或放出的热量 | 反应物转化率 |
| A | 1、1、0、0 | c1 | Q1 | α1 |
| B | 0、0、2、2 | c2 | Q2 | α2
|
| C | 2、2、0、0 | c3 | Q3 | α3 |
A.2c1= c2 =c3 B.2Q1=Q2=Q3 C.α1 =α2 =α3 D.α1 +α2 =1
(3)在一个绝热等容容器中,不能判断此流程的第II步反应达到平衡的是 。
①体系的压强不再发生变化 ②混合气体的密度不变
③混合气体的平均相对分子质量不变 ④各组分的物质的量浓度不再改变
⑤体系的温度不再发生变化 ⑥v(CO2)正=v(H2O)逆
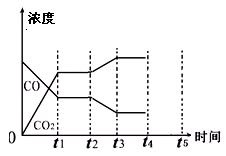
(4)下图表示此流程的第II步反应,在t1时刻达到平衡、在t2时刻因改变某个条件浓度发生变化的情况:图中t2时刻发生改变的条件是 、
(写出两种)。若t4时刻通过改变容积的方法将压强增大为原先的两倍,在图中t4和t5区间内画出CO、CO2浓度变化曲线,并标明物质(假设各物质状态均保持不变)。
科目:高中化学 来源: 题型:
食物是维持人类生命和健康的支柱。下表是某食品包装袋上的说明:
| 品名 | 蔬菜苏打饼 |
| 配料 | 面粉、鲜鸡蛋、精炼食用植物油、白砂糖、奶油、食盐、脱水青菜、橙汁、食品添加剂(碳酸氢钠) |
| 保质期 | 十二个月 |
| 生产日期 | 2010年11月6日 |
(1)对上表中各种配料成分的理解,不正确的是( )。
A.富含蛋白质的是鲜鸡蛋 B.富含维生素的是脱水青菜和橙汁
C.富含淀粉的是面粉和白砂糖 D.富含油脂的是精炼食用植物油和奶油
(2)以今天的日期为准,该饼干能否食用 ( 填“是”或“否”)原因是
(3)上表中碳酸氢钠是作为 ,其原理是(用化学方程式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
人类将在未来将逐渐由“碳素燃料文明时代”过渡至“太阳能文明时代”(包括风能、生物质能等太阳能转换形态),届时人们将适应“低碳经济”和“低碳生活”。下列说法错误的是
A.煤、石油和天然气都属于碳素燃料 B.发展太阳能经济有助于减缓温室效应
C.太阳能电池可将太阳能直接转化为电能
D.目前研究菠菜蛋白质“发电”不属于“太阳能文明”
查看答案和解析>>
科目:高中化学 来源: 题型:
将BaO2放入密闭真空容器中,反应 2BaO2(s)  2BaO(s)+O2(g) 达到平衡,保持温度不变,缩小容器容积,体系重新达到平衡,下列说法正确的是
2BaO(s)+O2(g) 达到平衡,保持温度不变,缩小容器容积,体系重新达到平衡,下列说法正确的是
A、平衡常数减小 B、BaO量不变 C、氧气压强不变 D、BaO2量减小
查看答案和解析>>
科目:高中化学 来源: 题型:
已知: C(s)+H2O(g)=CO(g)+H2(g) ΔH=akJ·mol-1
C(s)+ 1/2 O2(g) =CO(g) ΔH=-110kJ·mol-1
H-H、O=O和O-H键的键能分别为436、496和462kJ·mol-1,则a为
A.-332 B.-118 C.+350 D.+130
查看答案和解析>>
科目:高中化学 来源: 题型:
科学家制造出由4个氧原子构成的氧分子,并用质谱仪探测后证实了它的存在。下列关于该氧分子的说法正确的是
A.是氧元素的一种同位素 B.是氧元素的一种单质,分子内含有共价键
C.是一种新的氧化物 D.是臭氧的同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
中科院国家纳米科学中心2013年11月22日宣布,该中心科研人员在国际上首次“拍”到氢键的“照片”,实现了氢键的实空间成像,为“氢键的本质”这一化学界争论了80多年的问题提供了直观证据。这不仅将人类对微观世界的认识向前推进了一大步,也为在分子、原子尺度上的研究提供了更精确的方法。下列说法中正确的是
A.氢键是自然界中最重要、存在最广泛的化学键之一
B.正是氢键的存在,冰能浮在水面上
C.由于氢键的存在,沸点:HCl>HBr>HI>HF
D.由于氢键的存在,水分子变的更稳定了
查看答案和解析>>
科目:高中化学 来源: 题型:
现用18.4 mol·L-1的浓硫酸来配制480mL 0.2 mol·L-1的稀硫酸,可供选择的仪器有:①玻璃棒 ②烧杯 ③胶头滴管 ④药匙 ⑤托盘天平⑥量筒
(1)上述仪器在配制过程中不需要用到的是__________________。(填序号)除上述仪器外,尚缺最重要的仪器是 。
(2)需要用量筒量取浓硫酸的体积为___________mL。
(3)实验中用到玻璃棒,其作用分别是:___________、__________。
(4)配制时,一般可分为以下几个步骤:
①量取 ②计算 ③稀释 ④摇匀 ⑤转移 ⑥洗涤 ⑦定容 ⑧冷却。
其正确的操作顺序为:②→①→③→____ →____→____→____→④(填序号)
(5)在配制过程中,下列操作可引起所配溶液浓度偏低的有____________(填序号)
①定容时,仰视刻度线。
②未冷却至室温就转移到容量瓶中。
③容量瓶中含有少量蒸馏水。
④未洗涤稀释浓硫酸时用过的烧杯和玻璃棒。
⑤定容摇匀后,发现液面低于刻度线,又用胶头滴管加蒸馏水至刻度线。
(6)取所配制的稀硫酸100mL,与一定质量的锌充分反应,锌全部溶解后,生成的气体在标准状况下的体积为0.224L,则参加反应的锌的质量为 g,设反应后溶液的体积仍为100mL,则反应后溶液中H+的物质的量浓度为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
某元素的一种同位素X的原子质量数为A,含N个中子,它与1H原子组成HmX分子,在ag HmX中所含质子的物质的量是
A.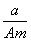 (A-N)mol B.
(A-N)mol B.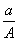 (A-N)mol C.
(A-N)mol C.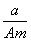 (A-N+m)mol D.
(A-N+m)mol D. 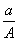 (A-N+m)mol
(A-N+m)mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com