
����18.4 mol��L-1��Ũ����������480mL 0.2 mol��L-1��ϡ���ᣬ�ɹ�ѡ��������У��ٲ����� ���ձ� �۽�ͷ�ι� ��ҩ�� ��������ƽ����Ͳ
��1���������������ƹ����в���Ҫ�õ�����__________________��������ţ������������⣬��ȱ����Ҫ�������� ��
��2����Ҫ����Ͳ��ȡŨ��������Ϊ___________mL��
��3��ʵ�����õ��������������÷ֱ��ǣ�___________��__________��
��4������ʱ��һ��ɷ�Ϊ���¼������裺
����ȡ �ڼ��� ��ϡ�� ��ҡ�� ��ת�� ��ϴ�� �߶��� ����ȴ��
����ȷ�IJ���˳��Ϊ���ڡ��١��ۡ�____ ��____��____��____���ܣ�����ţ�
��5�������ƹ����У����в���������������ҺŨ��ƫ�͵���____________������ţ�
�ٶ���ʱ�����ӿ̶��ߡ�
��δ��ȴ�����¾�ת�Ƶ�����ƿ�С�
������ƿ�к�����������ˮ��
��δϴ��ϡ��Ũ����ʱ�ù����ձ��Ͳ�������
�ݶ���ҡ�Ⱥ���Һ����ڿ̶��ߣ����ý�ͷ�ιܼ�����ˮ���̶��ߡ�
��6��ȡ�����Ƶ�ϡ����100mL����һ��������п��ַ�Ӧ��пȫ���ܽ�����ɵ������ڱ�״���µ����Ϊ0.224L����μӷ�Ӧ��п������Ϊ g���跴Ӧ����Һ�������Ϊ100mL����Ӧ����Һ��H+�����ʵ���Ũ��Ϊ ��
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ʵ����Ʒ����У����е��ǣ�������
| �� | A�� | ��ϴ��ƿ�е�NaOH��Һ��ȥCO2�л��е�HCl���� |
| �� | B�� | ��ij�����м���NaOH��Һ���ȣ�������ʹ��ɫʯ����ֽ�������弴֤����NH4+ |
| �� | C�� | ��ɫ��Ӧʵ������������ϴ��˿�����պ���մȡ�����ھƾ��������չ۲� |
| �� | D�� | ��Һ����ʱ����Һ©�����²�Һ����¿ڷų����ϲ�Һ����Ͽڵ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ʹ��ʯ�����ѽ�ĸ������������ȡ��������������������ͼ��
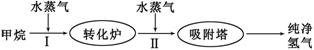
��1�������̵ĵ�II����ӦΪ��CO(g)��H2O(g) H2(g)��CO2(g)���÷�Ӧ��ƽ�ⳣ�����¶ȵı仯���±���
H2(g)��CO2(g)���÷�Ӧ��ƽ�ⳣ�����¶ȵı仯���±���
| �¶�/�� | 400 | 500 | 830 |
| ƽ�ⳣ��K | 10 | 9 | 1 |
���ϱ������ƶϣ��˷�Ӧ�� ��������š����ȷ�Ӧ����830���£�����ʼʱ������ܱ������г���1mo1CO��2mo1H2O����ﵽƽ���CO��ת����Ϊ ��
��2����500�棬���±������ʵ���������CO��H2O��H2��CO2��˳��Ͷ������ܱ������н���������II����Ӧ���ﵽƽ������й�ϵ��ȷ���� ��
| ʵ���� | ��Ӧ��Ͷ���� | ƽ��ʱH2Ũ�� | ���ջ�ų������� | ��Ӧ��ת���� |
| A | 1��1��0��0 | c1 | Q1 | ��1 |
| B | 0��0��2��2 | c2 | Q2 | ��2
|
| C | 2��2��0��0 | c3 | Q3 | ��3 |
A��2c1= c2 =c3 B��2Q1=Q2=Q3 C����1 =��2 =��3 D����1 +��2 =1
��3����һ�����ȵ��������У������жϴ����̵ĵ�II����Ӧ�ﵽƽ����� ��
����ϵ��ѹǿ���ٷ����仯 �ڻ��������ܶȲ���
�ۻ�������ƽ����Է����������� �ܸ���ֵ����ʵ���Ũ�Ȳ��ٸı�
����ϵ���¶Ȳ��ٷ����仯 ��v(CO2)����v(H2O)��
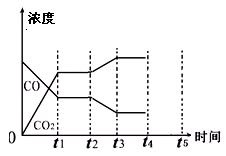
��4����ͼ��ʾ�����̵ĵ�II����Ӧ����t1ʱ�̴ﵽƽ�⡢��t2ʱ����ı�ij������Ũ�ȷ����仯�������ͼ��t2ʱ�̷����ı�������� ��
��д�����֣�����t4ʱ��ͨ���ı��ݻ��ķ�����ѹǿ����Ϊԭ�ȵ���������ͼ��t4��t5�����ڻ���CO��CO2Ũ�ȱ仯���ߣ����������ʣ����������״̬�����ֲ��䣩��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���и����е��������ʲ����Ժ��ֱ�����ϣ�ֻҪ�����������ʵ���һ��������ȫȼ������O2���������ֲ������
A��C3H6��C2H4 B��C2H6��C2H6O C��C2H4��C2H6O D��C3H4��C2H6O

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�ڹ��������£�CH4��Cl2�ܷ���ȡ����Ӧ������1 mol CH4��Cl2��Ӧ������Ӧ��ɺ��������л�ȡ��������ʵ���֮��Ϊn��CH3Cl����n��CH2Cl2����n��CHCl3����n��CCl4����1��2��3��4,�����ĵ�Cl2Ϊ
A��1.0 mol B��2.0 mol C��3.0 mol D��4.0 mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
һ������XԪ�ع��ɵ���̬����X2������3�֣���Է��������ֱ�Ϊ32��34��36����֪������3�ַ�����֮��Ϊ15��4��1���ɴ˿���ȷ������
A.��������X2ȫ��ת��Ϊ����ͬ��������X3����ôX3�ķ�������3��
B.������Ϊ16��һ�ֺ����ڴ������е�ԭ�Ӱٷ���Ϊ85%
C.ֻҪ������ͬλ����ɲ��䣬Xԭ�����κ������·���������ϣ����õ����� X2��������֮������15��4��1
D.��������X2��ƽ����������34
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ҹ�ѧ�߷��֣��Ծ�CuFeS2��Ϊԭ���ڷ���¯�к�O2����������Ӧ����������ȴ���ܽ⡢�������ᾧ���õ�CuSO4•5H2O��ʵ�����������й�����һ���̵������������
| ����¯¯��/�� | 560 | 580 | 600 | 620 | 640 | 660 | |
| ������ | ˮ����Cu% | 90.12 | 91.24 | 93.50 | 92.38 | 89.96 | 84.23 |
| ������Cu% | 92.00 | 93.60 | 97.08 | 97.82 | 98.16 | 98.19 | |
| ������Fe% | 8.56 | 6.72 | 3.46 | 2.78 | 2.37 | 2.28 |
A.��Ӧ���ж�����������
B.������ͭԪ����Ҫ����������ʽ����
C.���¶����ߣ����������������е��ܽ�Ƚ���
D.�¶���600��620����������ˮ����Cu��%���½���ԭ����ˮ����ͭ�ֽ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����藍�Cs�����仯��������ʣ�˵����ȷ����
A������蘆��۵�Ƚ����Ƹ� B��CsOH��NaOH�ļ���ǿ
C��Cs��H2O�ܾ��ҷ�Ӧ������������ը D��̼���������ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A��G�����л�����ǵ�ת����ϵ���£�
��ش��������⣺
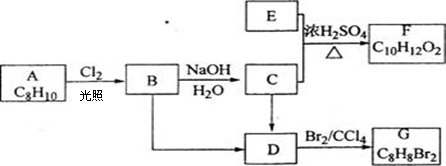 |
(1)��֪��6��0g������E��ȫȼ������8.8gCO2��3.6gH2O��E������������������ܶ�Ϊ30����E�ķ���ʽΪ ��
��2��AΪһȡ��������B�к���һ��������B����C�Ļ�ѧ����ʽΪ
��3��д������ת���Ļ�ѧ����ʽ��
B��D
E+C��F
��4������������ת���õ���F�ж���ͬ���칹�壬ͬʱ��������������F��ͬ���칹���� �֡�
�ٱ�����ֻ��������λȡ����������һ��Ϊ�� ����F������ͬ�Ĺ����š�
����1molij���������������л��������������Һ��Ӧʱ����2mol�������ƣ��䷴Ӧ����ʽ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com