
����Ŀ�����÷�Ǧ���ص�Ǧ��(PbO��Pb��PbSO4��)���Ʊ���ϸ��������Ʒ��3PbO��PbSO4��H2O (����)����Ҫ�Ʊ��������£�
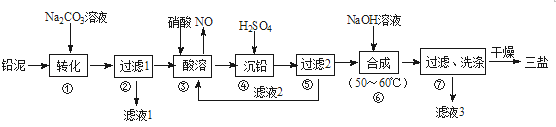
��1��������PbSO4ת��Ϊ����PbCO3�����ӷ���ʽΪ______________��
��2����Һ1����Һ3����ɫ���������ᾧ�ɵõ��ĸ���ƷΪ_________(д��ѧʽ)��
��3������������ʱ�����е�Ǧ����������Pb(NO3)2��NO�����ӷ���ʽΪ_______����Һ2��������Ҫ�ɷ�Ϊ________(д��ѧʽ)��
��4���������ϳ����εĻ�ѧ����ʽΪ___________��
��5��������ϴ�Ӳ���ʱ����������Ƿ�ϴ����ȫ�ķ�����_________��
���𰸡� CO32- +PbSO4 =PbCO3 + SO42- Na2SO410H2O����Na2SO4�� 3Pb +8H++2NO3- =3Pb2+ +2NO��+4H2O HNO3 4PbSO4+6NaOH = 3Na2SO4+3PbOPbSO4H2O+2H2O ȡ�������һ�ε�ϴ�ӹ���Һ���Թ��У������еμ������ữ��BaCl2��Һ������������ɫ�������������ϴ����ȫ
�������������������Ǧ���м���Na2CO3��Һ��PbSO4ת��Ϊ����PbCO3�����ӷ���ʽΪCO32-+PbSO4=PbCO3+SO42-��Ȼ����˵õ���Һ1ΪNa2SO4��Һ���������м����������ܣ�PbO��Pb��PbCO3�������ᷴӦ���� Pb(NO3)2��Pb�����ᷴӦ������NO��Ǧ����������Pb(NO3)2��NO�����ӷ���ʽΪ3Pb+8H++2NO3-=3Pb+2NO��+4H2O��Ȼ������Һ�м������ᣬ����bSO4���������ˣ���Һ2����Ҫ�ɷ���HNO3���������м���NaOH��Һ��������Ӧ4PbSO4+6NaOH=3Na2SO4+3PbOPbSO4H2O+2H2O������ϴ�Ӹ���õ�3PbOPbSO4H2O����Һ3�к���Na2SO4��
��1��ͨ�����Ϸ���֪��̼���ƺ�����Ǧ�����������ת�������ӷ���ʽΪCO32-+PbSO4=PbCO3+SO42-��
��2��ͨ�����Ϸ���֪����Һ1����Һ3����ɫ���������ᾧ�ɵõ��ĸ���ƷΪNa2SO410H2O(��Na2SO4)��
��3��ͨ�����Ϸ���֪�������ӷ�Ӧ����ʽΪ3Pb+8H++2NO3-=3Pb+2NO��+4H2O����Һ2����Ҫ�ɷ���δ��Ӧ��HNO3��
��4���÷�Ӧ����ʽΪ4PbSO4+6NaOH=3Na2SO4+3PbOPbSO4H2O+2H2O��
��5���ó�����������������������ӣ��������ữ���Ȼ������飬����鷽��Ϊȡ�������һ�ε�ϴ�ӹ���Һ���Թ��У������еμ������ữ��BaCl2��Һ������������ɫ�������������ϴ����ȫ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ҵ�������ϩ����ֱ��ˮ�Ϸ�����ˮ�Ϸ�������һЩת����ͼ��

ijЩ���ʵ��й��������±���
�۵�/�� | �е�/�� | ˮ���� | |
�Ҵ� | -114.1 | 78.3 | ���� |
��ȩ | -121 | 20.8 | ���� |
�������� | -83 | 77.0 | ���� |
�ش��������⣺
��1�����ˮ�Ϸ��е�ת���ۣ���ϩ��Ũ���ᷴӦ��������������(CH3CH2��OSO3H)���л���Ӧ������_____________��ת���ܵĻ�ѧ����ʽ��__________________��
��2��պ��B�IJ�����������������⻯�������ð���̣���Ӧ�Ļ�ѧ����ʽΪ________��ת���ݵĻ�ѧ����ʽΪ______________________________��
��3����һ����Ϊw��ͭ˿���ձ�ں�Ѹ�ٲ����Ҵ��У���ڵ�ͭ˿�ָ���ɫ��
��ʹͭ˿�ָ���ɫ�ķ�Ӧ�Ļ�ѧ����ʽΪ________________________��
����Ҫ֤��ͭ˿������ã�����Ҫ���еIJ�����_______________��
��4����֪��CH3CHO + NaHSO3 ��![]() ���������ǻ��һ����ƣ�������������ȩ�������·�ʽ�ᴿ��
���������ǻ��һ����ƣ�������������ȩ�������·�ʽ�ᴿ��
![]()
�٦����ǻ��һ����Ƶľ�������Ϊ___________________��
�ڷ������A��������________________��
��ijͬѧ��Ʒ������B��װ�ã��гֺͼ���װ������ȥ����ͼ��ʾ���������е�Һ��Ӧ��_____�ڽ������D����E����

�����йز�����װ�õķ�������ȷ����_____��������ĸ����ѡ���ۣ�
A���ձ���Ӧװ��ˮ
B��������Ӧͨ��ˮ
C��ͼʾװ�ÿ����ڳ�ȥ���������л��е��Ҵ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��H2SΪ��Ԫ���ᡣ20 ��ʱ����0.100 mol��L��1��Na2S��Һ�л���ͨ��HCl����(������Һ����ı仯��H2S�Ļӷ�)������ָ����Һ���������ʵ���Ũ�ȹ�ϵһ����ȷ����(����)
A. ͨ��HCl����֮ǰ�� c(S2��)>c(HS��)>c(OH��)>c(H��)
B. c(HS��)��c(S2��)�ļ�����Һ�У� c(Cl��)��c(HS��)>0.100 mol��L��1��c(H2S)
C. pH��7����Һ�У� c(Cl��)��c(HS��)��2c(H2S)
D. c(Cl��)��0.100 mol��L��1����Һ�У� c(OH��)��c(H��)��c(H2S)��c(S2��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��HCN(aq)��NaOH(aq)��Ӧ����H=��12.1kJ /mol��HCl(aq)��NaOH(aq)��Ӧ����H =��55.6kJ/ mol����HCN��ˮ��Һ�е������H����
A. ��67.7 kJ /mol B. ��43.5kJ /mol C. +43.5 kJ/ mol D. +67.7 kJ/ mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ݪ����������ҩ��ݪ�����еĻ��Գɷ�֮һ��������Ƣ������θ��ɢ�������ã�����һ�ֺϳ�·������(����������ȥ)��
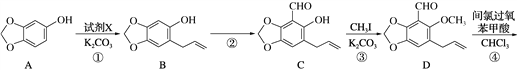
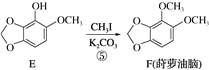
(1) ������A�����������________��________(�����������)��
(2) ��Ӧ�۵ķ�Ӧ������________��
(3) ��Ӧ���м����Լ�X�ķ���ʽΪC3H5Cl��X�Ľṹ��ʽΪ________________��
(4) B��һ��ͬ���칹����������������
��. ������������ȡ��������5�ֲ�ͬ��ѧ��������ԭ��
��. ���ܷ���������Ӧ������FeCl3������ɫ��Ӧ
д��һ�ַ���������ͬ���칹��Ľṹ��ʽ��________________��
(5) ��������֪ʶ����������Ϣ��д����![]() ��ClCH2CH2ClΪԭ���Ʊ�
��ClCH2CH2ClΪԭ���Ʊ�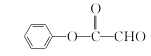 �ĺϳ�·������ͼ(���Լ�����) ______���ϳ�·������ͼʾ�����£�CH3CH2Br
�ĺϳ�·������ͼ(���Լ�����) ______���ϳ�·������ͼʾ�����£�CH3CH2Br![]() CH3CH2OH
CH3CH2OH![]() CH3COOCH2CH3
CH3COOCH2CH3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ�����ӵ���������ֵ������˵����ȷ����
A. 24gMg������N2��Ӧ����Mg3N2,ת�Ƶĵ�����Ϊ6NA
B. lmolNa218O2��������������Ϊ42NA
C. 9.8g��H2SO4��H3PO4��ɵĻ�����к��е���ԭ����Ϊ0.4NA
D. 1mol�������к��еĹ��ۼ���Ϊ12NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪����ʱ��0.1 mol/LijһԪ��HA��ˮ����0.1%�������룬���������������( )
A. ����Һ��pH=4 B. �����¶ȣ���Һ��pH�͵���ƽ�ⳣ������С
C. ����ĵ���ƽ�ⳣ��ԼΪ1��10-7 D. ����������HA������̶ȼ�С����ƽ�ⳣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������̶����ܱ������н��п��淴Ӧ2NO2![]() 2NO+O2����������Ϊ��Ӧ�ﵽƽ��״̬��־����( )
2NO+O2����������Ϊ��Ӧ�ﵽƽ��״̬��־����( )
����λʱ��������nmol O2��ͬʱ����2n mol NO2
����λʱ��������n mol O2 ��ͬʱ����2n mol NO
����NO2 ��NO��O2��ʾ�ķ�Ӧ����֮��Ϊ2��2��1
������������ɫ���ٸı� �����������ܶȲ��ٸı�
����������ѹǿ���ٸı� ����������ƽ����Է����������ٸı�
A���٢ܢޢ� B���ڢۢݢ� C���٢ۢܢ� D��ȫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ȥþ���л��е��������ۣ���ѡ�õ��Լ��ǣ� ��
A.����
B.NaOH��Һ
C.����
D.ʳ��ˮ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com