
 ij��A���л���ѧ��ҵ�Ļ���ԭ�ϣ������������������һ�����ҵ�ʯ�ͻ�����չˮƽ��A����һ��ֲ���������ڼ���A�ɷ�����ͼ��ʾ��һϵ�л�ѧ��Ӧ�����Т٢ڢ�����ͬ�ַ�Ӧ���ͣ�
ij��A���л���ѧ��ҵ�Ļ���ԭ�ϣ������������������һ�����ҵ�ʯ�ͻ�����չˮƽ��A����һ��ֲ���������ڼ���A�ɷ�����ͼ��ʾ��һϵ�л�ѧ��Ӧ�����Т٢ڢ�����ͬ�ַ�Ӧ���ͣ� ��
�� ��
�� ���� ��A�IJ���������������һ�����ҵ�ʯ�ͻ�����չˮƽ������һ��ֲ���������ڼ�����AΪ��ϩ����ϩ�����������ӳɷ�Ӧ����B��BΪ���飬��ϩ��HCl�����ӳɷ�Ӧ����C��CΪCH3CH2Cl����ϩ��ˮ�����ӳɷ�Ӧ����D��DΪ�Ҵ�����ϩ�����Ӿ۷�Ӧ���ɸ߷��ӻ�����E��E�Ǿ���ϩ���ݴ˽��
��� �⣺��1����A�IJ���������������һ�����ҵ�ʯ�ͻ�����չˮƽ������һ��ֲ���������ڼ�����AΪCH2=CH2��
A��B����ϩ����̼̼˫�����������ӳ��������飬��Ӧ�ķ���ʽΪ��CH2=CH2+H2$��_{��}^{Ni}$CH3CH3��
B��C����������������ȡ����Ӧ���������飬��Ӧ�ķ���ʽΪ��CH3CH3+Cl2$\stackrel{����}{��}$CH3CH2Cl+HCl��
A��C����ϩ��HCl�����ӳɷ�Ӧ����CH3CH2Cl����Ӧ����ʽΪ��CH2=CH2+HCl$��_{��}^{����}$CH3CH2Cl��
A��D����ϩ��ˮ�����ӳɷ�Ӧ�����Ҵ�����Ӧ����ʽΪ��CH2=CH2+H2O$\stackrel{ϡ����}{��}$CH3CH2OH��
A��E����ϩ�����Ӿ۷�Ӧ���ɾ���ϩ����ѧ����ʽ�� ��
��
����ABCDE�ֱ�Ϊ��CH2=CH2��CH3CH3��CH3CH2Cl��CH3CH2OH�� ��
��
�ʴ�Ϊ��CH2=CH2��CH3CH3��CH3CH2Cl��CH3CH2OH�� ��
��
��2����Ӧ������ϩ��HCl�����ӳɷ�Ӧ��CH2=CH2+HCl$��_{��}^{����}$CH3CH2Cl��
��Ӧ������ϩ�����Ӿ۷�Ӧ�� ��
��
�ʴ�Ϊ��CH2=CH2+HCl$��_{��}^{����}$CH3CH2Cl�� ��
��
���� ���⿼���л�����ƶϣ�Ϊ��Ƶ���㣬�����л�������������ʵĹ�ϵΪ���Ĺؼ������ط�����Ӧ�������Ŀ��飬ע��ת���й����ŵı仯����Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | $\frac{1}{2}$��$\frac{1}{22.4}$ | B�� | $\frac{1}{3}$��$\frac{1}{33.6}$ | C�� | $\frac{2}{3}$��$\frac{1}{11.2}$ | D�� | $\frac{3}{4}$��$\frac{1}{22.4}$ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
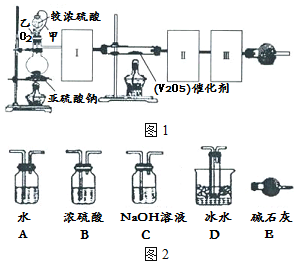
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
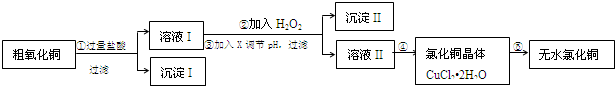
| �������↑ʼ����ʱ��pH | �������������ȫʱ��pH | |
| Fe3+ | 1.9 | 3.2 |
| Cu2+ | 4.7 | 6.7 |
| Fe2+ | 7.0 | 9.0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
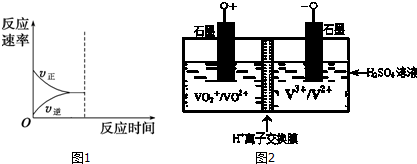
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �û�����ʹ�������������Һ��ɫ | |
| B�� | �û�����Һ����BaCl2�������ɳ��� | |
| C�� | �û�����H2SO4��Ӧ���������� | |
| D�� | �û��������������¿�����S��ÿ����1molSת��1.5NA������ |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com