
【题目】如图曲线a表示放热反应 X(g) + Y(g) + N(s) ![]() Z(g) + M(g)进行过程中X的转化率随时间变化的关系。在其它条件不变时改变某个条件,使反应过程按b曲线进行,可采取的措施是
Z(g) + M(g)进行过程中X的转化率随时间变化的关系。在其它条件不变时改变某个条件,使反应过程按b曲线进行,可采取的措施是

A.升高温度B.加大X的投入量
C.缩小容器的体积D.增加N的量
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】乙烯是一种重要的基本化工原料,可制备乙酸乙酯,其转化关系如图.

已知:H2C=CH﹣OH不稳定
I ①的反应类型是___.请写出乙烯官能团名称_____, 由A生成B的化学方程式_____.
II 某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中放有浓硫酸,B中放有乙醇、无水醋酸钠,D中放有饱和碳酸钠溶液。

已知:①无水氯化钙可与乙醇形成难溶于水的CaCl2·6C2H5OH;
②有关有机物的沸点见下表:
试剂 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
沸点(℃) | 34.7 | 78.5 | 118 | 77.1 |
请回答:
(1)浓硫酸的作用为_______;若用同位素18O示踪法确定反应产物水分子中氧原子的提供者,写出能表示18O位置的化学方程式__________
(2)球形干燥管C的作用是______若反应前D中加入几滴酚酞,溶液呈红色,反应结束后D中的现象是________。
(3)从D中分离出的乙酸乙酯中常含有一定量的乙醇、乙醚和水,应先加入无水氯化钙,分离出________;再加入(此空从下列选项中选择)________;然后进行蒸馏,收集77℃左右的馏分,以得到较纯净的乙酸乙酯。
A 五氧化二磷 B 碱石灰
C 无水硫酸钠 D 生石灰
(4)从绿色化学的角度分析,使用浓硫酸制乙酸乙酯不足之处主要有________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A只含有C、H、O三种元素,常用作有机合成的中间体。16.8g该有机物经燃烧生成44.0gCO2和14.4gH2O;质谱图表明其相对分子质量为84,红外光谱分析表明A分子中含有O—H键和位于分子端的—C≡C—键,核磁共振氢谱上有三个峰,峰面积之比为6∶1∶1。
(1)A的分子式是____________________________________。
(2)下列物质中,一定条件下能与A发生反应的是________。
A.H2 B.Na C.酸性KMnO4溶液 D.Br2
(3)A的结构简式是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应 Fe+H2SO4=FeSO4+H2↑的能量变化趋势如下图所示:

(1)该反应为___________________(填“吸热”或“放热”)反应。
(2)若要使该反应的反应速率加快,下列措施可行的是___________________(填字母)。
A.改铁片为铁粉 B.改稀硫酸为 98%的浓硫酸 C.升高温度 D.减小压强 E.加入少量的硝酸铜溶液 F.加入醋酸钠固体 G.加入氯化钠溶液
(3)若将上述反应设计成原电池,铜为原电池某一极材料,则铜为_________(填“正”或“负”)极。铜片上产生的现象为_____________________ , 该 极 上 发 生 的 电 极 反 应 为___________________________,外电路中电子由_____(填“正”或“负”,下同)极向_____________极移动。
(4)若将电解质溶液改为 FeCl3,则形成原电池的总反应式:__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列框图所示的转化关系中,![]() 、
、![]() 均为常见的金属单质;A、
均为常见的金属单质;A、![]() 在冷的
在冷的![]() 的浓溶液中均会发生钝化;
的浓溶液中均会发生钝化;![]() 为淡黄色的非金属单质。
为淡黄色的非金属单质。![]() 为红棕色固体氧化物,
为红棕色固体氧化物,![]() 为常见无色液体。
为常见无色液体。![]() 焰色为黄色,且能使酚酞变红(部分反应条件、反应过程中生成的水及其他产物略去)。
焰色为黄色,且能使酚酞变红(部分反应条件、反应过程中生成的水及其他产物略去)。

(1)![]() 的化学式为______。
的化学式为______。
(2)![]() 与
与![]() 反应的化学方程式为_____。
反应的化学方程式为_____。
(3)![]() 与氯气反应的离子方程式为_____。
与氯气反应的离子方程式为_____。
(4)![]() 与氨水反应的化学方程式为_______。
与氨水反应的化学方程式为_______。
(5)![]() 与
与![]() 反应的离子方程式为________。
反应的离子方程式为________。
(6)检验“黄色溶液”中阳离子的方案:________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】指出下列化学反应类型(氧化、酯化、加成、取代)
(1)CH2Cl2+Br2![]() CHBrCl2+HBr _____________
CHBrCl2+HBr _____________
(2)CH2=CH2+Br2→CH2BrCH2Br __________
(3)![]() +HNO3
+HNO3![]()
![]() NO2 +H2O _______________
NO2 +H2O _______________
(4)![]() ___________
___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒容密闭容器中存在下列平衡:![]() 。
。![]() 的平衡物质的量浓度与温度T的关系如图所示。则说法错误的是
的平衡物质的量浓度与温度T的关系如图所示。则说法错误的是
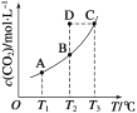
A.反应![]() 为吸热反应
为吸热反应
B.在![]() 时,若反应处于状态D,则一定有v正>v逆
时,若反应处于状态D,则一定有v正>v逆
C.平衡状态A与C相比,平衡状态A中的c(CO)大
D.若![]() 、
、![]() 时的平衡常数分别为
时的平衡常数分别为![]() ,则
,则![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,将0.10 mol·L-1盐酸逐滴滴入20.00 mL 0.10 mol·L-1氨水中,溶液中pH和pOH随加入盐酸体积变化曲线如图所示。已知:pOH= -lg c(OH-)。下列说法正确的是( )
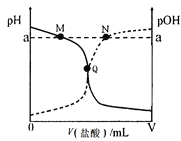
A. M点所示溶液中:c(NH4+)+c(NH3·H2O)= c(Cl-)
B. N点所示溶液中:c(NH4+)>c(Cl-)
C. Q点所示消耗盐酸的体积等于氨水的体积
D. M点和N点所示溶液中水的离子积相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】卤代烃 R—CH2—CH2—X 中化学键如图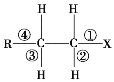 所示,则下列说法正确的是()
所示,则下列说法正确的是()
A. 发生水解反应时,被破坏的键是①和③
B. 发生消去反应时,被破坏的键是①和④
C. 发生水解反应时,被破坏的键是①
D. 发生消去反应时,被破坏的键是①和②
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com