
【题目】潜艇中氧气来源之一的反应是:2Na2O2+2H2O=4NaOH+O2↑。用NA表示阿伏加德罗常数,下列说法正确的是( )
A.22.4LO2含2NA个O原子
B.1.8gH2O含有的质子数为NA
C.1molNa2O2含共价键的总数为2NA
D.上述反应,每生成1molO2转移4mol电子
 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案科目:高中化学 来源: 题型:
【题目】不能正确表示下列变化的离子方程式是
A.用醋酸除去水垢:
B.用氢氧化钠溶液除去镁粉中的杂质铝:
C.室温下,测得小苏打溶液pH>7,证明碳酸是弱酸:![]()
D.将![]() 溶液与0.40mol·L-1NaOH溶液等体积混合:
溶液与0.40mol·L-1NaOH溶液等体积混合:
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】黑色固体A加热至红热投入到无色溶液B中发生如图转化关系。

(1)由此可以推断:A为________(填化学式,下同),B为_______,X为_______,C为_________,E为_________。
(2)写出A与B反应的化学方程式: ________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组以芳香族化合物A为主要原料,按下列线路合成抗癫痫药物W:

已知:![]()
请回答:
(1)下列说法正确的是________。
A.反应②是氧化反应 B.试剂X是浓硝酸和浓硫酸
C.反应③⑤的目的是保护![]() D.药物W的分子式是
D.药物W的分子式是![]()
(2)写出化合物C的结构简式________。
(3)写出反应⑥的化学方程式________。
(4)设计从G到H的合成路线(用流程图表示,无机试剂任选)________。
(5)写出化合物A的相邻同系物Y的同分异构体结构简式,且必须符合下列条件:________。
①能发生银镜反应;
②![]() 表明,分子中共有4种H原子;
表明,分子中共有4种H原子;
③除了苯环无其它环。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知热化学方程式:
H2O(g)═H2(g)+![]() O2(g)△H=+241.8kJ/mol
O2(g)△H=+241.8kJ/mol
H2(g)+![]() O2(g)═H2O(1)△H=﹣285.8kJ/mol
O2(g)═H2O(1)△H=﹣285.8kJ/mol
当1g液态水变为水蒸气时,其热量变化是
A.吸热44kJB.吸热2.44KJC.放热44kJD.放热2.44KJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)配平以下方程式
K2Cr2O7+__HC1=__KC1+__CrCl3+__H2O+__Cl2↑
以上反应中失电子的物质是_________,还原产物是______,每生成lmol这种还原产物,将有_________mol电子发生转移.氧化剂与还原剂的物质的量之比为_________.
(2)人体内的铁元素以Fe2+和Fe3+的形式存在。Fe2+易被吸收,所以补铁时,应补充含Fe2+的亚铁盐。服用维生素C可使食物中的Fe3+转化成Fe2+,利于人体对铁的吸收。
Ⅰ人体中经常进行Fe2+与Fe3+的转化,可表示为Fe2+![]() Fe3+。在过程A中,Fe2+作__________剂,过程B中,Fe3+作____________剂。
Fe3+。在过程A中,Fe2+作__________剂,过程B中,Fe3+作____________剂。
Ⅱ“服用维生素C可使食物中的Fe3+转化为Fe2+”这句话指出,维生素C在这个反应中作_______剂,具有_____________性。
(3)已知反应:2H2S+H2SO3=2H2O+3S↓,若氧化产物比还原产物多1.6g,则冋时会生成水的质量为____g.
(4)除去Na2CO3粉末中混入的NaHCO3杂质用______方法,化学方程式为_______.
(5)向FeBr2溶液中通入足量Cl2(己知氧化性Cl2>Br2>Fe3+)化学方程式为_______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己烷雌酚的一种合成路线如图:

下列说法不正确的是( )
A.化合物X难溶于水
B.在NaOH水溶液中加热,化合物X可发生取代反应
C.在一定条件,化合物Y可与CH3COOH发生缩聚反应
D.用FeCl3溶液可鉴别化合物X和Y
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国平原地区地下水质量差,铁、锰含量较高,需进行处理才能达到饮用水标准。地下水中铁锰的来源主要是矿物FeCO3和MnCO3。
(1)酸雨地区地下水中铁含量更高,结合化学用语从平衡移动角度解释原因_______。
(2)去除Fe2+
①除铁滤池经过曝气3~7天后,滤料表面形成______色物质,其成分是Fe(OH)3,使得溶液中Fe2+含量迅速下降,其作用过程如图所示。
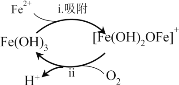
②将过程ii的离子方程式补充完整:________。
过程i:Fe2++Fe(OH)3=[Fe(OH)2OFe]++H+
过程ii:4[Fe(OH)2OFe]++ +10H2O= +
③有利于提高过程ii反应速率的措施是______(填序号)。
A. 降低温度 B. 通入足量O2 C. 搅拌
(3)去除Mn2+
向除锰滤池中加入ClO2将Mn2+氧化为MnO2,随着反应进行,滤池溶液的pH___(填“变大”“变小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】银白色固体A:①放在空气中可氧化生成白色固体B;②将A点燃,火焰呈黄色,生成淡黄色固体C;③A、B、C均可与无色液体D反应,生成碱性物质E,其中A跟D反应时还可以生成可燃性气体F,C跟D反应则生成另一种气体G;④F和G混合后遇火可剧烈反应而发生爆炸,并生成D。据此判断:
(1)A______,B______,C______,D________,E____,F_______,G_______。(填化学式)
(2)写出有关反应的化学方程式:
①___________________________________________。
②__________________________________________。
③__________________________________________。
④__________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com