
【题目】MnCO3可用于制备活性电极材料MnO2。以菱锰矿(含MnCO3、SiO2、FeCO3和少量Al2O3等)为原料制备碳酸锰粗产品的流程如下:

已知:①常温下,Ksp[Fe(OH)3]=8.0×10-38,Ksp[Al(OH)3]=4.0×10-34。
②氢氧化物沉淀的条件:Al3+、Fe3+完全沉淀的pH分别为4.6、3.4;Mn2+开始沉淀的pH为8.1。
(1)“酸浸”过程中不能用浓盐酸替代硫酸,原因是_________________________________。
(2)用离子方程式表示“氧化”过程中加MnO2的目的:_______________________________。
(3)“调pH”时,向含有硫酸铁和硫酸铝的混合溶液中滴加氢氧化钠溶液至两种沉淀共存,当c(Fe3+)=1.0×10-5mol·L-1时,c(Al3+)=______________mol·L-1。
(4)①“沉锰”过程中,反应的离子方程式为_____________________。
②“沉锰”过程中沉锰速率与温度的关系如图所示。当温度高于60℃时,沉锰速率随着温度升高而减慢的原因可能是_____________________________。

(5)从滤液3中可分离出一种不含碳元素的氮肥,它的化学式为_____________________________。
(6)工业上,可以将碳酸锰制成硫酸锰,再用惰性电极电解酸性硫酸锰溶液来制备活性二氧化锰,电解时的阳极反应式为________________________________。
【答案】 后续“氧化”过程中加入的二氧化锰会氧化浓盐酸 MnO2+2Fe2++4H===Mn2++2Fe3++2H2O 0.05 Mn2++2HCO3===MnCO3↓+CO2↑+H2O 温度过高时碳酸氢铵的分解速率显著加快,沉锰速率随碳酸氢铵浓度的减小而减慢 (NH4)2SO4 Mn2-2e+2H2O===MnO2+4H
【解析】菱锰矿用稀硫酸溶解,MnCO3、FeCO3、Al2O3都和稀硫酸反应生成硫酸盐,SiO2不反应,酸性条件下,加入MnO2将Fe2+氧化为Fe3+,MnO2还原生成Mn2+,调节溶液的pH,使Fe3+、Al3+完全转化为Fe(OH)3、Al(OH)3沉淀,过滤分离,滤渣1为SiO2、滤渣2为Al(OH)3、Fe(OH)3,滤液中存在 MnSO4、硫酸钠等,加入碳酸氢铵得到MnCO3,过滤分离,滤液3中含有硫酸铵、硫酸钠等。
(1)“酸浸”过程中不能用浓盐酸替代硫酸,原因是: 后续“氧化”过程中加入的二氧化锰会氧化浓盐酸。(2)“氧化”过程中加MnO2的目的:将亚铁氧化成铁离子,便于除去。用离子方程式表示MnO2+2Fe2++4H=Mn2++2Fe3++2H2O;(3)“调pH”时,向含有硫酸铁和硫酸铝的混合溶液中滴加氢氧化钠溶液至两种沉淀共存,当c(Fe3+)=1.0×10-5mol·L-1时,①Ksp[Fe(OH)3]=8.0×10-38=c(Fe3+)c3(OH-),②Ksp[Al(OH)3]=4.0×10-34=c(Al3+)c3(OH-),②比①式,解得:c(Al3+)= 0.05mol·L-1;(4)①“沉锰”过程中,MnCO3溶解度小,反应的离子方程式为Mn2++2HCO3=MnCO3↓+CO2↑+H2O。②当温度高于60℃时,沉锰速率随着温度升高而减慢的原因可能是: 温度过高时碳酸氢铵的分解速率显著加快,沉锰速率随碳酸氢铵浓度的减小而减慢;(5)从滤液3中含有硫酸铵、硫酸钠等,可分离出一种不含碳元素的氮肥,它的化学式为(NH4)2SO4。(6)电解时的阳极发生氧化反应,反应式为Mn2-2e+2H2O=MnO2+4H。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】下列各组物质分类正确的是
酸 | 碱 | 盐 | 氧化物 | |
A | 硫酸 | 纯碱 | 硅酸钠 | 干冰 |
B | 氢硫酸 | 烧碱 | 纯碱 | 氧化铜 |
C | 碳酸 | 生石灰 | 小苏打 | 二氧化硫 |
D | 二氧化碳 | 苛性钠 | 食盐 | 石灰石 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将9.6g铜单质置于200mL一定浓度的稀硝酸中,两者恰好完全反应.假定溶液体积不变,请回答下列问题:(要求写出计算过程) 
(1)反应生成的气体的体积(标况下);
(2)反应过程中转移电子的物质的量;
(3)参加反应的稀硝酸的物质的量浓度.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池.已知H2(g)、CO(g)和CH3OH(l)的燃烧热△H分别为﹣285.8kJmol﹣1、﹣283.0kJmol﹣1和﹣726.5kJmol﹣1 . 请回答下列问题:
(1)用太阳能分解10mol水消耗的能量是kJ.
(2)甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为 .
(3)在容积为2L的密闭容器中,由CO2和H2合成甲醇,在其他条件不变得情况下,考察温度对反应的影响,实验结果如图所示(注:T1、T2均大于300℃). 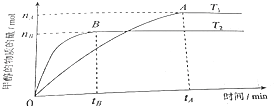
判断该可逆反应达到化学平衡状态的标志是(填字母).
①.v生成(CH3OH)=v消耗(CO2) ②.混合气体的密度不再改变
③.CO2、H2、CH3OH的浓度均不再变化 ④.混合气体的压强不再改变
(4)在直接以甲醇为燃料电池中,电解质溶液为酸性,负极的反应式为、正极的反应式为 . 理想状态下,该燃料电池消耗1mol甲醇所能产生的最大电能为702.1kJ,则该燃料电池的理论效率为(燃料电池的理论效率是指电池所产生的最大电能与燃料电池反应所能释放的全部能量之比).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据题意解答
(1)图1是1molNO2和1molCO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式: . 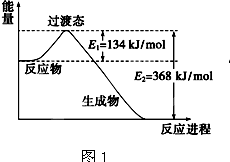
(2)观察图2a和b,根据盖斯定律,写出△H1、△H2、△H3、△H4、△H5和△H6的关系. 图a:;
图b: . 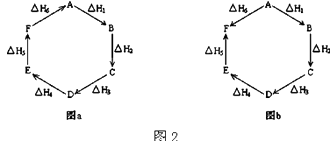
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在相同的密闭容器中,用高纯度纳米级Cu2O分别进行催化分解水的实验:2 H2O(g)![]() 2 H2(g) + O2(g) H>0,实验测得反应体系中水蒸气浓度(mol·L-1)的变化结果如下:
2 H2(g) + O2(g) H>0,实验测得反应体系中水蒸气浓度(mol·L-1)的变化结果如下:
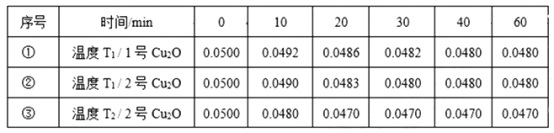
下列说法不正确的是
A. 实验时的温度T2高于T1
B. 2号Cu2O的催化效率比1号Cu2O的催化效率高
C. 实验①前20 min的平均反应速率v(O2) = 7×10ˉ5 mol·Lˉ1·minˉ1
D. 等质量纳米级Cu2O比微米级Cu2O催化效率高,这与Cu2O的粒径大小有关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生将一小块钠投入滴有酚酞的水中,此实验能证明钠下面4点性质中的( )
①钠比水轻 ②钠的熔点较低 ③钠与水反应在时要放出热量 ④钠与水反应后溶液呈碱性
A.①④B.①②④C.①③④D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应 A + 3B![]() 2C + 2D 在四种不同条件下的反应速率为:(1)v(A)=0.3mol/(L·s) (2)v(B)=0.6mol/(L·s) (3)v(C)=0.4mol/(L·s) (4)v(D)=0.45mol/(L·s),则该反应速率的快慢顺序为( )
2C + 2D 在四种不同条件下的反应速率为:(1)v(A)=0.3mol/(L·s) (2)v(B)=0.6mol/(L·s) (3)v(C)=0.4mol/(L·s) (4)v(D)=0.45mol/(L·s),则该反应速率的快慢顺序为( )
A. (2)>(4)>(3)>(1) B. (2)>(3)=(4)>(1)
C. (1)>(4)>(2)=(3) D. (4)>(3)>(2)>(1)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com