


| H2O |
| △ |
| H2O |
| △ |
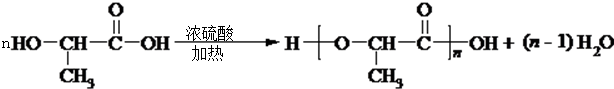
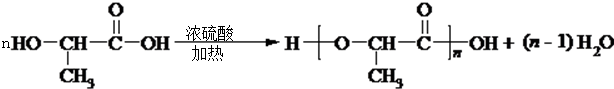
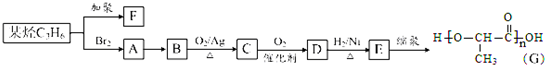
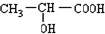 ,D和氢气发生加成反应生成E,则D的结构简式为
,D和氢气发生加成反应生成E,则D的结构简式为 ,C被氧化生成D,则C的结构简式为
,C被氧化生成D,则C的结构简式为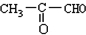 ,B氧化生成C,烃和溴发生加成反应生成溴代烃A,A发生水解反应生成醇B,根据C的结构简式知,B的结构简式为CH3CHOHCH2OH,
,B氧化生成C,烃和溴发生加成反应生成溴代烃A,A发生水解反应生成醇B,根据C的结构简式知,B的结构简式为CH3CHOHCH2OH, .
.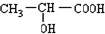 ,D和氢气发生加成反应生成E,则D的结构简式为
,D和氢气发生加成反应生成E,则D的结构简式为 ,C被氧化生成D,则C的结构简式为
,C被氧化生成D,则C的结构简式为 ,B氧化生成C,烃和溴发生加成反应生成溴代烃A,A发生水解反应生成醇B,根据C的结构简式知,B的结构简式为CH3CHOHCH2OH,
,B氧化生成C,烃和溴发生加成反应生成溴代烃A,A发生水解反应生成醇B,根据C的结构简式知,B的结构简式为CH3CHOHCH2OH, ,
, ,E的结构简式为
,E的结构简式为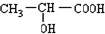 ,连接4个不同原子或原子团的碳原子是手性碳原子,与-OH相连的碳原子为手性碳原子,所以有1个手性碳原子,
,连接4个不同原子或原子团的碳原子是手性碳原子,与-OH相连的碳原子为手性碳原子,所以有1个手性碳原子, ;
;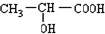 ,则D的结构简式为
,则D的结构简式为 ,D和氢气发生加成反应(或还原反应)生成E,
,D和氢气发生加成反应(或还原反应)生成E, ,C中官能团名称是醛基和羰基,
,C中官能团名称是醛基和羰基, ,H的D的同分异构体,符合下列条件:①与新制Cu(OH)2浊液共热,有砖红色沉淀产生说明含有醛基;
,H的D的同分异构体,符合下列条件:①与新制Cu(OH)2浊液共热,有砖红色沉淀产生说明含有醛基;| H2O |
| △ |
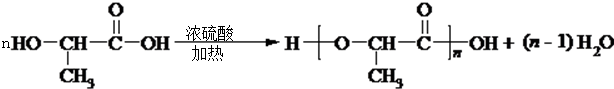
| H2O |
| △ |
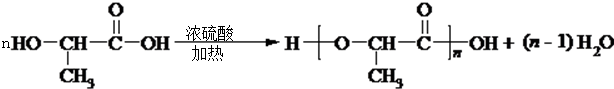 .
.

 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:

| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
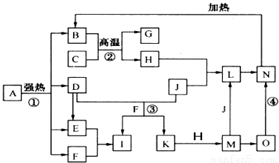
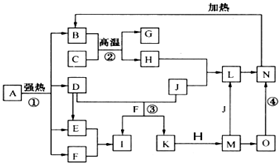 仔细阅读图,已知B、D、E、F、G是氧化物,其中D是形成酸雨的主要污染物,F、K是氢化物,且F在常温下为液态;C、H是日常生活中最为常见的金属单质,J是气态非金属单质,O是白色沉淀,且B、H、L、M、N、O中含有同种元素(图中部分反应物或产物已略去)请按要求回答:
仔细阅读图,已知B、D、E、F、G是氧化物,其中D是形成酸雨的主要污染物,F、K是氢化物,且F在常温下为液态;C、H是日常生活中最为常见的金属单质,J是气态非金属单质,O是白色沉淀,且B、H、L、M、N、O中含有同种元素(图中部分反应物或产物已略去)请按要求回答:
| ||
. |
| ||
. |
查看答案和解析>>
科目:高中化学 来源: 题型:

请按要求完成下列问题:
(1)L的化学式为___________。
(2)完成下列反应:
反应③的离子方程式:______________________________________________________,
反应④的化学方程式:______________________________________________________。
(3)反应②在工业生产上的用途是____________________________________________。
(4)反应①是分解反应,反应中生成的B、D、E、F的物质的量之比为1∶1∶1∶14,则反应①的化学方程式为 ________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
仔细阅读下图,已知B、D、E、F、G是氧化物,F、K是氢化物;C、H是日常生活中最为常见的金属单质,J是气态非金属单质,O是白色沉淀,且B、H、L、M、N、O中含有同种元素(图中部分反应物或产物已略去)。
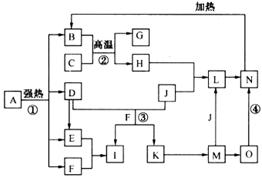
请按要求回答:
(1)反应①既是分解反应,又是氧化还原反应,产物B、D、E、F的物质的量之比1:1:1:14。A强热分解的化学反应方程式为 。
(2)写出反应②在工业生产上的一种用途: 。
(3)反应③的离子方程式为 ;
反应④的化学方程式为 。
(4)常以C或H制成容器盛装和运输I的浓溶液,其原理是
。
查看答案和解析>>
科目:高中化学 来源:2009-2010学年四川省眉山市仁寿县铧强中学高三(下)月考化学试卷(3月份)(解析版) 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com