
【题目】高铁酸钾(K2FeO4)是一种安全性很高的水处理剂,其合成的部分流程如下。
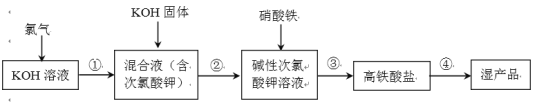
资料:
ⅰ.高铁酸钾可溶于水,微溶于浓KOH溶液,在碱性溶液中较稳定,在酸性或中性溶液中快速产生O2,且﹢3价铁能催化该反应。
ⅱ.次氯酸钾容易分解,2KClO![]() 2KCl+O2。
2KCl+O2。
(1)实验室使用高锰酸钾与浓盐酸制备氯气时,应选择下列装置中的_______。
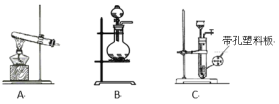
(2)写出步骤①的离子反应方程式_________________________________ 。
(3)加入KOH固体是为了过滤除盐,过滤除去的是__________________________________。
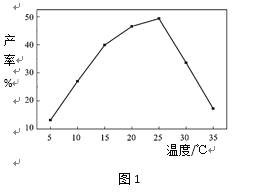
(4)相同投料比、相同反应时间内,反应温度对高铁酸钾产率的影响如图1所示:
请分析高铁酸钾产率随温度变化的原因:________________ 。
(5)相同投料比、相同反应时间内,硝酸铁浓度对产率的影响如图2所示:
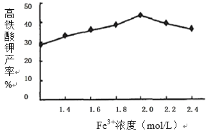
当Fe3+浓度大于2.0mol/L时,高铁酸钾产率变化的原因可能是:_________________________________________。
(6)高铁酸钾可用于除去水体中Mn(+2价),生成Mn(+4价)和Fe(+3价)。一定条件下,除去水体中1.1gMn(+2价),当去除率为90%时,消耗高铁酸钾的物质的量为______mol。
【答案】B ![]()
![]() 温度5℃≤T≤25℃时,温度升高速率加快,导致产率逐渐增加;T>25℃时,温度升高,次氯酸钾分解加剧,
温度5℃≤T≤25℃时,温度升高速率加快,导致产率逐渐增加;T>25℃时,温度升高,次氯酸钾分解加剧,![]() 浓度减小,反应速率减慢,导致产率下降 Fe3+的浓度过高催化了K2FeO4分解,导致产率下降 0.012
浓度减小,反应速率减慢,导致产率下降 Fe3+的浓度过高催化了K2FeO4分解,导致产率下降 0.012
【解析】
向KOH溶液中通入Cl2发生歧化反应生成KClO以及KCl,KCl对于后续合成高铁酸钾没有帮助,因此在第二步加入KOH固体时被除去;第三步,向溶液中加入硝酸铁,开始反应生成K2FeO4;题干中指出,高铁酸钾在碱性溶液中较稳定,在酸性溶液中会分解,并且Fe3+会催化该反应,因此,加硝酸铁时,量不能过多,避免Fe3+浓度过高,使K2FeO4分解;题干中还指出,KClO不稳定,因此在步骤三中,温度要控制得当,过低时反应速率太慢,过高时会加剧KClO分解,也不利于制备。
(1)浓盐酸与高锰酸钾反应制备Cl2,由于高锰酸钾易溶于水,所以可以认为是液体反应,因此装置A不可行;装置C中的塑料板也没有阻拦高锰酸钾的作用,C装置也不可行;故应选用B装置;
(2)第一步即向KOH溶液中通Cl2,发生的离子反应方程式为:![]() ;
;
(3)通过分析可知,第二步加KOH目的是除去KCl;
(4)通过分析可知,温度5℃≤T≤25℃时,温度升高速率加快,导致产率逐渐增加;T>25℃时,温度升高,次氯酸钾分解加剧,ClO-浓度减小,反应速率减慢,导致产率下降;
(5)通过分析可知,Fe3+的浓度过高催化了K2FeO4分解,导致产率下降;
(6)由题可知,K2FeO4除Mn(+2价)时,K2FeO4和Mn(+2价)的物质的量之比为2:3;去除率为90%时,水体中的1.1gMn(+2价)被去除了0.018mol,所以消耗的K2FeO4的物质的量为0.012mol。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】某有机化合物经李比希法测得其中含碳为54.5%、含氢为9.1%,其余为氧。用质谱法分析得知该有机物的相对分子质量为88。请回答下列有关问题:
(1)该有机物的分子式为___________.
(2)若该有机物在水溶液中呈酸性,且结构中不含支链,则其核磁共振氢谱峰面积之比为___________;该物质与乙酸相比,在水中的溶解度大的是___________(填名称),理由是___________。
(3)实验测得该物质不发生银镜反应,利用红外光谱仪测得该有机物分子的红外光谱如下图所示。

①该有机物的结构简式可能是___________、___________(写出两种即可)。
②写出其中一种与NaOH溶液反应的化学方程式___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组欲利用CuO与NH3反应,研究NH3的某种性质并测定其组成,设计了如下实验装置(夹持装置未画出)进行实验。请回答下列问题:

(1)仪器a的名称为______;仪器b中可选择的试剂为______。
(2)实验室中,利用装置A,还可制取的无色气体是______(填字母)。
A.Cl2 B.O2 C.CO2 D.NO2
(3)实验中观察到装置C中黑色CuO粉末变为红色固体,量气管有无色无味的气体,上述现象证明NH3具有______性,写出相应的化学方程式______。
(4)E装置中浓硫酸的作用______。
(5)读取气体体积前,应对装置F进行的操作:______。
(6)实验完毕,若测得干燥管D增重mg,装置F测得气体的体积为n L(已折算成标准状况),则氨分子中氮、氢的原子个数比为______(用含m、n字母的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙醇俗称酒精,在生活中使用广泛。
资料1:乙醇分子有两个末端,一端是憎水(易溶于油)的—C2H5;一端是亲水(易溶于水)的—OH。
资料2:破坏蛋白质分子中形成蜷曲和螺旋的各种力,使长链舒展、松弛,可导致蛋白质变性。
资料3:水分子可以松弛蛋白质外部亲水基团之间的吸引力,而—OH不能;—C2H5可以破坏蛋白质内部憎水基团之间的吸引力。
(1)乙醇的结构及性质
①1mol乙醇分子中的极性共价键有___________mol。
②从结构角度解释乙醇的沸点比乙烷高的原因____________________ 。
(2)乙醇的用途
①医用酒精(75%)制备过程与制酒的过程类似,不能饮用,但可接触人体医用。

结合题中资料,下列说法正确的是________________(填字母)。
a.糖化、发酵的过程均含有化学变化
b.获得医用酒精常采用的分离提纯方法是蒸馏
c.浓度99%的酒精消毒杀菌效果一定大于75%的酒精
②乙醇是一种很好的溶剂,在油脂的皂化反应中,加入乙醇可加快反应速率,其原因是 ______________ 。
(3)乙醇的工业制取
乙醇的工业制取方法很多,由碳的氧化物直接合成乙醇燃料已进入大规模生产。下图是由二氧化碳合成乙
醇的工艺流程。
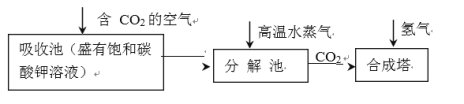
该流程中能循环使用的物质是_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下VL氨气溶解在1L水中(水的密度近似为1g/mL),所得溶液的密度为ρg/mL,质量分数为ω,物质浓度为c mol/L,则下列关系中不正确的是
A. ![]()
B. ![]()
C. ![]()
D. ![]() =1000Vρ/(17V+22400)
=1000Vρ/(17V+22400)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】次硫酸氢钠甲醛(NaHSO2·HCHO·2H2O)在印染、医药以及原子能工业中应用广泛,已知次硫酸氢钠甲醛具有强还原性,且在120 ℃以上发生分解。以Na2SO3、SO2、HCHO和锌粉为原料制备次硫酸氢钠甲醛的实验步骤如下:
步骤1:在烧瓶中(装置如图所示)加入一定量Na2SO3和水,搅拌溶解,缓慢通入SO2,至溶液pH约为4,制得NaHSO3溶液。
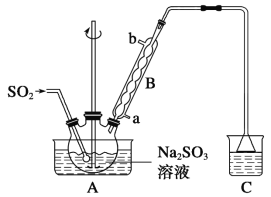
步骤2:将装置A中导气管换成橡皮塞。向烧瓶中加入稍过量的锌粉和一定量甲醛溶液,在80~90 ℃下,反应约3 h,冷却至室温,抽滤。
步骤3:将滤液真空蒸发浓缩,冷却结晶,抽滤。
(1)仪器B的名称为__________,装置A中通入SO2的导管末端是多孔球泡,其作用是:__________________________________________。
(2)装置C的作用是________________。
(3)①步骤2中,应采用何种加热方式____________,优点是________________;
②冷凝管中回流的主要物质除H2O外还有__________(填化学式)。
(4)步骤3中不在敞口容器中蒸发浓缩的原因是_____________________________。
(5)请写出步骤1中制取NaHSO3的化学方程式:_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A(C5H10O2)具有果香味,可用作食品加香剂,还可用作天然和合成树脂的溶剂。
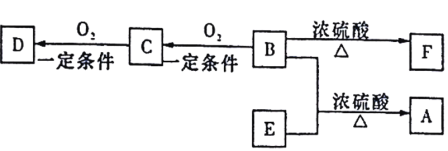
已知:①B、E分子中没有支链;
②D能与碳酸氢钠溶液反应放出二氧化碳;
③D、E具有相同官能团;E的相对分子质量比D大14;
④F是一种植物生长调节剂,能使溴的CCl4溶液褪色。
(1)B的化学名称为____________。D分子中所含的官能团的名称是____________。
(2)B与E生成A的反应类型是____________。
(3)写出F使溴的四氯化碳溶液褪色的化学反应方程式:________________________。
(4)A的结构简式为________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】MnO2是一种重要的无机功能材料,粗MnO2的提纯是工业生产的重要环节。某研究性学习小组设计了将粗MnO2(含有较多的MnO和MnCO3)样品转化为纯MnO2实验,其流程如图:

(1)第①步加稀H2SO4时,粗MnO2样品中的__(写化学式)转化为可溶性物质。
(2)第②步反应的离子方程式是_Mn2++_ClO3-+_H2O=_MnO2↓+_Cl2↑+_H+。
(3)第③步蒸发操作必需的仪器有铁架台(含铁圈)、酒精灯、__、__,已知蒸发得到的固体中有NaClO3和NaOH,则一定还含有__(写化学式)
(4)若粗MnO2样品的质量为12.69g,第①步反应后,经过滤得到8.7gMnO2,并收集到0.224LCO2(标准状况下),则在第②步反应中至少需要__molNaClO3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从煤和石油中可以提炼出化工原料A和B,A是一种果实催熟剂,它的产量可以用来衡量一个国家的石油化工发展水平。B是一种密度比水小的油状液体,B仅由碳、氢两种元素组成,碳元素与氢元素的质量比为12:1,B的相对分子质量为78。回答下列问题:
(1)A的电子式为______________,A的结构式为__________________。
(2)与A分子组成相差一个CH2原子团的A的同系物C与溴的四氯化碳溶液反应的化学方程式为_______________________,反应类型为_______________。
(3)在碘水中加入B振荡静置后的现象是_________________。
(4)B与浓硫酸、浓硝酸在50~60℃下反应的化学方程式为_____________,
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com