
| m |
| M |
| m |
| M |
| n |
| V |
| 500mL |
| 100mL |
| 0.15g |
| 40g/mol |
| 6×10-4g |
| 65g/mol |
| 9.23×10-6mol |
| 0.1L |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,1 mol水的体积约为22.4 L |
| B、含有2 mol氧原子的氧单质在标准状况下占有的体积一定是22.4 L |
| C、1 mol气体只有在标准状况下的体积才是22.4 L |
| D、标准状况下,2 L二氧化碳和3 L一氧化碳所含有的原子数目相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、核电站泄露的放射性物质131I和127I互为同位素,它们的化学性质相似 |
| B、纤维素、淀粉、蛋白质都是天然高分子化合物 |
| C、变质的油脂有难闻的特殊气味,是由于油脂发生了水解反应 |
| D、医药中常用酒精来消毒,是因为酒精能够使细菌蛋白质发生变性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Mg和Al |
| B、Al和Fe |
| C、Fe和Zn |
| D、Zn和Cu |
查看答案和解析>>
科目:高中化学 来源: 题型:
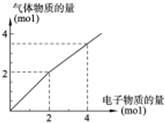 用惰性电极电解一定浓度的食盐水时,通过电子的物质的量与生成气体总物质的量的关系如图所示(不考虑氯气的溶解).若电解结束时,通过电子总物质的量为4mol,电解后恢复至常温,溶液的体积为2L,则混合气体中氢气的物质的量为
用惰性电极电解一定浓度的食盐水时,通过电子的物质的量与生成气体总物质的量的关系如图所示(不考虑氯气的溶解).若电解结束时,通过电子总物质的量为4mol,电解后恢复至常温,溶液的体积为2L,则混合气体中氢气的物质的量为查看答案和解析>>
科目:高中化学 来源: 题型:
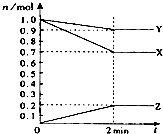 (1)某温度时,在2L容器中,X、Y、Z三种物质的物质的量随时间变化曲线如图所示.由图中数据分析,该反应的化学方程式为:
(1)某温度时,在2L容器中,X、Y、Z三种物质的物质的量随时间变化曲线如图所示.由图中数据分析,该反应的化学方程式为:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com