
【题目】高铁酸盐(如Na2FeO4)已经被广泛应用在水处理方面,以铁基材料为阳极,在高浓度强碱溶液中利用电解的方式可以制备高铁酸盐,装置如图。下列说法不正确的是

A. a为阳极,电极反应式为Fe—6e- +8OH- =FeO42- +4H2O
B. 为防止高铁酸根扩散被还原,则离子交换膜为阳离子交换膜
C. 在电解过程中溶液中的阳离子向a 极移动
D. 铁电极上有少量气体产生原因可能是4OH--4e-=O2↑+2H2O
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列对硫酸的叙述正确的是
A.因浓硫酸具有强氧化性,故不可用它来干燥氢气
B.浓硫酸可用铁铝容器存放是因为常温下浓硫酸不与这两种金属反应
C.浓硫酸有强氧化性,稀硫酸不具有氧化性
D.实验室中利用浓硫酸的高沸点性来制备HCl等气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.阅读下面短文。
原子核究竟是什么形状的呢?你也许会说,原子核应该是球形的吧。没错,对于大多数的原子而言,它们的原子核都是球形(如图1)或者比较接近球形的椭球形,就像橄榄球一样(如图2)。但是,科学家也发现极少数的原子核中的质子和中子会聚集成罕见的梨形(如图3)。

要想验证原子核是否为梨形,最直接的方法就是寻找不同核状态间的八极形变(octupole transition),这是梨形结构原子核特有的现象。利用这一手段,研究人员先后确认了224Ra、226Ra及其他一些重原子核均为梨形,但一直没有发现质量数小于200的梨形原子核。
近日,来自美国、英国和法国的一组科研团队制备了144Ba原子束,使其与铅箔发生碰撞并进入激发态。通过分析原子核产生的伽马射线光谱,研究人员发现几次八极形变的强度是核结构模型中预测数值的两倍多。由此,确认了144Ba的原子核也是梨形。
请回答下列问题:
(1)224Ra原子核的形状是_____________,224Ra和226Ra互称为____________。
(2)科学家确认144Ba的原子核是梨形,其根据是_____________(填字母)。
a.直接观察了144Ba原子核的形状 b.由核结构模型做出的理论计算 c.发现了八极形变现象
II.氧元素和硫元索组成的两种物质发生化学反应的微观示意图如图所示,其中●表示硫原子,O表示氧原子。

请回答下列问题:
(3)该反应的化学方程式是__________________________________。
(4)反应过程中,O2的浓度在5min内由5mol/L变成了1mol/L,用O2表示的化学反应速率是____________ mol·L-1·min-1。
(5)在等温等容条件下,该反应达到化学平衡状态的依据是___________(填字母)。
a.同一物质的正反应速率等于逆反应速率 b.混合气体的密度不变
c.混合气体中c(O2)不再改变 d.c(SO2)=c(O2)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语表示正确的是( )
A.Mg2+的结构示意图: 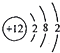
B.乙酸的结构简式:CH3CH2OH
C.硫酸钾的电离方程式:K2SO4═K2++SO ![]()
D.CO2的电子式:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用太阳能分解水制氢,若光解0.02mol水,下列说法正确的是( )
A.可生成H2的质量为0.02g
B.可生成氢的原子数为2.408×1023个
C.可生成H2的体积为0.224L(标准情况)
D.生成H2的量理论上等于0.04mol Na与水反应产生H2的量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列说法正确的是( )
A.1molCl2和足量的铁加热条件下反应,转移电子数一定为3NA
B.常温常压下,8.8g CO2和N2O的混合气体所含电子数为4.4 NA
C.常温下,PH=13的Ba(OH)2 溶液,0.1L,含OH﹣ , 0.02NA
D.1 L 1 mol/L的乙醇水溶液中含有氢原子总数为6NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在2 L恒容密闭容器中3种物质间进行反应,X、Y、Z的物质的量随时间的变化曲线如图所示,反应在t1 min 时达到平衡。
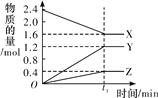
(1)请写出该反应的化学方程式:_____________________________。
(2)若上述反应中X、Y、Z分别为NH3、H2、N2,且已知1 mol 氨气分解成氮气和氢气要吸收46 kJ的热量,则至t1 min时,该反应吸收的热量为________;在此t1 min时间内,用H2表示该反应的平均速率v(H2)为__________。下列叙述能判断该反应达到平衡状态的是________(填字母代号)。
A.容器内各气体组分的质量分数不再发生改变
B.正反应速率与逆反应速率相等
C.容器内气体的密度不再发生改变
D.混合气体的平均相对分子质量不再发生改变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com