
分析 根据发生的反应有2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑、Na2CO3+2HCl═2NaCl+H2O+CO2↑、CO2+Ca(OH)2═CaCO3↓+H2O,以此来计算解答.
解答 解:设NaHCO3质量为x,Na2CO3质量为y,依题意得
2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑
168 106 44
x $\frac{106x}{168}$ $\frac{44x}{168}$
CO2+Ca(OH)2═CaCO3↓+H2O
44 100
$\frac{44x}{168}$ 1.0g
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 22.4
y+$\frac{106x}{168}$ 1.12
解得x=1.68g,y=4.24g,所以NaHCO3的物质的量为:$\frac{1.68g}{84g/mol}$=0.02mol,Na2CO3的物质的量为:$\frac{4.24g}{106g/mol}$=0.04mol,所以Na+的物质的量为0.02+0.04×2=0.1mol,所以Na+的数目为0.1NA 或 6.02x1022个,
故答案为:(1)1.68g;(2)0.1NA 或 6.02x1022个.
点评 本题考查学生利用化学反应方程式的计算,明确发生的化学反应是解答本题的关键,难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
 二氧化硫和氮的氧化物是大气的主要污染物,防止和治理其对环境的污染是当前环保工作的重要研究内容之一.
二氧化硫和氮的氧化物是大气的主要污染物,防止和治理其对环境的污染是当前环保工作的重要研究内容之一.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ①②③ | C. | ①③④ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 有大量的氯气泄漏时,用肥皂水浸湿软布蒙面,并迅速离开现场 | |
| B. | 金属钠着火燃烧时,用泡沫灭火器灭火 | |
| C. | 蒸馏操作时,加热到较高温度时,发现未加沸石,应立即打开瓶塞加入沸石 | |
| D. | 含硫酸的废液倒入水槽,用水冲入下水道 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 除去苯中的苯酚,可加浓溴水使苯酚生成三溴苯酚沉淀,滤去 | |
| B. | 将苯酚晶体置适量水中,待苯酚溶解一部分成饱和溶液后,仍残留无色晶体 | |
| C. | 苯酚的酸性比碳酸弱,所以它不能溶于Na2CO3溶液里 | |
| D. | 苯酚也可与硝酸发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
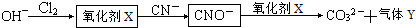
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(H+)=c(OH-)=1×10-6mol•L-1的溶液 | |
| B. | 等物质的量的强酸和强碱反应后所得到的混合溶液 | |
| C. | 将pH=5的盐酸稀释100倍所得到的溶液 | |
| D. | 非电解质溶于水得到的溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com