
【题目】t℃时Ag2CrO4在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是( )

A.加热蒸发饱和Ag2CrO4溶液再恢复到t℃,可使溶液由Y点变到Z点
B.在X点没有Ag2CrO4沉淀生成,则此时温度低于t℃
C.向饱和Ag2CrO4溶液中加入少量AgNO3固体,可使溶液由Z点到Y点
D.在t℃时,Ag2CrO4的Ksp为1×10-9
【答案】C
【解析】
试题分析:A.加热蒸发饱和Ag2CrO4溶液再恢复到t℃,沉淀析出后c(CrO42-)浓度不变,故A错误;B.在X点没有Ag2CrO4沉淀生成,则此时温度高于t℃,故B错误;C.向饱和Ag2CrO4溶液中加入少量AgNO3固体,溶解平衡逆向移动,c(CrO42-)浓度减小,可以使溶液由Z点到Y点,故C正确;D.依据 图象曲线上的数据结合溶度积常数概念计算得到;曲线上的点是沉淀溶解平衡,Ag2CrO4的沉淀溶剂平衡为:Ag2CrO4(s)2Ag+CrO42-,Ksp=c2(Ag+)c(CrO42-)=(10-3)210-6=10-12,故D错误;故答案为C。


 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案科目:高中化学 来源: 题型:
【题目】现有有机化合物A~E,其转化关系如图所示。

根据以上信息,回答下列问题:
(1)若A为氯代烃,质谱分析测得A的相对分子质量为92.5,且A的核磁共振氢谱图上有三个波峰,其面积之比为1:2:6,则A的结构简式为________,B中所含官能团的名称为________。
(2)请写出下列反应的化学方程式及反应类型。
①A→B:____________________________________________,
反应类型为___________________________________________。
②B+D→E:_________________________________________,
反应类型为__________________________________________。
(3)请写出有机物D的属于酯类的所有同分异构体的结构简式:___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下是由甲苯为起始原料的一系列变化,请填写下列空白:
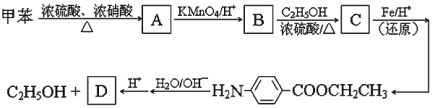
⑴ 写出化合物 B 的结构简式: 。
⑵ 由 B 到 C 的反应类型是 。
⑶ 任意写出两种同时符合下列要求的化合物 C 的同分异构体的结构简式(E、F、G 除外)。
① 化合物是1,4-二取代苯,其中苯环上的一个取代基是硝基;
② 分子中含有 -COO- 结构的基团。
![]()
![]()
![]()
⑷ E、F、G 中有一种化合物经酸性水解,其中的一种产物能与FeCl3溶液发生显色反应,这种化合物是 (在 E、F、G 中选择,填字母)。
⑸ 一定条件下,化合物 D 发生聚合反应的化学方程式是: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室以苯甲醛为原料制备间溴苯甲醛(实验装置主要部分见下图,相关物质的沸点见附表)。

附表相关物质的沸点(101kPa)

步骤1:将三颈瓶中的一定配比的无水AlCl3、1,2-二氯乙烷和苯甲醛充分混合后,升温至60℃,缓慢滴加经H2SO4干燥过的液溴,保温反应一段时间,冷却.
步骤2:将反应混合物缓慢加入一定量的稀盐酸中,_________________。
步骤3:有机相用10%NaHCO3溶液洗涤,再加入适量无水MgSO4固体,放置一段时间后过滤;
步骤4:减压蒸馏有机相,收集相应馏分。
(1)实验装置中可能的错误有______________,冷凝管进水口是______________;
(2)有同学建议将装置中温度计换成搅拌棒,那么温度计应移到什么地方使用______________;
(3)步骤2后续操作是_____________;
(4)步骤3中用10%NaHCO3溶液洗涤的具体操作是____________________,加入无水MgSO4固体的作用是______________。
(5)步骤4中采用蒸馏分离,请你预测蒸馏温度应先选择约_______℃,再选择约_______℃。
A.50 B.100 C.150 D.200 E.250 F.300
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积不变的密闭容器中进行反应:2SO2 (g)+O2(g)![]() 2SO3(g) ΔH<0。下列各图表示当其他条件不变时,改变某一条件对上述反应的影响,其中分析正确的是( )
2SO3(g) ΔH<0。下列各图表示当其他条件不变时,改变某一条件对上述反应的影响,其中分析正确的是( )

A. 图Ⅰ表示温度对化学平衡的影响,且甲的温度较高
B. 图Ⅱ表示t0时刻使用催化剂对反应速率的影响
C. 图Ⅲ表示t0时刻增大O2的浓度对反应速率的影响
D. 图Ⅳ中a、b、c三点中只有b点已经达到化学平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溴化钙可用于石油钻井,也可用于制造溴化铵及光敏纸、灭火剂、制冷剂等。制备CaBr22H2O的主要流程如下:

工业提取液溴主要采用空气吹出法,其主要流程如下:

请回答:
(1)Fe与液溴的反应温度不能超过40℃的原因是_________。
(2)试剂B最好选用_________。
(3)操作Ⅰ的步骤为蒸发浓缩、、________、洗涤、干燥。
(4)下列说法中错误的是_________。
a.滤渣A的成分可能是Fe、Fe(OH)2 、Fe(OH)3;
b.操作Ⅱ的名称是萃取
c.流程图中虚线框部分步骤的主要目的是除去杂质、富集Br2
d.成品溴中含有的少量Cl2,可加入Na2SO3溶液,然后分液除去
(5)制得的CaBr22H2O可以通过以下方法测定纯度:称取5.00 g样品溶于水,滴入足量Na2CO3溶液,充分反应后抽滤,将沉淀洗涤、烘干、冷却、称量,得到2.00 g固体。
①抽滤时用到的仪器除了安全瓶、抽气泵外,还需要_____________________________。
②抽滤中洗涤沉淀的操作方法是_________。
③以下关于抽滤的操作不正确的是________________
A.放在布氏漏斗内的滤纸大小应略小于漏斗内径,但又能将全部小孔盖住
B.过滤时,溶液量不应超过漏斗容量的2/3
C.吸滤瓶内液面将达到支管口时,应拔掉抽滤瓶上的橡皮管,从支管口处倒出溶液
D.停止吸滤时,应先拆下连接抽气泵和抽滤瓶的橡皮管,然后关闭水龙头
④测得CaBr22H2O的质量分数为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2可作为合成低碳烯烃的原料加以利用。如:2CO2(g)+6H2(g)![]() CH2=CH2(g)+4H2O(g) ΔH= a kJ·mol-1如图所示为在体积为1 L的恒容容器中,投料为3 mol H2和1 mol CO2时,测得的温度对CO2的平衡转化率和催化剂催化效率的影响。
CH2=CH2(g)+4H2O(g) ΔH= a kJ·mol-1如图所示为在体积为1 L的恒容容器中,投料为3 mol H2和1 mol CO2时,测得的温度对CO2的平衡转化率和催化剂催化效率的影响。

已知:H2和CH2=CH2的标准燃烧热分别是-285.8 kJ·mol-1和-1411.0 kJ·mol-1。H2O(g) ![]() H2O(l) ΔH=-44 kJ·mol-1
H2O(l) ΔH=-44 kJ·mol-1
请回答:
(1)a=__________kJ·mol-1。
(2)上述由CO2合成CH2=CH2的反应在____________下自发(填“高温”或“低温”),理由是____________。
(3)计算250 ℃时该反应平衡常数的数值K=____________。
(4)下列说法正确的是____________。
a.平衡常数大小:M>N
b.反应物活化分子百分数大小:M>N
c.其他条件不变,若不使用催化剂,则250℃时CO2的平衡转化率可能位于点M1
d.其他条件不变,若投料改为4 mol H2和1 mol CO2时,则250℃时CO2的平衡转化率可能位于点M2
e.当压强、混合气体的密度或n(H2)/n(CO2)不变时均可视为化学反应已达到平衡状态
(5)保持某温度(大于100℃)不变,在体积为V L的恒容容器中以n(H2)∶n(CO2)=3∶1的投料比加入反应物,至t0时达到化学平衡。t1时将容器体积瞬间扩大至2V L并保持不变,t2时重新达平衡。作出容器内混合气体的平均相对分子质量![]() 随时间变化的图像。
随时间变化的图像。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据要求完成下列各小题实验.(a、b为弹簧夹,加热及固定装置已略去)

(1)验证碳、硅非金属性的相对强弱。(已知酸性:亚硫酸>碳酸)
① 实验步骤:连接仪器、 、加药品后,打开a关闭b,然后滴入浓硫酸,加热;
② 铜与浓硫酸反应的化学方程式 ,装置A中的试剂是 ;
③ 能说明碳的非金属性比硅强的实验现象是 ;
(2)验证SO2的氧化性、还原性和酸性氧化物的通性。
① 在(1)②操作后打开b,关闭a ;
② H2S溶液中有浅黄色浑浊出现,化学方程式是 ;
③ BaCl2溶液中无明显现象,将其分成两份,分别滴加下列溶液,将产生的沉淀的化学式填入下表中相应位置。

写出其中SO2显示还原性生成沉淀的离子方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生用锌片、铜片、发光二极管、滤纸、导线等在玻璃片制成如图所示的原电池,当滤纸用醋酸溶液润湿时,二极管发光。下列有关该电池的说法正确的是( )

A.铜片上的电极反应:Cu2++2e﹣=Cu
B.电子通过溶液由锌片流向铜片
C.电池工作时电能直接转化为化学能
D.该电池工作时,若有16.25gZn被溶解,导线中转移0.50mol电子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com