
【题目】下列各组物质中,满足表中图示物质在通常条件下一步转化关系的组合只有( )
序号 | X | Y | Z | W |
|
① | CuO | Cu(OH)2 | CuSO4 | Cu | |
② | NaCl | NaHCO3 | Na2CO3 | NaOH | |
③ | Cl2 | Ca(ClO)2 | HClO | HCl | |
④ | SO2 | H2SO3 | Na2SO3 | NaHSO3 |
A.①②③
B.①③④
C.②③④
D.①②④
【答案】C
【解析】解:①CuO与水不反应,故①错误;②饱和NaCl溶液与二氧化碳、氨气反应可生成NaHCO3 , 为侯氏制碱法的反应原理,NaHCO3分解生成Na2CO3 , Na2CO3与氢氧化钙反应生成NaOH,NaOH与盐酸反应可生成NaCl,故②正确;
③氯气与氢氧化钙反应生成Ca(ClO)2 , Ca(ClO)2与酸反应生成HClO,HClO不稳定,见光分解可生成HCl,HCl被氧化可生成氯气,故③正确;
④二氧化硫与水反应生成亚硫酸,亚硫酸与氢氧化钠反应生成亚硫酸钠,亚硫酸钠与酸反应可生成NaHSO3、二氧化硫,故④正确.
故选C.
①CuO与水不反应;
②NaCl溶液与二氧化碳、氨气反应可生成NaHCO3 , NaHCO3分解生成Na2CO3 , Na2CO3与氢氧化钙反应生成NaOH,NaOH与盐酸反应可生成NaCl;
③氯气与氢氧化钙反应生成Ca(ClO)2 , Ca(ClO)2与酸反应生成HClO,HClO分解可生成HCl,HCl被氧化可生成氯气;
④二氧化硫与水反应生成亚硫酸,亚硫酸与氢氧化钠反应生成亚硫酸钠,亚硫酸钠与酸反应可生成NaHSO3、二氧化硫.


科目:高中化学 来源: 题型:
【题目】A、B、C、D均为中学所学的常见物质且均含有同一种元素,它们之间的转化关系如下图所示(反应条件及其他物质已经略去):A ![]() B
B ![]() C
C ![]() D.
D.
(1)若A、D的水溶液均呈酸性,且D为强酸.①则A、D分别为A: , D: . (填写化学式,下同)
②简述检验B物质的方法 .
③写出D的浓溶液和Cu在加热条件的化学方程式 .
(2)若A金属,D为强碱,则①C的化学式为 , 等物质的量的B和C中所含离子的物质的量(填写相等或不相等).
②在C→D的化学反应中,还原剂是 , 1摩尔C完全反应转移电子的物质的量为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)pH相同的下列溶液中:①NH4Cl ②(NH4)2SO4 ③NH4HSO4,c(NH4+)相对大小为(用序号回答)_______________。
(2)25℃时,将amol/L的氨水与0.01mol/L的盐酸溶液等体积混合,所得溶液呈中性。用含a的代数式表示一水合氨的电离平衡常数Kb=_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列溶液中,一定能够大量共存的离子组是( )
A.加入苯酚显紫色的溶液:Na+、Mg2+、Cl﹣、SO![]()
B.加入金属铝能放出大量H2的溶液:NH4+、K+、HCO![]() 、CH3COO﹣
、CH3COO﹣
C.使淀粉碘化钾试纸变蓝的溶液:Cu2+、Ba2+、S2﹣、I﹣
D.加入金属铁能放出大量H2的溶液:Na+、Al3+、ClO﹣、NO![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组欲制取氨气并探究其性质.请回答:
(1)实验室利用固体与固体反应制取氨气的化学方程式是 .
(2)①上图是进行氨气喷泉实验的装置,引发喷泉的操作步骤是 . ②氨气使烧杯中溶液由无色变为红色,其原因是(用方程式表示) .
(3)在上图的烧瓶中充满干燥气体,胶头滴管及烧杯中分别盛有液体.下列组合中不可能形成喷泉的是
A.HCl和H2O
B.NH3和H2O
C.NH3和苯
D.CO2和烧碱溶液.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据所学知识完成题目:
(1)将CO、O22种气体分别盛放在2个容器中,并保持2个容器内气体的温度和密度均相等,这2种气体对容器壁所施压强的大小关系是 .
(2)同温、同压下某瓶充满O2时重116克,充满CO2重122克,充满某气体时重114克.则某气体的相对分子质量为 .
(3)A物质按下式分解:2A=B↑+2C↑+2D↑,测得生成的混合气体在相同条件下的密度是H2密度的m倍,则A的摩尔质量为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒温恒容下,将2mol气体A和2mol气体B通入体积为2L的密闭容器中,发生如下反应:2A(g)+B(g)![]() xC(g)+2D(s),2min后反应达到平衡状态,此时剩余1.2mol B,并测得C的浓度为1.2mol/L。
xC(g)+2D(s),2min后反应达到平衡状态,此时剩余1.2mol B,并测得C的浓度为1.2mol/L。
(1)从开始反应到平衡状态,生成C的平均反应速率为__________。
(2)x=_________,该反应的化学平衡表达式为________________。
(3)A的转化率与B的转化率之比为________。
(4)下列各项可作为该反应达到平衡状态的标志是_______(填字母)。
A.压强不再变化 B.气体密度不再变化
C.气体平均相对分子质量不再变化 D.A的消耗速率与B的消耗速率之比为2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酸浸法制取硫酸铜的流程示意图如下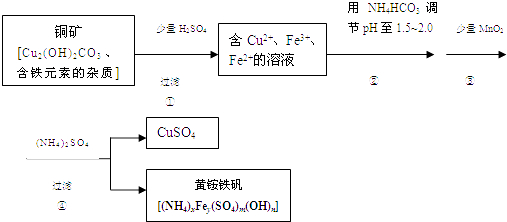
(1)步骤①中Cu2(OH)2CO3 发生反应的化学方程式为 .
(2)在步骤③发生的反应中,1mol MnO2转移2mol 电子,该反应的离子方程式为 .
(3)该小组为测定黄铵铁矾的组成,进行了如下实验:a.称取4.800g样品,加盐酸完全溶解后,配成100.00mL溶液A;
b.量取25.00mL溶液A,加入足量的KI,用0.2500molL﹣1Na2S2O3溶液进行滴定(反应方程式为I2+2Na2S2O3=2NaI+Na2S4O6),消耗30.00mLNa2S2O3溶液至终点.
b.量取25.00mL溶液A,加入足量的NaOH溶液充分反应后,过滤、洗涤、灼烧得红色粉末0.600g.
c.另取25.00mL溶液A,加足量BaCl2溶液充分反应后,过滤、洗涤、干燥得沉淀1.165g.
①用Na2S2O3溶液进行滴定时,滴定到终点的颜色变化为 △ .
②通过计算确定黄铵铁矾的化学式(写出计算过程).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com