
【题目】一种新型动力电池( LiFePO4电池)总反应式为Li1-xFePO4+LixC6![]() C6+LiFePO4,内部结构如图1所示,只有Li+通过聚合物隔膜。以此电池电解Na2SO4溶液(电极材料为石墨),可制得NaOH和H2SO4,其原理如图2所示。下列说法错误的是
C6+LiFePO4,内部结构如图1所示,只有Li+通过聚合物隔膜。以此电池电解Na2SO4溶液(电极材料为石墨),可制得NaOH和H2SO4,其原理如图2所示。下列说法错误的是

A. 电池放电时,LixC6在负极发生氧化反应
B. 电池放电时,正极反应式为 Lil-xFePO4+xLi-+xe-= LiFePO4
C. 电解时,图2的b电极反应式为2H2O-4e-=O2↑+4H+
D. 电解时,当转移0.2mol电子,A口产生气体的质量1.6g
【答案】D
【解析】
LiFePO4电池放电时,LixC6在负极上发生氧化反应,Li1-xFePO4在正极上发生还原反应。电解Na2SO4溶液可通过阴阳离子移向判断阴阳极。
A. 由电池的总反应可知,放电时, LixC6在负极上失电子发生氧化反应,A正确;
B.放电时,正极发生还原反应,电极反应式为Lil-xFePO4+xLi-+xe-= LiFePO4,B正确;
C.SO42-移向b极,说明b极为阳极,阳极发生失电子的氧化反应,电极反应为:2H2O-4e-=O2↑+4H+,C正确;
D.Na+移向a极,说明a极为阴极,阴极发生得电子的还原反应,电极反应为:2H2O+2e-=H2↑+2OH-,当转移0.2mol电子,产生氢气0.1mol,质量为0.2g;
答案:D。


科目:高中化学 来源: 题型:
【题目】砷及其化合物在半导体、农药制造等方面用途非常广泛。回答下列问题:
(1)ASH3的电子式为___;AsH3通入AgNO3溶液中可生成Ag, As2 O3和HNO3,该反应中氧化剂与还原剂的物质的量之比为___。
(2)改变O. 1 mol · L-1三元弱酸H3 AsO4溶液的pH,溶液中的H3 AsO4、H2 AsO4-、HAsO42-以及AsO43-的物质的量分布分数随pH的变化如图所示:

①1gKal ( H3 AsO4)=___;用甲基橙作指示剂,用NaOH溶液滴定H3 ASO4发生的主要反应的离子方程式为___
②反应H2 AsO4-+AsO43-=2HAsO42-的lgK=_____
(3)焦炭真空冶炼砷的其中两个热化学反应如下:
As2O3(g)+3C(s)=2As(g)+3CO(g) ![]() H1=akJ/mol
H1=akJ/mol
As2O3(g)+3C(s)=1/2As4(g)+3CO(g) ![]() H2=bkJ/mol
H2=bkJ/mol
则反应4As(g)=As4(g)![]() H=_______kJ/mol(用含a、b的代数式表示)。
H=_______kJ/mol(用含a、b的代数式表示)。
(4)反应2As2S3(s)=4AsS(g)+S2(g)达平衡时气体总压的对数值lg(p/kPa)与温度的关系如图所示:

①对应温度下,B点的反应速率v(正) ___v(逆)(填“>’,’’<”或“一”)。
②A点处,AsS(g)的分压为___kPa,该反应的Kp=___kPa5 (Kp为以分压表示的平衡常数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】t℃时,将3 mol A和2 mol B气体通人体积为2L的密闭容器中(容积不变),发生如下反应:3A(g)+B(g) ![]() 2C(g),2 min时反应达到平衡状态(温度不变),测得C的浓度为0.2 mol/L,请填写下列空白:
2C(g),2 min时反应达到平衡状态(温度不变),测得C的浓度为0.2 mol/L,请填写下列空白:
(1)该过程用A表示的反应速率为:v(A)=_______;该温度下该反应的化学平衡常数表达式为__________。
(2)比较达到平衡时,A、B两反应物的转化率:α(A)______α(B)(填“>”、“=”或“<”)。
(3)判断反应达到平衡状态的依据是(填字母序号)__________。
a.生成C的速率与消耗B的速率相等 b.混合气体的密度不变
c.混合气体的相对平均分子质量不变 d.A的质量分数不再发生变化
(4)若升高温度,再次达平衡时,平衡常数数值变大,则该反应的![]() H_____0(填“>”、“=”或“<”)。
H_____0(填“>”、“=”或“<”)。
(5)若保持温度不变时,继续向原平衡混合物的容器中通入少量氦气(氦气和A、B、C都不反应)后,则化学反应速率会__________(填“加快”、“减慢”或“不变”),化学平衡将_________(填“正反应方向移动”、“逆反应方向移动”或“不移动”)。
(6)在恒温恒容密闭容器中进行上述反应,起始投料时各物质的浓度如下表:
A | B | C | |
投料I | 3.0 mol/L | 1.0 mol/L | 0 |
投料II | 2.0 mol/L | 1.0 mol/L | 2.0 mol/L |
按投料I进行反应,测得达到化学平衡状态时A的转化率为40%,若按投料II进行反应,起始时反应进行的方向为________(填“正向”、“逆向”或“不移动)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高锰酸钾可以通过电解法进行制备,装置如图所示,下列说法错误的是
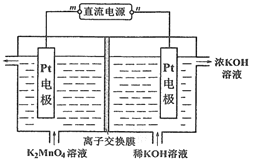
A. 阳极的电极反应式:MnO42- – e-= MnO4-
B. 该装置的离子交换膜为阳离子交换膜
C. 当电路通过a mol电子时,阴极室电解质溶液增加2a mol离子
D. 若电解流出液中KMnO4、K2MnO4和KOH物质的量之比为a∶b∶c,则流进电解池的电解液中K2MnO4和KOH的物质的量之比为 (a + b)∶( c + a )
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】菱锰矿的主要成分是MnCO3,还含有少量Fe、Al、Ca、Mg等元素。氯化铵焙烧菱锰矿制备高纯度碳酸锰的工艺流程如下:

已知:①相关金属离子[c0(Mn+)=0.1 mol/L]形成氢氧化物沉淀的pH范围如下:
金属离子 | Al3+ | Fe3+ | Fe2+ | Ca2+ | Mn2+ | Mg2+ |
开始沉淀的pH | 3.8 | 1.5 | 6.3 | 10.6 | 8.8 | 9.6 |
沉淀完全的pH | 5.2 | 2.8 | 8.3 | 12.6 | 10.8 | 11.6 |
②常温下,CaF2、MgF2的溶度积常数分别为1.46×10-10、 7.42×10-11
回答下列问题:
(1) “焙烧”时发生的主要反应的化学方程式为__________。气体X为________(填化学式),写出它生活中的一种用途_______________。
(2)焙烧时温度对锰浸出率的影响如图所示。焙烧时适应温度为_______________。

(3)浸出液“净化除杂”过程如下:首先用MnO2将Fe2+氧化为Fe3+,再调节溶液的pH将Al3+、Fe3+变成沉淀除去,溶液的pH的范围为____然后加入NH4F将Ca2+、Mg2+转化为CaF2、MgF2沉淀除去,两种沉淀共存时,溶液中![]() =________(所得结果保留两位小数)。
=________(所得结果保留两位小数)。
(4)碳化结晶的原理(用离子方程式表示): ______________________。
(5)将制得的高纯度碳酸锰溶于过量稀硫酸后用惰性电极电解,在某极得到重要的无机功能材料MnO2,该电极的电极反应式为_________。
(6)在该工艺流程中可以循环使用的物质有__________。(填化学式)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,0.1 mol/L H2A溶液中存在H2A、HA和A2-三种形态的粒子,其物质的量分数δ(x)随溶液PH变化的关系如图所示[已知δ(x)=c(X)/(C(H2A)+ C(HA-)+C(A2-)),下列说法不正确的是(图中a=1.35、b=4.17)

A. PH=7的溶液中C(Na+)=2[(C(A2-)+C(HA-)+C(H2A)]
B. 0.lmol/LNaHA溶液中C(OH-)+C(A2-)=C(H+)+C(H2A)
C. 已知Pka=-1gKa,则Pka2=4.17
D. PH=3的溶液中C(HA-)>C(A2-)+C(H2A)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物H可用于制备树脂、塑料和涂料等。其合成路线如下图所示:

已知:R—CH=CH2![]() RCH2CH2OH(其中B2H6为乙硼烷)
RCH2CH2OH(其中B2H6为乙硼烷)
请回答下列问题:
(1) 11.2 L(标准状况)的烃A在氧气中充分燃烧可以生成88 g CO2和45 g H2O。A的分子式是____________________。
(2)B和C在氢氧化钠的醇溶液中加热得到的有机物只有一种结构。B和C均为一氯代烃,它们的名称(系统命名)分别为_____________、_____________。
(3)在催化剂存在下1 mol F与2 mol H2反应,生成2甲基1丙醇。F的结构简式是_________________。其含有的官能团名称是_______________________。
(4)B→D,C→D的反应类型均为___________。请任写一个化学方程式_________________。
(5)写出F→G的化学方程式______________________________________________。
(6)写出E+G→H的化学方程式___________________________________________。
(7)写出与G具有相同官能团的G的所有同分异构体的结构简式_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高温下,超氧化钾晶体(KO2)呈立方体结构。如图为超氧化钾晶体的一个晶胞(晶体中最小的重复单元)。则下列有关说法正确的是( )

A. KO2中只存在离子键
B. 超氧化钾的化学式为KO2,每个晶胞含有1个K+和1个O2-
C. 晶体中与每个K+距离最近的O2-有6个
D. 晶体中,所有原子之间都以离子键相结合
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组在一个恒压密闭容器中加入CH3OH和CO气体,发生反应CH3OH(g) + CO(g) ![]() CH3COOH(l)。已知在某温度下,达到平衡时,CH3OH(g)、CO(g)、CH3COOH(l)的物质的量分别为0.08mol、0.10mol、0.12mol,且容器的体积刚好为2L。往上述已达到平衡的恒压容器中,再在瞬间通入0.12mol CH3OH和0.06molCO混合气体,平衡的移动方向为
CH3COOH(l)。已知在某温度下,达到平衡时,CH3OH(g)、CO(g)、CH3COOH(l)的物质的量分别为0.08mol、0.10mol、0.12mol,且容器的体积刚好为2L。往上述已达到平衡的恒压容器中,再在瞬间通入0.12mol CH3OH和0.06molCO混合气体,平衡的移动方向为
A. 正向 B. 逆向 C. 不移动 D. 无法确定
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com