
| A、向稀盐酸中滴加AgNO3溶液:Ag++HCl═AgCl↓+H+ |
| B、向醋酸溶液中滴加NaOH溶液:OH-+H+═H2O |
| C、向固体BaCO3中滴加稀硝酸:BaCO3+2H+═Ba2++H2O+CO2↑ |
| D、相同物质的量浓度的AlC13溶液与NaOH溶液等体积混合:Al3++4OH-═AlO2-+2 H2O |


 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案科目:高中化学 来源: 题型:
 用如图所示装置进行实验.实验过程中,两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清.查阅资料发现,高铁酸根(FeO42-)在溶液中呈紫红色.
用如图所示装置进行实验.实验过程中,两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清.查阅资料发现,高铁酸根(FeO42-)在溶液中呈紫红色.查看答案和解析>>
科目:高中化学 来源: 题型:

| 气体 | 氮气 | 氢气 | 氨 |
| 熔点(℃) | -210.01 | -252.77 | -77.74 |
| 沸点(℃) | -195.79 | -259.23 | -33.42 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| N2 |
| △ |
| H2O |
| H2O |
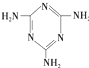 (三聚氰胺)
(三聚氰胺) ),三聚氰酸分子中N原子采取
),三聚氰酸分子中N原子采取 是电石的晶胞示意图,则一个晶胞中含有
是电石的晶胞示意图,则一个晶胞中含有查看答案和解析>>
科目:高中化学 来源: 题型:
| A、10mL水 |
| B、10mL 0.1mol/LCaCl2溶液 |
| C、20mL 0.1mol/LNaHSO4 |
| D、40mL 0.1mol/LNa2CO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①④ | B、④ | C、②③ | D、③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、锌为负极,锌发生还原反应Zn-2e-=Zn2+ |
| B、电流方向经外电路由锌到铜 |
| C、工作时SO42-离子向正极移动 |
| D、外电路电子流入的一极为正极,电子流出的一极为负极 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、3.6 mol |
| B、3.2 mol |
| C、2.4 mol |
| D、1.2 mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com