
【题目】25℃时,水的电离达到平衡:H2O![]() H++OH- △H>0 ,下列叙述正确的是( )
H++OH- △H>0 ,下列叙述正确的是( )
A.向水中加入少量固体硫酸氢钠(忽略溶液温度改变),c(H+)增大,Kw不变
B.向水中加入少量的CH3COONa(忽略溶液温度改变),平衡向右移动,c(H+)增大
C.向水中加入稀氨水,平衡向左移动,c(OH―)降低
D.将水加热,c(H+)增大,c(OH―)降低,Kw增大
【答案】A
【解析】
水电离生成氢离子、氢氧根离子,所以加入能电离出氢离子或氢氧根离子的物质抑制水电离,加入和氢离子或氢氧根离子反应的物质能促进水电离,温度不变,离子积常数不变,据此分析解答。
A.向水中加入硫酸氢钠固体,硫酸氢钠电离出氢离子导致溶液中c(H+)增大,温度不变Kw不变,故A正确;
B.水中加入醋酸钠,醋酸钠为强碱弱酸盐,醋酸根水解促进水的电离,平衡向右移动,但c(H+)减小,故B错误;
C.向水中加入稀氨水,一水合氨电离出OH-而导致溶液中c(OH-)增大,从而抑制水电离,平衡向左移动,故C错误;
D.水的电离是吸热过程,升高温度促进水电离,则Kw增大,c(H+)增大,c(OH―)也增大,故D错误;
故答案为A。


科目:高中化学 来源: 题型:
【题目】某课外活动小组的同学,在实验室做锌与浓硫酸反应的实验中,甲同学认为产生的气体是二氧化硫,而乙同学认为除二氧化硫气体外,还可能产生氢气。为了验证甲、乙两位同学的判断是否正确,丙同学设计了如图所示实验装置(锌与浓硫酸共热时产生的气体为X,且该装置略去),试回答下列问题:
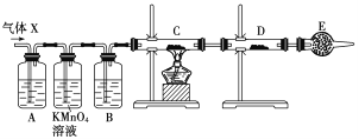
(1)上述反应中生成二氧化硫的化学方程式为______________________________。
(2)乙同学认为还可能产生氢气的理由是__________________________________。
(3)丙同学在安装好装置后,必不可少的一步操作是________________________。
(4)A中加入的试剂可能是_____,作用是__________________________________;B中加入的试剂可能是_____,作用是__________________________________;E中加入的试剂可能是_____,作用是__________________________________。
(5)可以证明气体X中含有氢气的实验现象是:C中:_________________________,D中:_________________________ 。如果去掉装置B,还能否根据D中的现象判断气体X中有氢气?_____ (填“能”或“不能”),原因是______________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列各装置图的叙述中,不正确的是

A.装置①中,d为阳极、c为阴极
B.装置②可用于收集H2、NH3、CO2、Cl2、NO2等气体
C.装置③中X若为四氯化碳,可用于吸收氨气,并防止倒吸
D.装置④可用于干燥、收集氨气,并吸收多余的氨气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】装置a、b、c中分别盛有试剂1、2、3,用如图所示的装置进行实验(夹持仪器略去,必要时可加热),能达到相应实验目的的是
选项 | 试剂1 | 试剂2 | 试剂3 | 实验目的 | 装置 |
A | 浓 | Cu片 | KI-淀粉溶液 | 验证 |
|
B | 盐酸 | 石灰石 | 饱和 | 制备 | |
C | 稀硫酸 | 溶液X | 澄清石灰水 | 验证溶液X中是否有 | |
D | 70%硫酸 |
| 酸性 | 证明 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下的定容容器中,当反应A(s)+2B(g)![]() C(g)+D(g)达到平衡状态后,下列哪些物理量不再发生变化,
C(g)+D(g)达到平衡状态后,下列哪些物理量不再发生变化,
①混合气体的压强 ②混合气体的密度 ③B的物质的量浓度 ④气体总物质的量 ⑤混合气体的平均相对分子质量 ⑥v(C)与v(D)
A. ②③⑤ B. ①②③ C. ②③④⑥ D. ①②③④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知氨气可以与灼热的氧化铜反应得到氮气和金属铜,用下图中的装置可以实现该反应。实验时C中粉末逐渐变为红色,D中出现无色液体。下列有关说法正确的是

A.反应中氧化剂和还原剂的物质的量之比为2∶3
B.装置D中液体可以使干燥的红色石蕊试纸变蓝
C.装置B中加入的物质可以是碱石灰或无水氯化钙
D.为防止装置D中发生倒吸,可以改用向下排空气法收集氮气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知有机物F和高分子N的合成路线如图所示:
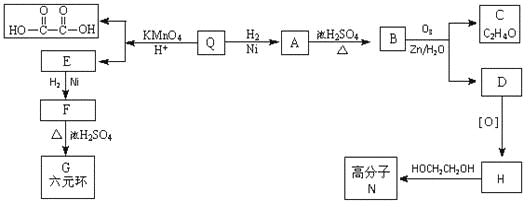
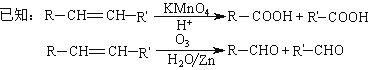
(1)Q只含碳、氢、氧三种元素,且其碳、氢、氧元素质量比为9:1:6 ,经测定Q的相对分子质量是128。1 mol Q可与1 mol Br2加成,并能与1 mol NaHCO3恰好完全反应,且分子中无支链。Q的分子式是________。
(2)A所含官能团的名称是______、_______;A→B的反应类型是_________;
(3)写出C与银氨溶液反应的化学方程式:____________;
(4)G的结构简式是_________;Q的反式结构简式是____________。
(5)下列说法正确的是___________。
A.C能与苯酚在一定条件下生成高分子化合物
B.D催化加氢的产物与F互为同分异构体
C.F能发生氧化反应、取代反应、加成反应
D.高分子N的每条分子链中含有(n-1)个酯基
(6)写出满足下列条件H的一种同分异构体的结构简式_______________________
①能与NaHCO3反应 ②能发生银镜反应 ③核磁共振氢谱有4个吸收峰
(7)写出H→N的化学方程式:_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上在恒容密闭容器中用下列反应合成甲醇:CO(g)+2H2(g)![]() CH3OH(g)△H
CH3OH(g)△H
(1)该反应的平衡常数表达式为_______;
(2)如表所列数据是反应在不同温度下的化学平衡常数(K)
温度 | 250℃ | 300℃ | 350℃ |
K | 2.041 | 0.270 | 0.012 |
①由表中数据判断该反应的△H______0(填“>”、“=”或“<”);
②某温度下,将2molCO和6molH2充入2L的密闭容器中,充分反应10s后达到平衡时测得c(CO)=0.2mol/L,则CO的转化率为____,用H2表示反应速率为_____,此时的温度为______;
(3)要提高CO的转化率,可以采取的措施是______;
a.升温 b.加入催化剂 c.增加CO的浓度
d.恒容充入H2 e.恒压充入惰性气体 f.分离出甲醇
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com