
����Ŀ�����й��ڵ������Һ��������ȷ����(����)
A. �����£�pH��7��NH4Cl�백ˮ�Ļ����Һ������Ũ�ȴ�С˳��Ϊ:c(Cl��)>c(NH![]() )>c(H��)��c(OH��)
)>c(H��)��c(OH��)
B. ��pH��4�Ĵ�����Һϡ�ͺ���Һ���������ӵ�Ũ�Ⱦ�����
C. �к�pH���������ͬ������ʹ�����Һ������NaOH�����ʵ�����ͬ
D. �����£�ͬŨ�ȵ�Na2S��NaHS��Һ��ȣ�Na2S��Һ��pH��
���𰸡�D
��������Aѡ�pH=7��NH4Cl�백ˮ�Ļ����Һ��c��H+��=c��OH���������ݵ���غ㣺 c��NH+4��+ c��H+��=c��OH����+c��Cl��������֪c��NH+4��= c��Cl��������ˮ�������ģ�������Һ������Ũ�ȴ�СΪ��c��Cl����=c��NH+4����c��H+��=c��OH��������A����Bѡ��������ӻ�������c��H+����c��OH�����ɷ��ȣ���������Һϡ����c��H+����С��c��OH��������B����Cѡ���ͬpH����������ᣬ�����Ũ�ȵ���H+Ũ�ȣ��������Ũ��Զ����H+Ũ�ȣ����д�������û�е��룬�������Ũ�ȴ�������Ũ�ȣ������ʱ����������NaOH���࣬��C����Dѡ�������ˮ��̶ȴ������������ˮ��̶ȣ���Һ����ǿ�������£�ͬŨ�ȵ�Na2S��NaHS��Һ��ȣ�Na2S��Һ��pH��D��ȷ����ѡD��


 ��������ܸ�ϰϵ�д�
��������ܸ�ϰϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й�����Ԫ�ص�˵����ȷ���ǣ� ��
A.Ԥ�ȵ���˿����������ȼ�գ������غ�ɫ������
B.��ԭ������Ũ���Ṳ�ȣ�������ʹƷ����Һ��ɫ������
C.��п��Ƥ�������⣬ԭ����ʹ������������������������
D.��ӡˢ��·��ķ�Һ�У������������ۣ����ٵ���KSCN��Һ�Ժ�ɫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��Ӧ2HI(g)![]() H2(g)+I2(g)�������仯��ͼ��ʾ������˵����ȷ����
H2(g)+I2(g)�������仯��ͼ��ʾ������˵����ȷ����

A. 0.2molHI��ַֽ⣬����1.25kJ����
B. ���������Ea������H����
C. �����������䣬�����¶�����Ӧ���ʼӿ���HI�ֽ��ʲ���
D. �����������䣬����ѹǿ����Ӧ���ʼӿ���HI�ֽ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ������ܴﵽʵ��Ŀ�ĵ��ǣ� ��
A. �ó���©��������������Ҵ���Ӧ�IJ���
B. �������ſ������ռ�ͭ����ϡ���ᷴӦ������![]()
C. �����Ȼ�����Һʱ�����Ȼ����ܽ��ڽ�Ũ���������ټ�ˮϡ��
D. ��![]() ��
��![]() �������ͨ������ʳ��ˮ�ɵõ�������
�������ͨ������ʳ��ˮ�ɵõ�������![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CH2=CHCl(����ϩ���е�-13.9C)�Ǿ��ȼ�ϩ�ĵ��塣ijѧϰС���������ױ������������Ȼ��������ȡ����ϩ���ش�����������
��1������ͬѧ�������װ���Ʊ��Ȼ����������

��װ��A��B�����Ʊ�����HCl��Ũ������ʾ��������_____������I��������_______��B�ĺ���װ�÷�������ʱ��������II���ֵ�������____________________��
��װ��C��O2ʱ������Ӧ�����ӷ���ʽΪ____________________��
��2������ͬѧ���ü����Ƶõ��Ȼ������������������װ����ȡ����ϩ��

��װ��D��������������������������������__________��____________��
��E�з�����Ӧ�Ļ�ѧ����ʽΪ______________________��
��װ��G��������______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ȸʯ��Ҫ�ɷ���Cu2(OH)2CO3,��������FeCO3��Si�Ļ����ʵ�����Կ�ȸʯΪԭ���Ʊ�����ͭ����IJ�������:
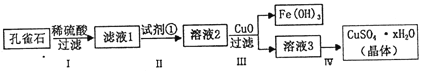
��1������I���漰����Ҫ��Ӧ�����ӷ���ʽ��ʾΪ___________.
��2�����������Լ�����_______(�����).
a.KMnO4 b.H2O2 c.Fe�� d.KSCN
��3������������CuO ��Ŀ����_________
��4���������������ͭ���壬��Ҫ����_____________��ȴ�ᾧ�����˵Ȳ���.
��5���ⶨ����ͭ����(CuSO4��xH2O)�нᾧˮ��xֵ:��ȡ2.41g����ͭ���壬��____(��ʵ����������)�м������������ٸı�ʱ��������ĩ������Ϊ1.6g.������x=______(��������ȷ��0.1)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ������������أ������й�˵����ȷ����( )
A.ά����C���л�ԭ�ԣ�������������������
B.���ࡢ�����ʡ���֬������Ȼ�߷��ӻ�����
C.ú��������Һ�����������仯���̣��ɱ�Ϊ�����Դ
D.����������ľ�����ά�����ڹ���ͨ�ŵĹ��ά�����������ǽ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D��E��F����Ԫ�أ�����A��B��C��D��EΪ����������Ԫ�أ�����֮��Ĺ�ϵ���£�
��ԭ�Ӱ뾶��A��C��B��E��D
��ԭ�ӵ�������������A=D��C=E��A+B=C
��ԭ�ӵĺ�����Ӳ�����B=C=2A��D=E
����BԪ�ص���Ҫ���ϼۣ��������+�����=2
V��F�ĵ��ʻ�Ͻ����������Ľ�������
��ش�
��1��������A��B����Ԫ�ذ�ԭ�Ӹ�����Ϊ3��1��ɵ����ʣ�������C��D����Ԫ�ذ�ԭ�Ӹ�����Ϊ1��2��ɵ����ʣ��õ���ʽ�ֱ��ʾ���ҵ��γɹ��̣�
�ף���
�ң� ��
��2��д����F�ĺ�ɫ������������BԪ�ص�����������Ӧ��ˮ�����ϡ��Һ��Ӧ�����ӷ���ʽ�� ��
��3������Ԫ��A��B��C��D��E��F������Ԫ�ؿ��γ�һ�ֳ������Σ������ø���������������ɣ������Ӹ�����Ϊ1��1��2���������Һ�м����ữ��BaCl2��Һ������ɫ����������NaOH��Һ�����ȣ�������ʹʪ��ĺ�ɫʯ����ֽ���������壬��ø��εĻ�ѧʽΪ����
��4���������������0.1L 0.1mol/L����Һ�������м���0.06mol BaCl2������ȫ��Ӧ����Һ��c��SO42����Ϊ����֪��������Һ����仯���ó�����KSP=2��10��9��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й����л������������ȷ���ǣ� ��
A. ʯ�͵ķ����ú���������Ƿ����˻�ѧ�仯
B. ������ˮ�����ۻ�Ͽ��Ƴ��屽
C. ���ࡢ��֬����������һ�������¾�����ˮ��
D. ʯ���ѻ�����ҪĿ�����������Һ��ȼ�ϵIJ���������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com