
ЁОЬтФПЁПФГЛЏбЇаЫШЄаЁзщЕФЭЌбЇгУШчЭМЫљЪОзАжУбаОПгаЙиЕчЛЏбЇЕФЮЪЬтЁЃЕББеКЯKЪБЃЌЙлВьЕНЕчСїБэЕФжИеыЗЂЩњСЫЦЋвЦЁЃ
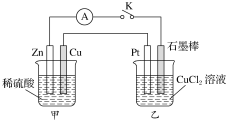
ЧыЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉМззАжУЕФУћГЦЪЧ________ЃЛввзАжУЕФУћГЦЪЧ________ЃЛZnМЋЮЊ________МЋЃЛPtМЋЮЊ______МЋЁЃ
ЃЈ2ЃЉаДГіЕчМЋЗДгІЪНЃКCuМЋ_____________ЃЛЪЏФЋАєМЋ____________ЁЃ
ЃЈ3ЃЉЕБМзжаВњЩњ![]() ЦјЬхЪБЃЌввжаЮіГіЭЕФжЪСПгІЮЊ________ЃЛввжаВњЩњЕФЦјЬхдкБъзМзДПіЯТЕФЬхЛ§гІЮЊ________ЁЃ
ЦјЬхЪБЃЌввжаЮіГіЭЕФжЪСПгІЮЊ________ЃЛввжаВњЩњЕФЦјЬхдкБъзМзДПіЯТЕФЬхЛ§гІЮЊ________ЁЃ
ЃЈ4ЃЉШєввжаШмвКВЛБфЃЌНЋЦфЕчМЋЖМЛЛГЩЭЕчМЋЃЌБеКЯKвЛЖЮЪБМфКѓЃЌввжаШмвКЕФбеЩЋ________ЃЈЬюЁАБфЩюЁБЁЂЁАБфЧГЁБЛђЁАЮоБфЛЏЁБЃЉЁЃ
ЃЈ5ЃЉШєввжаЕчМЋВЛБфЃЌНЋЦфШмвКЛЛГЩ![]() ШмвКЃЌБеКЯKвЛЖЮЪБМфКѓЃЌМзжаШмвКЕФpHНЋ________ЃЈЬюЁАдіДѓЁБЁЂЁАМѕаЁЁБЛђЁАВЛБфЁБЃЌЯТЭЌЃЉЃЛввжаШмвКЕФpHНЋ_______ЁЃ
ШмвКЃЌБеКЯKвЛЖЮЪБМфКѓЃЌМзжаШмвКЕФpHНЋ________ЃЈЬюЁАдіДѓЁБЁЂЁАМѕаЁЁБЛђЁАВЛБфЁБЃЌЯТЭЌЃЉЃЛввжаШмвКЕФpHНЋ_______ЁЃ
ЃЈ6ЃЉШєввжаЕчМЋВЛБфЃЌНЋЦфШмвКЛЛГЩБЅКЭ![]() ШмвКЃЌБеКЯKвЛЖЮЪБМфЃЌЕБвѕМЋЩЯга
ШмвКЃЌБеКЯKвЛЖЮЪБМфЃЌЕБвѕМЋЩЯга![]() ЦјЬхЩњГЩЪБЃЌЭЌЪБга
ЦјЬхЩњГЩЪБЃЌЭЌЪБга![]() ЮіГіЃЌМйЩшЮТЖШВЛБфЃЌЪЃгрШмвКжаШмжЪЕФжЪСПЗжЪ§гІЮЊ_____ЃЈгУКЌwЁЂaЕФДњЪ§ЪНБэЪОЃЌВЛБиЛЏМђЃЉЁЃ
ЮіГіЃЌМйЩшЮТЖШВЛБфЃЌЪЃгрШмвКжаШмжЪЕФжЪСПЗжЪ§гІЮЊ_____ЃЈгУКЌwЁЂaЕФДњЪ§ЪНБэЪОЃЌВЛБиЛЏМђЃЉЁЃ
ЁОД№АИЁПдЕчГи ЕчНтГи ИК бє ![]()
![]() 6.4g 2.24L ЮоБфЛЏ діДѓ діДѓ
6.4g 2.24L ЮоБфЛЏ діДѓ діДѓ ![]()
ЁОНтЮіЁП
(1)ZnЁЂCuКЭЯЁСђЫсПЩЙЙГЩдЕчГиЃЌЦфжаZnЪЧИКМЋЃЌCuЪЧе§МЋЃЛввзАжУЪЧЕчНтГиЃЌЪЏФЋАєЮЊвѕМЋЃЌPtЮЊбєМЋЃЛ
(2)CuМЋЩЯЗЂЩњЛЙдЗДгІЃЛЪЏФЋАєЩЯвВЗЂЩњЛЙдЗДгІЃЛ
(3)ЭЈЙ§МзЁЂввзАжУжаЕчзгЕФЮяжЪЕФСПЯрЕШЃЌЕБМзжаВњЩњ![]() ЪБЃЌЕчТЗжаЭЈЙ§
ЪБЃЌЕчТЗжаЭЈЙ§![]() ЕчзгЃЌввжаЮіГі
ЕчзгЃЌввжаЮіГі![]() КЭЗХГі
КЭЗХГі![]() ЃЛ
ЃЛ
(4)ШєНЋввжаСНИіЕчМЋЖМЛЛГЩЭЃЌдђввзАжУЯрЕБгкЕчНтОЋСЖЭЕФзАжУЃЌбєМЋШмНтЕФЭКЭвѕМЋЮіГіЕФЭвЛбљЖрЃЌШмвКжа![]() ЕФХЈЖШЛљБОВЛБфЃЛ
ЕФХЈЖШЛљБОВЛБфЃЛ
(5)ШєНЋввжаШмвКЛЛГЩNaClШмвКЃЌдђввзАжУОЭЪЧЕчНтБЅКЭЪГбЮЫЎЕФзАжУЃЌвђЗДгІЩњГЩСЫNaOH,ЙЪЕчНтКѓШмвКЕФpHдіДѓЁЃЗДгІЪБМзШмвКжаЯћКФСЫH![]() ЃЌШмвКЫсадМѕШѕЃЛ
ЃЌШмвКЫсадМѕШѕЃЛ
(6)ЕчНт![]() ШмвКЕФБОжЪЪЧЕчНтЫЎЃЌвѕМЋЩЯЮіГіЕФ
ШмвКЕФБОжЪЪЧЕчНтЫЎЃЌвѕМЋЩЯЮіГіЕФ![]() ЦјЬхЪЧ
ЦјЬхЪЧ![]() ЃЌдђЗДгІжага
ЃЌдђЗДгІжага![]() БЛЕчНтЃЌДЫ
БЛЕчНтЃЌДЫ![]() КЭЮіГіЕФ
КЭЮіГіЕФ![]() ЙЙГЩБЅКЭШмвКЃЌИУБЅКЭШмвКгыЪЃгрБЅКЭШмвКЕФШмжЪжЪСПЗжЪ§ЯрЭЌЁЃ
ЙЙГЩБЅКЭШмвКЃЌИУБЅКЭШмвКгыЪЃгрБЅКЭШмвКЕФШмжЪжЪСПЗжЪ§ЯрЭЌЁЃ
ЃЈ1ЃЉZnЁЂCuКЭЯЁСђЫсПЩЙЙГЩдЕчГиЃЌЦфжаZnЪЧИКМЋЃЌCuЪЧе§МЋЃЛввзАжУЪЧЕчНтГиЃЌЪЏФЋАєЮЊвѕМЋЃЌPtЮЊбєМЋЃЌ
Д№АИЮЊЃКдЕчГиЃЛЕчНтГиЃЛИКЃЛбєЃЛ
ЃЈ2ЃЉCuМЋЩЯЗЂЩњЛЙдЗДгІЃК![]() ЃЛЪЏФЋАєЩЯвВЗЂЩњЛЙдЗДгІЃК
ЃЛЪЏФЋАєЩЯвВЗЂЩњЛЙдЗДгІЃК![]() ЃЌ
ЃЌ
Д№АИЮЊЃК![]() ЃЛ
ЃЛ![]() ЃЛ
ЃЛ
ЃЈ3ЃЉЭЈЙ§МзЁЂввзАжУжаЕчзгЕФЮяжЪЕФСПЯрЕШЃЌЕБМзжаВњЩњ![]() ЪБЃЌЕчТЗжаЭЈЙ§
ЪБЃЌЕчТЗжаЭЈЙ§![]() ЕчзгЃЌввжаЮіГі
ЕчзгЃЌввжаЮіГі![]() КЭЗХГі
КЭЗХГі![]() ЃЌЩњГЩЭЕФжЪСПЮЊ0.1molЁС64g/mol=6.4gЃЌЩњГЩТШЦјБъзМзДПіЯТЕФЬхЛ§ЮЊ0.1molЁС22.4L/mol=2.24LЃЌ
ЃЌЩњГЩЭЕФжЪСПЮЊ0.1molЁС64g/mol=6.4gЃЌЩњГЩТШЦјБъзМзДПіЯТЕФЬхЛ§ЮЊ0.1molЁС22.4L/mol=2.24LЃЌ
Д№АИЮЊЃК6.4gЃЛ2.24LЃЛ
ЃЈ4ЃЉШєНЋввжаСНИіЕчМЋЖМЛЛГЩЭЃЌдђввзАжУЯрЕБгкЕчНтОЋСЖЭЕФзАжУЃЌбєМЋШмНтЕФЭКЭвѕМЋЮіГіЕФЭвЛбљЖрЃЌШмвКжа![]() ЕФХЈЖШЛљБОВЛБфЃЌШмвКЕФбеЩЋЛљБОВЛБфЁЃ
ЕФХЈЖШЛљБОВЛБфЃЌШмвКЕФбеЩЋЛљБОВЛБфЁЃ
Д№АИЮЊЃКЮоБфЛЏЃЛ
ЃЈ5ЃЉШєНЋввжаШмвКЛЛГЩ![]() ШмвКЃЌдђввзАжУОЭЪЧЕчНтБЅКЭЪГбЮЫЎЕФзАжУЃЌвђЗДгІЩњГЩСЫ
ШмвКЃЌдђввзАжУОЭЪЧЕчНтБЅКЭЪГбЮЫЎЕФзАжУЃЌвђЗДгІЩњГЩСЫ![]() ЃЌЙЪЕчНтКѓШмвКЕФpHдіДѓЁЃЗДгІЪБМзШмвКжаЯћКФСЫ
ЃЌЙЪЕчНтКѓШмвКЕФpHдіДѓЁЃЗДгІЪБМзШмвКжаЯћКФСЫ![]() ЃЌШмвКЫсадМѕШѕЃЌpHвВдіДѓЁЃ
ЃЌШмвКЫсадМѕШѕЃЌpHвВдіДѓЁЃ
Д№АИЮЊЃКдіДѓЃЛдіДѓЃЛ
ЃЈ6ЃЉЕчНт![]() ШмвКЕФБОжЪЪЧЕчНтЫЎЃЌвѕМЋЩЯЮіГіЕФ
ШмвКЕФБОжЪЪЧЕчНтЫЎЃЌвѕМЋЩЯЮіГіЕФ![]() ЦјЬхЪЧ
ЦјЬхЪЧ![]() ЃЌдђЗДгІжага
ЃЌдђЗДгІжага![]() БЛЕчНтЃЌДЫ
БЛЕчНтЃЌДЫ![]() КЭЮіГіЕФ
КЭЮіГіЕФ![]() ЙЙГЩБЅКЭШмвКЃЌИУБЅКЭШмвКгыЪЃгрБЅКЭШмвКЕФШмжЪжЪСПЗжЪ§ЯрЭЌЁЃдђЪЃгрШмвКжаШмжЪЕФжЪСПЗжЪ§
ЙЙГЩБЅКЭШмвКЃЌИУБЅКЭШмвКгыЪЃгрБЅКЭШмвКЕФШмжЪжЪСПЗжЪ§ЯрЭЌЁЃдђЪЃгрШмвКжаШмжЪЕФжЪСПЗжЪ§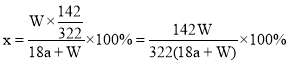
Д№АИЮЊЃК![]() ЁЃ
ЁЃ


 ИїЕиЦкФЉИДЯАЬибЕОэЯЕСаД№АИ
ИїЕиЦкФЉИДЯАЬибЕОэЯЕСаД№АИ аЁВЉЪПЦкФЉДГЙи100ЗжЯЕСаД№АИ
аЁВЉЪПЦкФЉДГЙи100ЗжЯЕСаД№АИ УћаЃУћЪІХргХзївЕБОМгКЫаФЪдОэЯЕСаД№АИ
УћаЃУћЪІХргХзївЕБОМгКЫаФЪдОэЯЕСаД№АИ
| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПNaOHБъзМШмвКЕФХфжЦКЭБъЖЈЃЌашОЙ§NaOHШмвКХфжЦЁЂЛљзМЮяжЪH2C2O42H2OЕФГЦСПвдМАгУNaOHШмвКЕЮЖЈЕШВйзїЁЃЯТСагаЙиЫЕЗЈе§ШЗЕФЪЧ

A.гУЭММзЫљЪОВйзїзЊвЦNaOHШмвКЕНШнСПЦПжа
B.гУЭМввЫљЪОзАжУзМШЗГЦЕУ0.1575gH2C2O42H2OЙЬЬх
C.гУЭМБћЫљЪОВйзїХХГ§МюЪНЕЮЖЈЙмжаЕФЦјХн
D.гУЭМЖЁЫљЪОзАжУвдNaOHД§ВтвКЕЮЖЈH2C2O4ШмвК
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПФГНігЩЬМЁЂЧтЁЂбѕШ§жждЊЫизщГЩЕФгаЛњЛЏКЯЮяЃЌОВтЖЈЦфЯрЖдЗжзгжЪСПЮЊ90ЁЃШЁгаЛњЮябљЦЗ1.8 gЃЌдкДПбѕжаЭъШЋШМЩеЃЌНЋВњЮяЯШКѓЭЈЙ§ХЈСђЫсКЭМюЪЏЛвЃЌСНепЗжБ№діжи1.08 gКЭ2.64 gЁЃЪдЧѓИУгаЛњЮяЕФЗжзгЪНЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПNaNO2ЪЧвЛжжАзЩЋЛђЮЂЛЦЩЋаБЗНОЇЬхЃЌвзШмгкЫЎЃЌЮЂШмгкввДМЁЃФГаЃЭЌбЇЩшМЦЪЕбщжЦБИNaNO2ВЂЬНОПЦфаджЪЁЃЛиД№ЯТСаЮЪЬтЃК
(1)МззщЭЌбЇвРОнЗДгІNa2CO3+NO+NO2=2NaNO2+CO2ЃЌВЂРћгУЯТСазАжУжЦБИЩйСПКЌNaNO2ЕФШмвКЁЃ(EжабѕЦјЩдЙ§СП)
A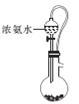 B
B![]() C
C![]() D
D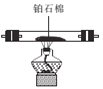 E
E![]() F
F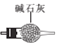
Ђйе§ШЗЕФСЌНгЫГађЃКAЁЊFЁЊEЁЊ ___ЁЊ ___ЁЊ___ ЁЊЮВЦјДІРэЁЃ(ЬюзжФИ)
ЂкзАжУAЕФЩеЦПжаЪЂЗХЕФЮяжЪЪЧ____(ЬюУћГЦ)ЃЌCзАжУЕФзїгУЪЧ ___ЁЃ
(2)ввзщЭЌбЇвРОнЗДгІPb+NaNO3![]() NaNO2+PbO(ФбШмгкЫЎ)ЃЌВЂАДЯТСаЪЕбщСїГЬжЦБИNaNO2ЃК
NaNO2+PbO(ФбШмгкЫЎ)ЃЌВЂАДЯТСаЪЕбщСїГЬжЦБИNaNO2ЃК
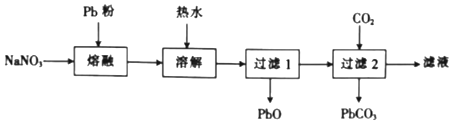
ЂйЁАШлШкЁБЪБгУPbЗлДњЬцЧІСЃЕФФПЕФЪЧ____ЁЃ
ЂкгЩЁАЙ§ТЫ2ЁБЕФТЫвКЕУЕНNaNO2ОЇЬхЛЙашОЙ§ЕФОпЬхВйзїЮЊ____ЁЂ____ЁЂЙ§ТЫЁЂгУввДМЯДЕгКѓИЩдяЁЃ
(3)БћзщЭЌбЇЬНОПNaNO2ЕФаджЪЃЌШЁЩйСПввзщжЦЕУЕФNaNO2ШмгкЫЎжЦЕУNaNO2ШмвКЁЃ
ЂйШЁЩйСПNaNO2ШмвКгкЪдЙмжаЃЌЕЮШыбЮЫсЫсЛЏЃЌдйМгШыKIКЭЕэЗлШмвКЃЌеёЕДЃЌШмвКБфРЖЃЌЫЕУїNaNO2Опга____(ЬюЁАбѕЛЏадЁБЛђЁАЛЙдадЁБ)ЁЃ
ЂкЯђЫсадKMnO4ШмвКжаЕЮШыNaNO2ШмвКЃЌШмвКзЯЩЋж№НЅЭЪШЅЃЌЗЂЩњЗДгІЕФРызгЗНГЬЪНЮЊ____(MnO4-БЛЛЙдЮЊMn2+)ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЮЂЩњЮяЕчГиЪЧжИдкЮЂЩњЮяЕФзїгУЯТНЋЛЏбЇФмзЊЛЏЮЊЕчФмЕФзАжУЃЌЦфЙЄзїдРэШчЭМЫљЪОЁЃЯТСагаЙиЮЂЩњЮяЕчГиЕФЫЕЗЈДэЮѓЕФЪЧ

A.е§МЋЗДгІжагаCO2ЩњГЩ
B.ЮЂЩњЮяДйНјСЫЗДгІжаЕчзгЕФзЊвЦ
C.жЪзгЭЈЙ§НЛЛЛФЄДгИКМЋЧјвЦЯђе§МЋЧј
D.ЕчГизмЗДгІЮЊC6H12O6+6O2=6CO2+6H2O
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПдквЛЖЈЮТЖШЯТЃЌЯђБљДзЫсжаМгЫЎЯЁЪЭЃЌШмвКЕМЕчФмСІБфЛЏЧщПігвЭМЫљЪОЃЌЛиД№ЯТСаЮЪЬтЁЃ
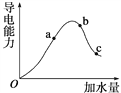
ЃЈ1ЃЉЁАOЁБЕуЪБвКЬхВЛФмЕМЕчЃЌЫЕУїДзЫсжа________РызгМќ(ЬюЁАКЌгаЁБЛђЁАВЛКЌЁБ)ЁЃ
ЃЈ2ЃЉaЁЂbЁЂcШ§ЕуДзЫсЕчРыГЬЖШгЩДѓЕНаЁЕФЫГађЮЊ________ЃЛaЁЂbЁЂcШ§ЕуЖдгІЕФШмвКжаc(HЃЋ)зюДѓЕФЪЧ________ЁЃ
ЃЈ3ЃЉвЊЪЙcЕуШмвКжаc(CH3COOЃ)діДѓЖјc(HЃЋ)МѕаЁЃЌПЩВЩШЁЕФСНжжДыЪЉЪЧ______________ЁЃ
ЃЈ4ЃЉШєЪЕбщВтЕУcЕуДІШмвКжаc(CH3COOH)ЃН0.1 molЁЄLЃ1ЃЌc(CH3COOЃ)ЃН0.001 molЁЄLЃ1ЃЌдђИУЬѕМўЯТCH3COOHЕФЕчРыГЃЪ§KaЃН________ЁЃ
ЃЈ5ЃЉдкЯЁЪЭЙ§ГЬжаЃЌЫцзХДзЫсХЈЖШЕФНЕЕЭЃЌЯТСаЪМжеБЃГждіДѓЧїЪЦЕФСПЪЧ________________
AЃЎc(HЃЋ) BЃЎHЃЋИіЪ§
CЃЎCH3COOHЗжзгЪ§ D.![]()
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПвНвЉАЂЫЙЦЅСжЕФНсЙЙМђЪНШчЭМЁЃЪдЛиД№ЃК
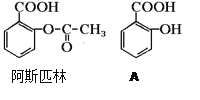
(1)АЂЫЙЦЅСжПЩПДГЩѕЅРрЮяжЪЃЌПкЗўКѓдкЮИГІзїгУЯТЃЌАЂЫЙЦЅСжЗЂЩњЫЎНтЗДгІЃЌЩњГЩAКЭBСНжжВњЮяЁЃЦфжаAЕФНсЙЙМђЪНШчЭМЃЌдђАЂЫЙЦЅСжЕФЗжзгЪНЮЊЃК______________BЕФНсЙЙМђЪНЮЊЃК_______BжаЕФЙйФмЭХЪЧЃК______________ЃЈУћГЦЃЉ
ЂЦЩЯЪіЫЎНтВњЮяBгыМзДМЁЂХЈСђЫсЙВШШЗДгІЕФЛЏбЇЗНГЬЪНЮЊЃК_____________________________________________________
ЂЧ МзДМдкЭзїДпЛЏМСЪБгыбѕЦјЗДгІЕФЛЏбЇЗНГЬЪНЮЊЃК______________________________
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПФІАнЕЅГЕПЩРћгУГЕРКДІЕФЬЋбєФмЕчГиАхЯђжЧФмЫјжаЕФяЎРызгЕчГиГфЕчЃЌяЎРызгЕчГиЗДгІдРэЮЊ Li1ЃxCoO2+LixC6![]() LiCoO2+6CЃЌзАжУЪОвтЭМШчЭМЫљЪОЁЃЯТСаЫЕЗЈДэЮѓЕФЪЧ
LiCoO2+6CЃЌзАжУЪОвтЭМШчЭМЫљЪОЁЃЯТСаЫЕЗЈДэЮѓЕФЪЧ

A.ГфЕчЪБЃЌвѕМЋжЪСПдіМгЃЌЗЂЩњЛЙдЗДгІ
B.ГфЕчЪБЃЌЕчТЗжаУПга 1 mol ЕчзгЭЈЙ§ЃЌдђга 1 mol Li+ЭЈЙ§ОлКЯЮяЕчНтжЪФЄ
C.ИУяЎРызгЕчГиЗХЕчЪБЃЌЛЏбЇФмзЊЛЏЮЊЕчФм
D.ЗХЕчЪБЃЌе§МЋЕФЕчМЋЗДгІЪНЮЊ LiCoO2-xe-=Li1-xCoO2+xLi+
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПККЛЦмЫЫиЪЧДЋЭГжаВнвЉЛЦмЫЕФгааЇГЩЗжжЎвЛЃЌЖджзСіЯИАћЕФЩБЩЫгаЖРЬизїгУЁЃЯТСагаЙиККЛЦмЫЫиЕФа№Ъіе§ШЗЕФЪЧ(вбжЊЭЊЛљжЛгыЧтЦјМгГЩЃЌгыBr2ВЛЗДгІЃЉЃЈ ЃЉ
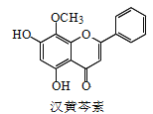
A.ККЛЦмЫЫиЕФЗжзгЪНЮЊC16H13O5
B.ИУЮяжЪгіFeCl3ШмвКЯдЩЋ
C.1molИУЮяжЪгыфхЫЎЗДгІЃЌзюЖрЯћКФ1molBr2
D.гызуСПH2ЗЂЩњМгГЩЗДгІКѓЃЌИУЗжзгжаЙйФмЭХЕФжжРрМѕЩй1жж
ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com