
����Ŀ����15mL0.lmol��L-1KOH��Һ����μ���0.2mol��L-1������Һ����ҺpH�ͼ�����ᣨ���ᣩ�������ϵ������ͼ��ʾ�����й�ϵ��ȷ���ǣ� ��

A. ��B�㣺c(K+)=c(HCOO-)��c(OH-)=c(H+)����a=7.5
B. ��A��B������һ�㣬c(HCOO-)��c(K+)��c(OH-)��c(H+)
C. ��D�㣺c(HCOO-)+c(HCOOH)��2c(K+)
D. B��C�Σ�ˮ�ĵ���̶���������С
���𰸡�C
��������
A��B����Һ�����ԣ���c��OH-��=c��H+�����������ǿ�������Σ�Ҫʹ��Һ�����ԣ�������ʵ���Ӧ�������ڼ����a��7.5��A����B����A��B������һ�㣬��Ϊ��ʼʱc��OH-����c��HCOO-������Ҳ�п�����c��K+����c��OH-����c��HCOO-����c��H+����B����C��D�����������������������ʵ���Ϊ0.02L��0.2mol/L��0.004mol��KOH�����ʵ���Ϊ0.015L��0.1mol/L=0.0015mol����Ӧ��c��CH3COO-��+c��CH3COOH����2c��K+����C��ȷ��D���������Ϸ�����֪B������������B��C��ˮ�ĵ���̶���С��D����ѡC��


 ��ҵ����ϵ�д�
��ҵ����ϵ�д� ͬ��ѧ��һ�ζ���ϵ�д�
ͬ��ѧ��һ�ζ���ϵ�д� �����ܾ�ϵ�д�
�����ܾ�ϵ�д� ���ƿ�����ϵ�д�
���ƿ�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ�ӷϾ���ͨп�̵���������л����Ʊ�KMnO4�����ʵ�һ�ֹ���(�����ǷϾɵ����ʵ�ʴ��ڵ�������������)��

��1��KMnO4ϡ��Һ��һ�ֳ����������������������������������Ƶ���__________(�����)��
A.˫��ˮ B.75%�ƾ� C.84����Һ(NaClO��Һ) D.����
��2���ٺ�ɫ��������ˮ��ʱΪ��߽������ʣ������õĴ�ʩΪ___________________________�����һ�����ɣ���
������ˮϴ���պ������һ�ֺ�ɫ�Ļ��������a�еõ��ۿ����Ҫ�ɷ���K2MnO4��KCl���ù����з�����Ӧ�Ļ�ѧ����ʽΪ_____________________________________��
��ͼ�в���A��һ��������ˮ�ĺ�ɫ���壬�仯ѧʽΪ_________________________��
��3���ⶨKMnO4��Ʒ�Ĵ��ȿ��ñ�Na2S2O3��Һ���еζ���
������250 mL0.100 0 mol��L-1��Na2S2O3��Һ����Ҫʹ�õIJ����������ձ�����ͷ�ιܡ���Ͳ��_________________________��_________________________��
��ȡKMnO4�����Һ���ữ������0.100 0 mol��L-1��Na2S2O3��Һ���еζ����жϵζ����յ������Ϊ___________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ��������ԭ��Ӧ����(����)
A. CaCO3![]() CaO��CO2��
CaO��CO2��
B. CH4��2O2![]() 2H2O��CO2
2H2O��CO2
C. Na2CO3��2HCl��2NaCl��H2O��CO2��
D. 2NaOH��H2SO4��Na2SO4��2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�о�С������BaS�Ļ�ԭ���ᴿHBr��Һ������ȡ�廯þ�ķ���������

��1�� ����ԭ��������BaS���˹���̫���ԭ����______��
��2�������ijɷ���______��
��3���ᾧ��õ�MgBr2��6H2O���Ҵ�ϴ�ӣ���ϴ��Һ�л����Ҵ���ʵ�鷽����______��
��4��������ͼװ�ý�MgBr2��6H2O��ˮ�õ�MgBr2��

��ͨ��HBr��Ŀ����______��
��ͼ�п���װ�õ�������______��
��5����֪��BaS+H2O2��Ba(OH)2+S�����벹������ʵ������BaS��ȡ�ߴ�BaSO3��ʵ�鷽����ȡBaS��ˮ�������߽�����ڽ���Һ�м������H2O2�����ˣ�______����ʵ������ʹ�����Լ��У�SO2���壬����SO2��ˮ����������������ʹ���������У���ո����䡢pH�ƣ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͼ���к������������Һ�����������������ɳ����������������������ͼ���ܶ�Ӧ������������
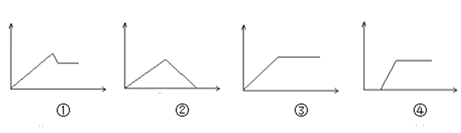
A. ͼ�ٿ�����MgCl2��AlCl3��Һ��μӰ�ˮ������
B. ͼ�ڿ�����AlCl3��Һ��μ�NaOH��Һ������
C. ͼ�ۿ�����NaAlO2��Һ�μ�ϡ����������
D. ͼ�ܿ����Ǻ�һ����HCl��AlCl3��Һ��μӰ�ˮ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ�����ֵ�������й�������ȷ����
A. ��״���£�11.2L14CO2���е�������Ϊ11NA
B. 5.6gFe��������S�ۼ��ȳ�ַ�Ӧת�Ƶĵ�����Ϊ0.2NA��
C. 1molNa2O2����������������ĿΪ4NA
D. 1LpH=6�Ĵ�ˮ�к���OH������ĿΪ10-8NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ��ʾ,�밴Ҫ��ش���������

��1����K1���ϲ�K2.AΪ___________(����������")�����ڸõ缫�ɹ۲쵽��������__________��B���ĵ缫��ӦΪ______________________������0.4mol����ת��ʱ,������ͭ������Ϊ____ g.
��2����K2,�ϲ�K1��AΪ_______(��������������)�����ڸõ缫�ɹ۲쵽��������___________��B���ĵ缫��ӦΪ____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ũ�Ⱦ�Ϊ0.1mol/L��MgCl2��Һ����ˮ��Һ���������1:2��ϡ���֪Mg(OH)2��Ksp=4.0��10��12������˵����ȷ����
A�����ǰ����ˮ��Һ��c(NH4+)��c(OH��)=1��1
B����Ϻ�c(NH4+)��c(Cl��)=1��1
C����Ϻ�c(Mg2+)��c(OH��)= 4.0��10��12
D�����Ϻ�ķ�ɢϵ�м���FeCl3��Һ����ɫ��������ɫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)��һ�������£�CO(g)+H2O(g)![]() CO2(g)+H2(g)����������Ϊ2L���ܱ��������Բ�ͬ����̼��[n(H2O)/n(CO)]����H2O(g)��CO��CO��ƽ��ת���ʦ�(CO)���¶ȵĹ�ϵ����ͼ��ʾ��
CO2(g)+H2(g)����������Ϊ2L���ܱ��������Բ�ͬ����̼��[n(H2O)/n(CO)]����H2O(g)��CO��CO��ƽ��ת���ʦ�(CO)���¶ȵĹ�ϵ����ͼ��ʾ��

��R��ƽ�ⳣ��K=__________________��
����̼��X_________2.0(�>����<����=��)���жϵ�������______________��
�����������COƽ��ת���ʵĴ�ʩ��_________��
A��ʹ�ø�Ч���� B��ͨ��He����ʹ��ϵ��ѹǿ����
C�����ͷ�Ӧ�¶� D��Ͷ�ϱȲ��䣬���ӷ�Ӧ���Ũ��
(2)��֪����ӦI��4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g) ��H<0
4NO(g)+6H2O(g) ��H<0
��ӦII��4NH3(g)+3O2(g)![]() 2N2(g)+6H2O(g) ��H<0
2N2(g)+6H2O(g) ��H<0
��������ʱ�ᷢ����������������ӦI�͢�Ϊ�����ô����Ը÷�Ӧ��ѡ���ԣ���1L�ܱ������г���1molNH3��2molO2����Ӧ��ϵ��ͼ���ô����ڸ���ʱѡ��Ӧ_________(�I����II��)��520��ʱ��4NH3(g)+3O2(g)![]() 2N2(g)+6H2O(g)��ƽ�ⳣ��K=_______(ֻ���г����ּ���ʽ)��
2N2(g)+6H2O(g)��ƽ�ⳣ��K=_______(ֻ���г����ּ���ʽ)��

(3)�����������(S2O42-)Ϊ���ʣ�ʹ�ü�ӵ绯ѧ���ɴ���ȼú�����е�NO��װ����ͼ��ʾ��

���������ĵ缫��ӦʽΪ___________��
��NO����ת�������Ҫ����ΪNH4+����ͨ��ʱ��·��ת����0.3mol e-�����ͨ����������������յ�NO�ڱ�״���µ����Ϊ___________mL��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com